
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Аминокислоты
|
|
Работу выполнила: Мальцева Валерия
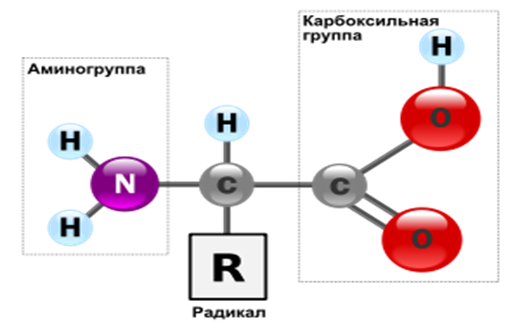
Аминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водорода заменены на аминные группы.
История:
Первая аминокислота — аспарагин — была открыта в 1806, последняя из аминокислот, обнаруженных в белках, — треонин — была идентифицирована в 1938. Каждая аминокислота имеет тривиальное (традиционное) название, иногда оно связано с источником выделения. Например, аспарагин впервые обнаружили в аспарагусе (спарже), глутаминовую кислоту — в клейковине (от англ. gluten — глютен) пшеницы, глицин был назван так за его сладкий вкус (от греч. glykys — сладкий).
История открытия К началу XIX столетия появляются первые работы по химическому изучению белков. Уже в 1803 г. Дж. Дальтон дает первые формулы белков - альбумина и желатина - как веществ, содержащих азот. В 1810 г. Ж. Гей-Люссак проводит химические анализы белков - фибрина крови, казеина и отмечает сходство их элементного состава. Решающее значение для понимания химической природы белков имело выделение при их гидролизе аминокислот. Вероятно, первым это сделал А. Браконно в 1820 г., когда, действуя на белки серной кислотой, при кипячении он получил «клеевой сахар», или гликокол (глицин), при гидролизе фибрина из мяса - лейцин и при разложении шерсти - также лейцин и смесь других продуктов гидролиза. Первой открытой аминокислотой был, видимо, аспарагин, выделенный Л. Вокленом из сока спаржи Asparagus (1806). В это же время Ж. Пруст получил лейцин при разложении сыра и творога. Затем из продуктов гидролиза белка были выделены многие другие аминокислоты.
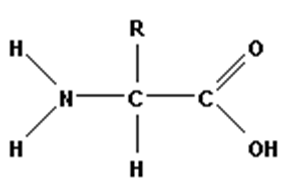 общая формула аминокислот
общая формула аминокислот
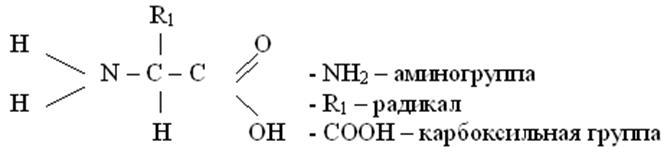
Физические свойства:
По физическим свойствам аминокислоты резко отличаются от соответствующих кислот и оснований. Все они кристаллические вещества, лучше растворяются в воде, чем в органических растворителях, имеют достаточно высокие температуры плавления; многие из них имеют сладкий вкус. Эти свойства отчётливо указывают на солеобразный характер этих соединений. Особенности физических и химических свойств аминокислот обусловлены их строением — присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной и основной. α-аминокислоты являются амфотерными электролитами.
Химические свойства:
Все аминокислоты — амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы —COOH, так и основные свойства, обусловленные аминогруппой —NH2. Аминокислоты взаимодействуют с кислотами и щелочами:
NH2 —CH2 —COOH + HCl → HCl • NH2 —CH2 —COOH (хлороводородная соль глицина)
NH2 —CH2 —COOH + NaOH → H2O + NH2 —CH2 —COONa (натриевая соль глицина)
Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов, то есть находятся в состоянии внутренних солей.
NH2 —CH2COOH Equilibrium rl.svg N+H3 —CH2COO-
Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.
Этерификация:
NH2 —CH2 —COOH + CH3OH → H2O + NH2 —CH2 —COOCH3 (метиловый эфир глицина)
Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков, нейлона, капрона.
Реакция образования пептидов:
HOOC —CH2 —NH —H + HOOC —CH2 —NH2 → HOOC —CH2 —NH —CO —CH2 —NH2 + H2O
Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов.
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO−. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот. Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе.
Получение:
1. Действие аммиака на галоидзамещенные жирные кислоты:
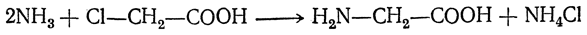
Чтобы свести к минимуму нежелательное образование иминодиуксусной кислоты по реакции
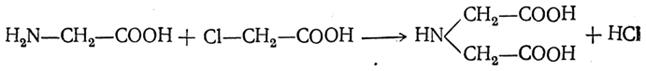
реакцию ведут с очень большим избытком аммиака или в присутствии карбоната аммония, который защищает аминогруппу. Образующееся карбаминовое производное аминокислоты
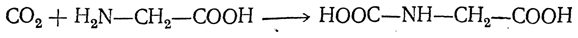
легко разлагается при нагревании.
2. Получение из циангидринов альдегидов и кетонов (циангидринный метод). Важной реакцией получения α-аминокислот является действие аммиака на циангидрины альдегидов и кетонов
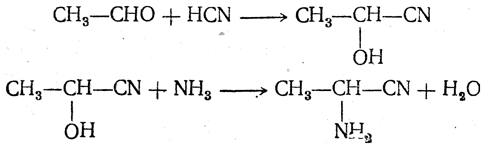
с последующим омылением аминонитрила в аминокислоту:
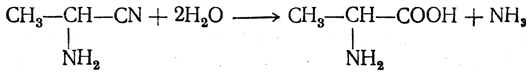
Аминонитрилы можно получить также, действуя на альдегиды или кетоны непосредственно цианистым аммонием. Эта реакция приобрела особое значение после того, как Н. Д. Зелинский с сотрудниками показали, что синильную кислоту и аммиак или цианистый аммоний можно заменить смесью водных растворов хлористого аммония и цианистого калия, в результате обменного разложения дающих цианистый аммоний, который и вступает в реакцию с альдегидами или кетонами:

3. Синтезы из сложных эфиров, содержащих подвижный атом водорода. Большое значение приобрели синтезы аминокислот из малонового, циануксусного и ацетоуксусного эфиров. Пользуясь этими методами, можно получить аминокислоты, содержащие различные радикалы.
а) Синтез из малонового эфира. Из малонового эфира получают нитрозомалоновый эфир, который восстанавливают в аминомалоновый эфир водородом в присутствии катализатора или цинком в кислой среде:

Защитив аминогруппу ацетилированием
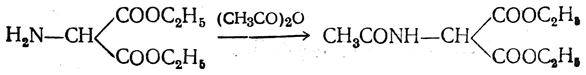
полученный ацетиламиномалоновый эфир алкилируют, действуя на него последовательно металлическим натрием и галоидным алкилом:
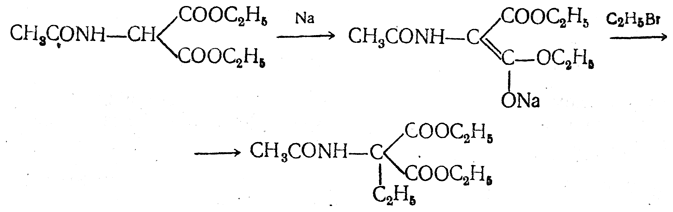
После омыления и декарбоксилирования получается α-аминокислота:
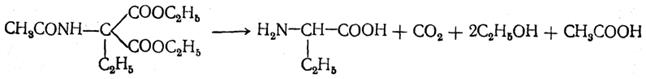
б) Синтез из циануксусного эфира проводится аналогично синтезу из малонового эфира.
в) Синтез из ацетоуксусного эфира. При действии на однозамещенные ацетоуксусные эфиры раствором фенилдиазотата, а затем щелочью отщепляется уксусная кислота и образуется неустойчивое азосоединение, которое изомеризуется в фенилгидразон соответствующей кетокислоты:
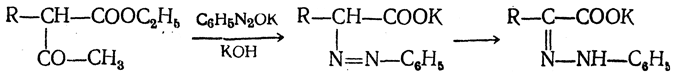
Восстановление фенилгидразона кетокислоты цинком в солянокислой спиртовой среде приводит к α-аминокислоте:
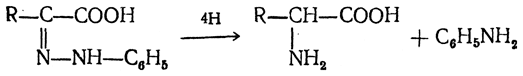
Этот метод синтеза аминокислот предложен В. В. Феофилактовым.
Date: 2015-08-06; view: 1340; Нарушение авторских прав