
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Классификация окислительно-восстановительных реакций. Основой для классификации ОВР служит местоположение окислителя и восстановителя
|
|
Основой для классификации ОВР служит местоположение окислителя и восстановителя.
1. Межатомные (а) или межмолекулярные (б) ОВР. Окислитель и восстановитель входят в состав разных веществ.
а) 2 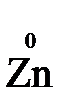 +
+ 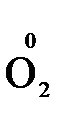 = 2
= 2 
б)  + 2
+ 2 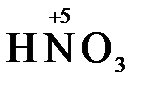 =
= 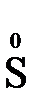 + 2
+ 2 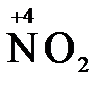 + 2H2O
+ 2H2O
2. Внутримолекулярные ОВР. Окислитель и восстановитель входят в состав одного вещества.
2 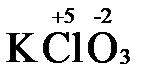 = 2
= 2 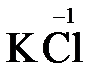 + 3
+ 3 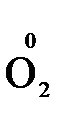
3. Реакции диспропорционирования (дисмутации, самоокисления-самовосстановления). Окислителем и восстановителем являются атомы одного и того же элемента, находящиеся в промежуточной степени окисления и входящие в состав одного вещества. Часть атомов повышает свою степень окисления, а другая часть ее понижает.
3 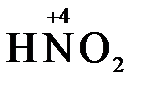 =
= 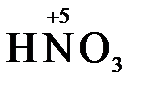 + 2
+ 2 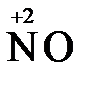 + H2O
+ H2O
4. Реакции конпропорционирования – это реакции, в которых атомы одного и того же элемента имеют разные степени окисления, переходят к промежуточной степени окисления.
Реакции конпропорционирования могут быть:
а) внутримолекулярными (в соединении имеется элемент с разными степенями окисления):
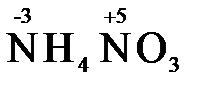 =
= 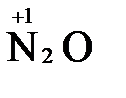 + 2 H2O
+ 2 H2O
б) межмолекулярными (в разных соединениях имеется один и тот же элемент с разными степенями окисления)
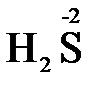 +
+ 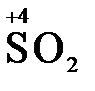 ® 3 S0 + 2 H2O
® 3 S0 + 2 H2O
Date: 2015-07-27; view: 429; Нарушение авторских прав