
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Тройные соударения и тримолекулярные реакции
|
|
В качестве элементарных реакций в газовой фазе тримолекулярные соударения не являются распространёнными, поскольку даже в хаотических броуновских движениях очень мала вероятность одновременных столкновений трёх частиц. Вероятность тримолекулярной стадии резко возрастает, если она протекает на границе раздела фаз, и фрагменты поверхности конденсированной фазы оказываются её участниками. За счёт подобных реакций часто создаётся основной канал изъятия у активных частиц избыточной энергии и их исчезновения в сложных превращениях.
Рассмотрим тримолекулярное превращение вида: 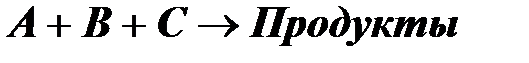
Качественная модель последовательных бимолекулярных соударений:
1. А + В → АВ АВ + С → Продукты
2. А + С → АС АС + В → Продукты
3. С + В → СВ СВ + А→ Продукты
Основное допущение основано на детальном равновесии на первой стадии:
Квазиравновесный режим образования бимолекулярных комплексов
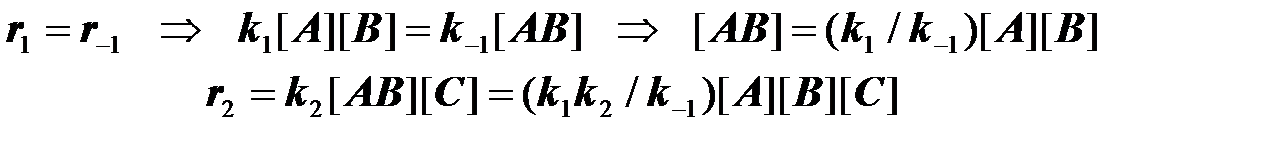
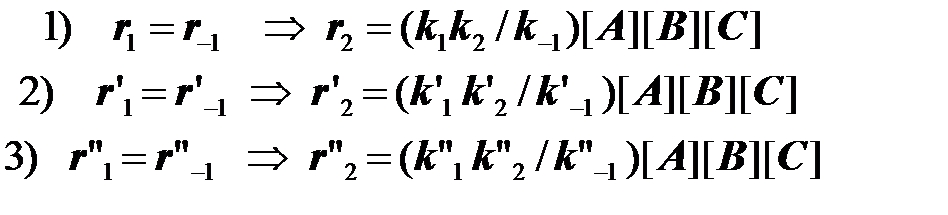
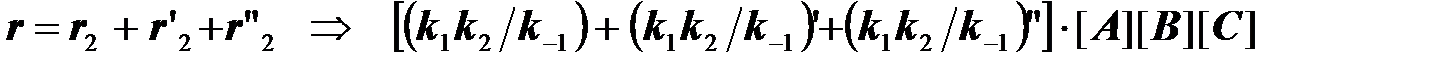

Результирующая константа скорости должна принять вид:

Комбинация трёх энергий активации создаёт формальное разнообразие возможных вариантов механизма (рис. 1).
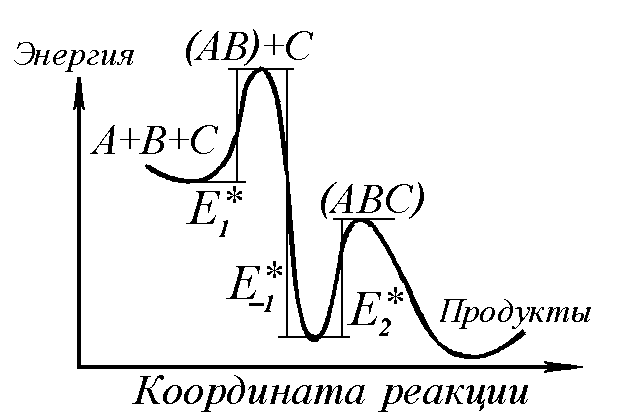
Рисунок 1 "Зависимость энергии активации от координаты реакции"
При этом «наблюдаемая» энергия активации тримолекулярной реакции может оказаться и отрицательной величиной.
Для реакции:
2NO + O2 → 2NO2
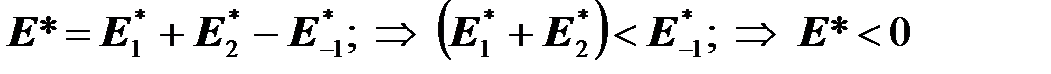
Подобная трактовка тримолекулярных реакций принадлежит Траутцу. Её не следует переоценивать. Это лишь качественная теория. Она не в состоянии объяснить все особенности таких реакций. Это возможно лишь на основе ТАК, которая не ограничена лишь вышеприведенным простейшим выводом, и требует значительно более глубокого анализа на основе статистической механики.
Тримолекулярная реакция валентно-ненасыщенных частиц:
2NO + O2 → 2NO2
2NO + Cl2 → 2NOCl
2NO + H2 → N2O + H2O
Cтехиометрические уравнения баланса вовсе не обязаны соответствовать схеме элементарных актов.
Тримолекулярными являются также очень важные реакции рекомбинации валентно-насыщенных частиц в превращениях типа:
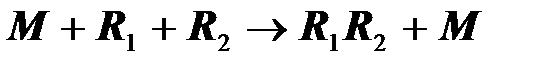 ,
,
где R1, R2- обладающие свободной валентностью атомы или молекулярные свободные радикалы, а M - любая третья частица. С формально-кинетической точки зрения всякий такой процесс выглядит как процесс второго порядка, и третья частица не учитывается в материальном балансе и не определяет стехиометрию процесса.
Её функция состоит только лишь в отводе избытка энергии от образующейся частицы
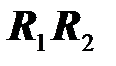
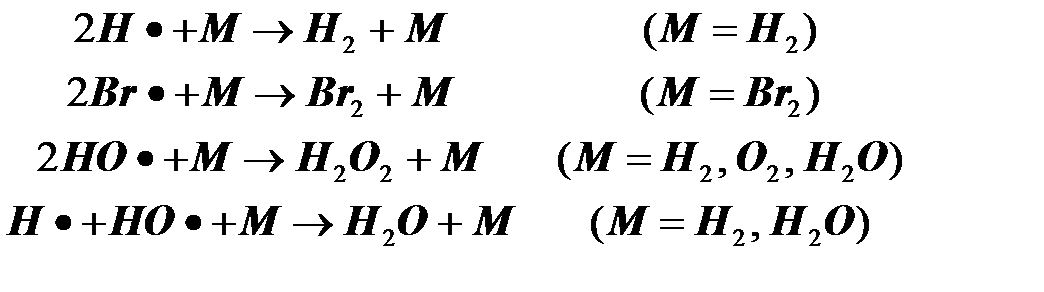
Тримолекулярные процессы подобного рода протекают на стенках сосуда, и символом M будут уже обозначены центры соударения на стенке. Их присутствие без специальных приёмов не обнаружимо, и роль этих стадий будет замаскирована в виде концентрационных сомножителей в эффективных константах скоростей. Роль таких стабилизирующих тройных столкновений тем выше, чем более эффективно они способны отводить выделяющуюся избыточную энергию, а она тем выше, чем больше атомов в молекуле третьей частицы M. Это вызвано тем, что с увеличением размера частицы растёт число колебательных степеней свободы, и за счёт именно их возбуждений растёт вероятность отвода энергии на межатомные связи молекулы M от вновь образуемой молекулы продукта [6].
Date: 2015-07-27; view: 893; Нарушение авторских прав