
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

IV.7. Гидрогенолиз галогенопроизводных
|
|
Гидрогенолиз связи С-галоген является важным методом дегалогенирования органических соединений. Устойчивость к гидрогенолизу возрастает в следующем ряду: иодо- ˂ бромо- ˂ хлоро- ˂ фторопроизводные. Иодо- и бромоалканы легко восстанавливаются на скелетном никелевом катализаторе в присутствии гидроксида калия для связывания галогеноводорода при температуре 250 С и атмосферном давлении. Хлориды в этих условиях гидрогенолизуются медленнее, многие из них на платиновых, родиевых и никелевых катализаторах при 250 С не восстанавливаются. Алкилфториды гидрировать даже в жестких условиях не удается.
В ненасыщенных галогенопроизводных восстановительное дегалогенирование протекает особенно легко, если атом галогена находится в аллильном или пропаргильном положении. При этом во всех случаях восстанавливается и непредельная группировка. Атомы галогена, связанные непосредственно с атомами углерода винильной и этинильной групп, замещаются водородом труднее, но легче, чем расположенные изолированно от кратной связи или в галогеноалканах. Эта закономерность объясняется участием кратной связи в формировании переходного состояния при гидрогенолизе связи С-галоген в галогеновинильных, этинильных, аллильных и пропаргильных производных. В ароматических соединениях атом галогена в бензильном положении замещается намного быстрее, чем находящийся в ароматическом цикле. Дегалогенирование может быть осуществлено без восстановления бензольного кольца.
Прекрасным катализатором гидрогенолиза галогенопроизводных разных типов является никель Ренея.
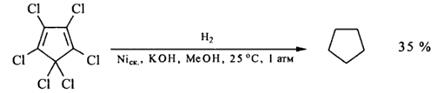
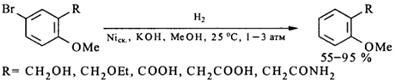
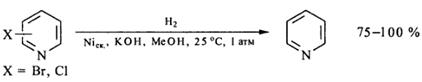
На этом катализаторе галогеносодержащие азосоединения при температуре 250 С и давлении 1-3 атм в присутствии щелочи подвергаются дегалогенированию и происходит расщепление связи N=N, а без добавления щелочи происходит только гидрогенолиз азогруппы.

Многие галогенопроизводные с высокими выходами, а часто количественно дегалогенируются при 250 С и атмосферном давлении на палладиевых катализаторах:
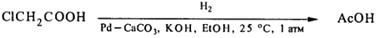


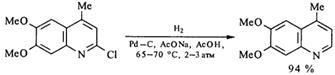

Как на палладиевом, так и на скелетном никелевом катализаторе при дефиците водорода возможно восстановительное сочетание галогенопроизводных, то есть расщепление связи С-галоген с образованием новой углерод-углеродной связи и, следовательно, с усложнением углеродного скелета молекулы:
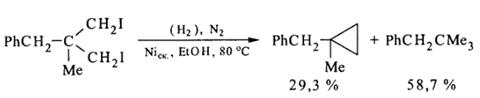
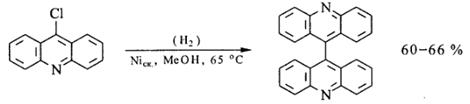
Арилгалогениды на оксиде платины при температуре 50-700 С и давлении водорода 3 атм не только дегалогенируются, но и полностью гидрируются. Выходы циклоалканов при этом составляют 70-95%:
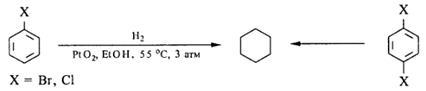
Наиболее лкгко происходит гидрогенолиз связи С-Cl в ацилгалогенидах. Реакция протекает в мягких условиях и является методом синтеза альдегидов (гл.1, стр.5). Дезактиватор (хинолин-S) готовят растворением серы в хинолине при кипячении. Вместо палладиевых катализаторов с успехом может применяться оксид платины, дезактивированный тиомочевинной. В указанных условиях не восстанавливаются даже такие реакционноспособные группы как нитрогруппа, двойные углерод-углеродные связи:
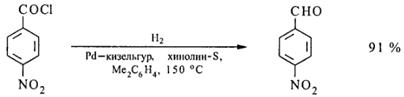
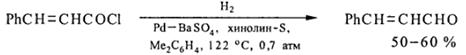
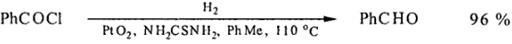
Побочными продуктами при получении альдегидов этим методом являются спирты, углеводороды, сложные и иногда простые эфиры. Выходы альдегидов составляют 50-95%.
Date: 2015-07-27; view: 769; Нарушение авторских прав