
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

I. Гидрирование как метод восстановления
|
|
Гидрирование используется для решения синтетических и, реже, аналитических задач и реализуется в стандартном препаративном и промышленном масштабах. Присоединяя этим методом водород по кратным связям, можно исчерпывающе или частично восстанавливать различные углеродные и гетероатомные ненасыщенные фрагменты молекулы, такие как, ацетиленовая и этиленовая связи, карбонильная и нитрильная группы, ароматическое и гетероароматическое ядра и др., и тем самым заменять одни функциональные группы другими или удалять ненасыщенные реакционные центры.
Во многих случаях в условиях гидрирования протекает гидрогенолиз, т.е. полный разрыв связи между атомами реакционного центра, например, С-О, C-S, C-N, C-Cl, C-Br, C-I, C-C, N-N с присоединением водорода по месту расщепления.
Гидрогенолиз связи C-Cl лежит в основе одного из способов получения альдегидов – реакция Розенмунда:

Применение палладиевого катализатора (Pd-BaSO4 или Pd-C), обычно частично дезактивированного небольшим количеством сернистого соединения, и мягкие условия гидрирования позволяют практически избежать дальнейшего восстановления образующегося альдегида.
Способность связи С-галоген к гидрогенолизу используется при удалении атомов галогена из ароматических циклов. Так, 4,5-дииодо-1-метил- и 2,4,5-трииодо-1-метилимидазолы легко восстанавливаются в 4-иод-1-метилимидазол рассчитанным количеством водорода при атмосферном давлении и температуре 200 С на скелетном никелевом катализаторе в присутствии основания:
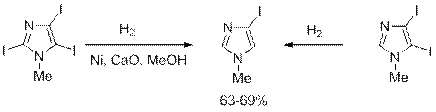
Направленно получить тот же моноиодид прямым иодированием 1-метилимидазола не удается, так как скорости вступления первого, второго и третьего атомов иода в гетероцикл близки между собой.
Легко подвергаются гидрогенолизу связи С-гетероатом (O,N) в бензильном положении. Этим определяется возможность применения бензильной и родственной групп как защитных при синтезе полифункциональных соединений. Снятие такой защиты достигается гидрированием соединения на палладиевом катализаторе при температуре 200 С и атмосферном давлении:
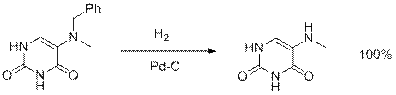
Гидрирование как аналитический метод сыграло заметную роль в истории химии при установлении строения непредельных органических соединений. В настоящее время оно иногда используется для количественного определения степени ненасыщенности веществ, особенно смесей (например, жиров), непредельных карбоновых кислот, ацетиленовых соединений и др. Степень ненасыщенности при этом обычно характеризуется так называемым числом гидрирования – массой водорода в граммах, необходимой для гидрирования 10 кг вещества.
Особенность гидрирования как синтетического метода заключается в применении для восстановления веществ разных классов одного и того же восстановителя и общих катализаторов. Эта особенность ограничивает возможность избирательного гидрирования соединений, если необходимо, например, обеспечить заданную глубину восстановления группы, способной к более глубокому восстановлению, или прогидрировать одну из нескольких восстанавливающихся групп, не затрагивая остальных.
Тем не менее возникающие затруднения во многих случаях успешно преодолеваются подбором катализатора и условий реакции.
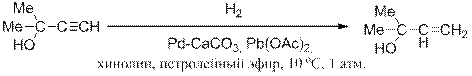
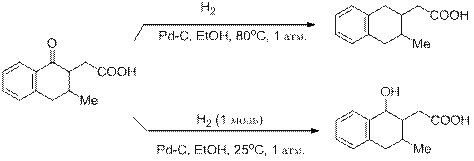
Гидрирование при атмосферном давлении термодинамически разрешено при относительно невысоких температурах. С повышением температуры начинает играть роль процесс дегидрирования насыщенных групп и, таким образом, гидрирование становится обратимым. При высоких температурах преобладает обратная реакция дегидрирования. Так, алкины и алкены могут гидрироваться в алканы, а бензол в циклогексан при умеренных температурах и атмосферном давлении, поскольку в этих условиях насыщенные углеводороды стабильнее соответствующих ненасыщенных. При достаточно высоких температурах относительная стабильность этих соединений изменяется на противоположную и гидрирование становится невозможным.
Положение равновесия процесса гидрирования – дегидрирования зависит от давления водорода, причем с повышением давления гидрирование проходит эффективнее при высоких температурах.
Существуют две разновидности каталитического восстановления водородом – гетерогенное и гомогенное гидрирование. При гетерогенном гидрировании субстрат находится в жидкой или газовой фазе, а реакция протекает на поверхности твердого катализатора. Катализаторами являются переходные металлы в мелкодисперсном или пористом состоянии, а также оксиды или сульфиды металлов.
При гомогенном гидрировании активация молекулярного водорода и реакция происходят в растворе субстрата и катализатора – соединения переходного металла. Важнейший из таких катализаторов – трис(трифенилфосфин)родий хлорид RhCl(PPh)3 (катализатор Уилкинсона).
Гетерогенное гидрирование традиционно и, являясь хорошей основой экологически чистой технологии, широко применяется не только в лабораторной практике, но и в промышленности (гидрогенизация жиров, получение многоатомных спиртов из полисахаридов, анилина из нитробензола, циклогексанона из фенола, производство бензола и нафталина гидродеалкилированием, гидроочистка и гидрообессеривание нефтяных фракций).
Date: 2015-07-27; view: 1017; Нарушение авторских прав