
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Стадия воспаления
|
|
Сосудистые расстройства. Экссудация и эмиграция. Результат образования в воспаленном очаге большого количества вазоактивных веществ — медиаторов воспаления, которые расслабляют мышечные элементы стенки артериол и прекапилляров. Основные патогенетические изменения микроциркуляции отражены на рис 24. Нарушение микроциркуляции является необходимой предпосылкой для развития последующих этапов воспаления. Только при замедлении кровотока и его полной остановки становится возможным накопление медиаторов воспаления на достаточно коротком отрезке сосудистого русла. Благодаря накоплению хемокинов и очаге воспаления начинается эмиграция лейкоцитов, то есть выход форменных элементов белой крови за пределы сосудистого русла в зону альтерации Хемокины - это большая группа цитокинов, стимулирующая двигательную активность лейкоцитов. Они привлекают в очаг воспаления различные типы лейкоцитов, обеспечивая их адгезию с эндотелиальными клетками и транспорт через сосудистую стенку. По И.Мечникову, "движущей силой, началом" (premium movens) воспаления является скопление лейкоцитов вокруг повреждающего агента. Согласно классической концепции, пока лейкоциты находятся внутри сосуда, воспаления нет. Как только начинается выход из сосудов лейкоцитов, их скопление в месте повреждения появляются основания говорить собственно о воспалении. Таким образом, внесосудистая миграция лейкоцитов и их скопление в месте повреждения - одно из главных явлений при воспалительном ответе. Без выхода лейкоцитов и их скопления в одном месте в форме инфильтрата нет воспаления. Скопление клеток в очаге воспаления носит название воспалительного инфильтрата. Клеточный состав инфильтрата в значительной степени зависит от этиологического фактора. Важное место в патогенезе воспаление имеет адгезия (прилипание) лейкоцитов к эндотелиальным клеткам с последующей миграцией в очаг. Усиление синтеза адгезивных белков самими эндотелиальными клетками происходит под влиянием определенных медиаторов воспаления, в частности хемокинов. Адгезины - молекулы, управляющие адгезивными реакциями. Они вырабатываются не только эндотелиальными клетками, но и лейкоцитами. Известно несколько классов молекул клеточной адгезии. Наиболее изученными из них являются селектины и интегрины. С участием селектинов происходит выход лейкоцитов из осевого кровотока в пристеночный и неокончательная, обратимая их адгезия к эндотелию сосудов. Интегрины осуществляют окончательное прикрепление лейкоцитов к эндотелию, способствуют выходу лейкоцитов через стенку сосудов. Кроме того, интегрины обеспечивают взаимодействие клеток с белками внеклеточного матрикса после их эмиграции из сосудов. Способствуют адгезии лейкоцитов и изменения происходящие в самих лейкоцитах при их активации. Во-первых, нейтрофилы в фазе инициации воспаления активизируются и образуют агрегаты. Агрегации лейкоцитов способствуют лейкотриены, ФАТ, С5а-фрагмент системы комплемента. И. во-вторых, это продукты, секретируемые лейкоцитами (лактоферрин).. После прикрепления к эндотелию лейкоциты начинают эмиграцию (рис 5-7.) в очаг воспаления. Направление движения лейкоцитов определяется накоплением хемоакттарантов (от лаг. attractio - притяжение). Это продукты жизнедеятельности бактерий, бактериальный эдотоксин, белки, полипептиды, продукты разрушенных клеток, частичной деградации коллагена. Свойствами хемоаттарактантов обладают С5а и СЗа фракции комплемента, кинины, простагландины, лейкотриены. ФНО, активный фактор Хагемана, активатор плазминогена, фибринопептид В, лимфокины, монокины, иммуноглобулины.
Сначала в очаг воспаления проникают нейтрофилы/ПЯЛ, приступая к фагоцитозу (рис.5.) и активизируют каскад биохимических и морфологических изменений в очаге с формированием грануляционного вала, привлекают в очаг и другие клетки воспаления.
При не осложненном развитии воспалительного процесса уже через 18-24 ч число моноцитов в инфильтрате превышает количество нейтрофилов. Но не всегда нейтрофилы своевременно замешаются мононуклеарами. В этих случаях воспаление приобретает затяжной характер при снижении бактерицидности нейтрофилов, при избыточном выделении медиаторов воспаления, которые приводят к стойким нарушения микроциркуляции. Деструкции соединительной ткани и выраженное накопление хемотаксических веществ, привлекает новые порции нейтрофилов. Хронизация воспаления сопровождается изменениями медиаторного фона. Если общепринятыми медиаторами острого воспалительного процесса являются ИЛ-1,ФНО-а, то медиаторами подострого и хроническою воспаления служат ИЛ-4, ИЛ-6. С самого начала воспалительной реакции в поврежденных тканях нарушается обмен веществ. Вначале интенсивность обмена веществ повышается ("пожар обмена"). Усиливаются катаболические процессы. Первоначально в очаге воспаления возрастает потребление кислорода, очень интенсивно используется приносимая с током крови глюкоза. Однако в связи с развитием венозного застоя напряжение кислорода падает со 100-110 мм рт.ст. до 10-15 мм рт.ст. Нарушение доставки кислорода и повреждение митохондрий приводят к быстрому угнетению аэробного окисления углеводов и активации анаэробного гликолиза. Как следствие этого, в очаге воспаления возникает дефицит макроэргов, происходит накопление больших количеств недоокисленных продуктов обмена (молочной, α-кетоглютаровой, яблочной, янтарной кислот и др .) В очаге воспаления происходит значительное усиление протеолитических процессов, отмечается усиленный распад белков, накопление полипептидов, свободных аминокислот.
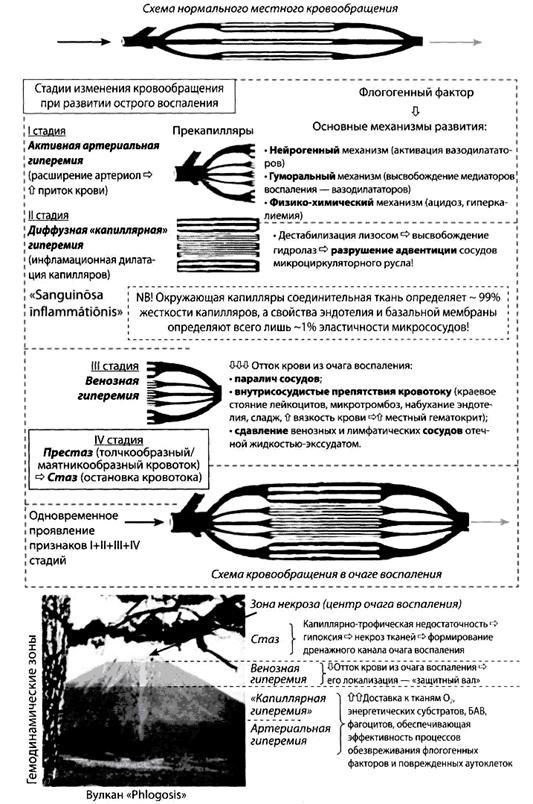
Рис.25. Изменение местного кровообращения при воспалении (В. Войнов 2007)
Усиливаются процессы липолиза, что приводит к повышению содержания свободных жирных кислот, нарастает количество кетоновых тел.
Однако по мере нарастания повреждения интенсивность метаболизма снижается, Таким образом, при воспалении обмен веществ меняется как качественно, так и количественно.
Вследствие нарушения тканевого окисления и накопления в тканях недоокисленных продуктов развивается метаболический ацидоз. Концентрация водородных ионов повышается тем больше, чем сильнее выражено воспаление. Наиболее низкий рН наблюдается при гнойном воспалении (рН может снизиться до 5.0). Последствиями развивающегося ацидоза в очаге воспаления являются активация протеолитнческих ферментов, дилятация сосудов и повышение проницаемости их стенок. В тканях воспалительного очага происходит резкое изменение онкотического и осмотического давления. Повышение онкотического давления является результатом усиления катаболических процессов: крупные белки расщепляются на более мелкие, их концентрация нарастает. К тому же мелкодисперсные белки поступают в зону воспаления из сосудистого русла. В результате повышается гидрофильноеть тканей. Разрушение клеток приводит к высвобождению внутриклеточных ионов, электролитов, что обусловливает гипер ионию и гиперосмию, способствуя гидратации тканей.
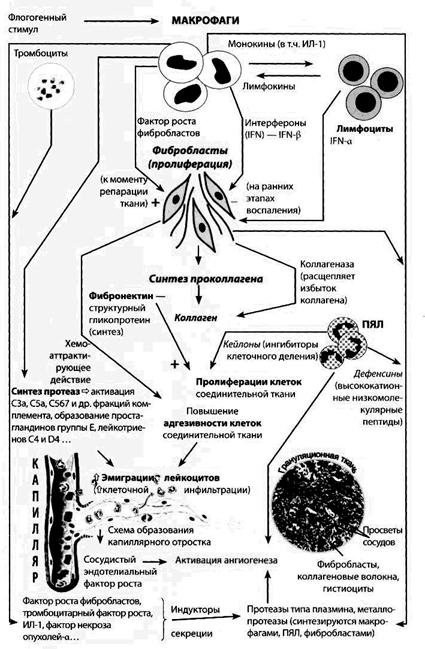
Рис. 26. Механизмы пролиферации в очаге воспаления (В. Войнов 2007)
Date: 2015-07-22; view: 963; Нарушение авторских прав