Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Визначення резервної лужності і кислотної ємності крові
|
|
Більшість біологічних процесів в організмі (за винятком процесів травлення в шлунку) урівноважені кислими (Н+) і лужними (ОН–) іонами, тобто проходять у нейтральному або слаболужному середовищі. Тому величина рН плазми крові коливається у незначних межах: від 7,35 до 7,45.
Показник рН може змінюватися за рахунок кислот і лугів, які надходять в організм з кормом. Кислоти утворюються з білків і жирів внаслідок проміжного обміну речовин у клітинах і тканинах, при бродильних процесах в органах травлення, фізичному навантаженні. Луги надходять в організм переважно з рослинними кормами. Утворення кислот і лугів проходить також при розвитку різних патологічних процесів.
Незважаючи на вплив кислот і лугів, величина рН крові стабільна. Постійність рН забезпечується, передусім, буферними системами крові, а також активною діяльністю нирок, які виводять з організму непотрібні лужні і кислі продукти обміну речовин, легень, що виділяють залишки вуглекислоти, травної системи, шкіри і молочної залози.
Внаслідок стабільності рН, оцінку стану кислотно-лужної рівноваги проводять за результатами дослідження буферних систем, які є в крові: гідрокарбонатної, фосфатної, білкової і гемоглобін-оксигемоглобінової. Останні дві найбільш ємні.
Запас усіх буферних систем крові називається кислотною ємністю, а запас бікарбонатів крові, визначений за загальною кількістю вуглекислоти, яка міститься в плазмі, – лужним резервом.
Стан кислотно-лужної рівноваги найбільш повно можна визначити за допомогою мікрометоду апаратами типу “Аструп” за наступними показниками: рН, парціальний тиск вуглекислоти, бікарбонат крові, буферні основи та їх зрушення.
У практиці лабораторій ветеринарної медицини визначають резервну лужність плазми крові дифузійним методом за допомогою здвоєних колб (за І.П.Кондрахіним), кислотної ємності крові – методами Беляєва – Большакова – Коромислова.
Титрометричний метод визначення кислотної
ємності сироватки або плазми крові
(за А.О. Кудрявцевою і В.Ф. Коромисловим)
Принцип методу. Лужні речовини сироватки крові зв’язуються з соляною кислотою, а вільна соляна кислота титрується лугом з індикатором Таширо. В точці еквівалентності колір переходить із брудно-буро-фіолетового в яскраво-зелений, який зберігається протягом кількох хвилин. Інколи випадає осад білка, але він не заважає титруванню.
Обладнання: хімічні або бактеріологічні пробірки, хімічні склянки на 50 чи 100 мл або колби на 50 мл, бюретка на 50 мл, мікробюретка, піпетки на 1 або 10 мл, крапельниця, мірна колба на 1 л, лійка та про-
бірки.
Реактиви: 0,01 N-ний розчин соляної кислоти; 0,01 N-ний розчин натрію гідроокису; реактив Таширо (обережно змішують 50 мл 0,03 %-ного спиртового розчину метилового червоного і 7,5 мл 0,19 %-ного водного розчину метиленового синього). Всі реактиви готують на прокип’яченій дистильованій воді.
Методика визначення. У склянку або колбу наливають 10 мл 0,01 N-го розчину соляної кислоти, 0,2 мл сироватки крові і 1–3 краплі реактиву Таширо, обережно перемішують і титрують 0,01 N-ним розчином натрію гідроокису до появи зеленого забарвлення. Одночасно визначають коефіцієнт поправки – відтитровують при таких самих умовах
10 мл 0,01 N-го розчину HCl 0,01 N-ним розчином NaOH.
Кислотну ємність (X) вираховують за формулою:
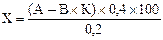 ;
;
Х = (А – В ´ К) ´ 200,
|
Коефіцієнт поправки (К) вираховують за наступною формулою:
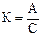 ,
,
де: А – кількість 0,01 N-ного розчину соляної кислоти, мл; С – кількість 0,01 N-ного розчину натрію гідроокису, витрачена на титрування, мл.
При правильному зберіганні в закритих пробірках у вільному від парів лугів і кислот місці (краще в холодильнику) кислотна ємність сироватки крові залишається незмінною протягом 2–3-х днів. Для більш тривалого зберігання сироватку крові консервують: у пробірку наливають 1 мл 0,1 N-го розчину соляної кислоти і вносять 0,2 мл сироватки, закривають пробкою і ставлять у холодильник. В день дослідження добавляють 9 мл дистильованої води, вільної від аміаку і вуглекислого газу, і титрують. Встановлено, що при нормальних показниках крові (кількість каротину, кальцію, фосфору, загального білка, глюкози) у зимово-стійловий період кислотна ємність сироватки крові великої рогатої худоби становить 270–460, а в літній – 300–480 мг/100мл. Для перерахунку в одиниці, які допускаються ВООЗ нарівні з одиницями SI, одержаний результат ділять на 4 і виражають у ммоль/л.
Визначення резервної лужності крові
дифузійним методом за допомогою здвоєних колб
(за І.П.Кондрахіним )
Принцип методу. В одній частині колби плазма крові підлягає дії сірчаної кислоти, внаслідок чого вивільнюється вуглекислий газ, який знаходиться у складі бікарбонатів. Виділений вуглекислий газ поглинається розчином натрію гідроксиду, який знаходиться у другій частині колби. Надлишок NaOH, який не вступив у реакцію з вуглекислим газом, та половину натрію вуглекислого (Na2CO3), утвореного внаслідок поглинання СО2, титрують розчином сірчаної кислоти. За кількістю зв’язаного початкового натрію гідроксиду визначають кількість виділеного з плазми вуглекислого газу, яка дорівнює вмісту бікарбонатів.
Реактиви. 1) 0,1 N-ний (0,05 моль/л) розчин сірчаної кислоти (готують з фіксаналу); 2) 0,02 N-ний (0,01 моль/л; точно!) розчин сірчаної кислоти (готують з 0,1 N-ного розчину сірчаної кислоти; 3) 0,1 N-ний розчин натрію гідроксиду; 4) 0,02 N-ний (0,02 моль/л) розчин натрію гідроксиду [готують з 0,1 N-ного (0,1 моль/л) розчину натрію гідроксиду; титр цього розчину перевіряють перед дослідженням і доводять до потрібної величини]; 5) 5 %-ний розчин сірчаної кислоти; 6) 1 %-ний спиртовий розчин фенолфталеїну.
Обладнання: здвоєні колби з гумовими пробками (не менше 30 шт.); мікробюретки на 2 і 5 мл; центрифужні пробірки із товстого скла.
Методика визначення. У чисті, сухі центрифужні пробірки вносять 0,5–1 мл вазелінового масла, 1–2 краплі 1 %-ного розчину гепарину. Кров беруть з яремної вени в підготовлену пробірку, закривають пробкою, обережно перемішують. В лабораторії її центрифугують при 3000 об/хв протягом 20 хв. Плазму крові зберігають в холодильнику при температурі 4 °С.
За кількістю проб крові з врахуванням паралельних досліджень підбирають здвоєні колби і не менше трьох здвоєних колб залишають для контролю. Точність результатів усієї серії досліджень залежить від точності титрування розчину натрію гідроксиду в контрольних колбах. Усі колби закривають гумовими пробками.
Дослідження проводять серійно. В одну з кожної пари здвоєних колб, почергово відкриваючи, вносять за допомогою бюретки або піпетки (не видуваючи) по 2 мл 0,02 N-ного розчину натрію гідроксиду і щільно закривають пробкою. У паралельну колбу, крім контрольних (знову почергово відкриваючи і закриваючи), вносять із піпетки (не видуваючи) 0,5 мл плазми крові, яка знаходиться під вазеліновим маслом. Після цього в колби з плазмою (контрольні без плазми), також почергово, вносять із піпетки (не видуваючи) по 1 мл 5 %-ного розчину сірчаної кислоти і швидко щільно закривають пробкою. Перевіряють, чи добре закриті колби, обережно руховими рухами перемішують плазму крові з кислотою і залишають на 4 год (можна і більше, звичайно на ніч). Перемішування плазми крові з кислотою проводять не менше 3-х разів. Через 4 год (або вранці наступного дня) починають титрування. Для цього почергово відкривають колбу, де знаходиться розчин натрію гідроксиду, вносять туди 1–2 краплі розчину фенолфталеїну і титрують з мікробюретки на 2 мл 0,02 N-ним розчином сірчаної кислоти до повного знебарвлення розчину. Титрування дослідних та контрольних проб виконують з однаковою швидкістю.
За різницею результатів титрування в контрольних та дослідних зразках знаходять кількість мл 0,02 N-ного розчину натрію гідроксиду, зв’язаного з вуглекислим газом, витісненим із бікарбонатів крові. Розрахунок проводять за формулою:
Х об%СО2 = (Vк – Vп) ´ 89,6,
де: Vк – кількість 0,02 N-ного розчину сірчаної кислоти в мл, яка пішла на титрування вмісту контрольної проби; Vп – кількість 0,02 N-ного розчину сірчаної кислоти в мл, яка пішла на титрування дослідної проби; 89,6 – коефіцієнт перерахунку 0,02 N-ного розчину натрію гідроксиду на СО2.
Клінічне значення. Зниження резервної лужності крові свідчить про зрушення кислотно-основної рівноваги у бік ацидозу, а підвищення – алкалозу. Метаболічний ацидоз зустрічається при одноманітному висококонцентратному або силосно-жомовому типі годівлі, кетозі, вторинній остеодистрофії, ацидозі рубця, цукровому діабеті, розладах травлення, особливо при діареї у молодняку, нефриті, нефрозі, септичних процесах. Респіраторний ацидоз виникає внаслідок уповільнення процесу виділення вугільної кислоти легенями при розладах серцевої діяльності, емфіземі легень, при знаходженні тварин у середовищі з високою концентрацією у повітрі вуглекислоти. Метаболічний алкалоз у тварин буває при алкалозі рубця, введенні в організм великих доз кухонної солі, а респіраторний – при гіпервентиляції легень, виведенні з організму великої кількості вуглекислого газу.
Date: 2015-07-01; view: 619; Нарушение авторских прав