
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Гипербиозы
|
|
Гипербиозы – это такое явление, когда процессы ассимиляции преобладают над процессами диссимиляции. Гипербиотические процессы – процессы избыточного роста и размножения клеток, тканей, органов. Гипербиотические процессы могут рассматриваться как компенсаторно-приспособительные (гипертрофия, гиперплазия, регенерация) и как сугубо патологические, характеризующиеся неограниченным, беспредельным ростом (опухоли). Наконец возможна особая форма патологического роста тканей, при которой имеет место сочетание гипо- и гипербиотических процессов. Эта форма роста возникает при пересадках органов и тканей (трансплантация).
3.1. Гипертрофия (от греч. hyper – избыток, trope – питание) – увеличение органа или ткани в объеме с усилением функции.
Увеличение объема ткани, органа происходит или за счет увеличения размера клеток (истинная гипертрофия), или за счет увеличения их количества (гиперплазия). Чаще всего гипертрофия развивается за счет увеличения клеток и увеличения количества гипертрофированных клеток.
Различают гипертрофию истинную и ложную.
Истинная гипертрофия – увеличение объема ткани или органа вследствие равномерного разрастания паренхиматозных клеток и всех других составных частей (элементов). При этом функциональные возможности органа повышаются. Примером являются гипертрофия гладких мышц матки в период беременности, увеличение молочной железы в период лактации. Для развития гипертрофии необходимы два условия:
1 – усиление функциональной активности органа или ткани;
2 – увеличение кровоснабжения гипертрофирующего органа и обеспечение поступления к нему питательных веществ. Отсутствие достаточного питания в условиях усиленной функции органа ведет к развитию атрофических процессов. Так как питание и обмен веществ у высших животных и человека регулируются нервной и эндокринной системами, то им и следует придавать большое значение в патогенезе гипертрофии.
Ложная гипертрофия – увеличение объема органа при разрастании соединительной или жировой ткани. Количество паренхиматозных клеток остается без изменений или даже уменьшается, а функциональная способность органа может снижаться. Например, увеличение объема щитовидной железы при эндемическом зобе в результате разрастания ее соединительной ткани или гипертрофия молочной железы за счет жировой ткани. Подобную картину можно наблюдать в начальной стадии цирроза печени, когда ее увеличение обусловлено разрастанием соединительной ткани. Или при увеличении объема мышцы вследствие нарастания жировой ткани между мышечными волокнами.
По этиологии и патогенезу различают следующие виды гипертрофии:
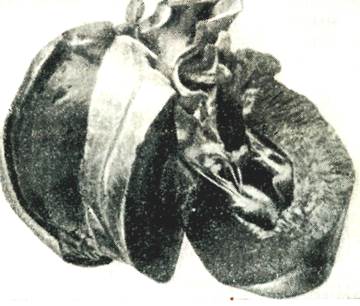
• Рабочая или функциональная – это увеличение органа или ткани за счет объема и размножения клеток, вызванное усиленной работой органа. Интенсивно работающий орган гипертрофируется. Во время лактации гипертрофируется молочная железа; развитие эмбриона в матке сопровождается гипертрофией ее стенки. В этих ситуациях увеличение массы органов происходит не только за счет величины клеток, но и за счет их усиленного размножения (гиперплазии). К патологическим рабочим гипертрофиям относится гипертрофия сердечной мышцы при пороках сердца. Так, при сужении устья аорты или при недостаточности ее клапанного аппарата, создается препятствие для работы левого желудочка и происходит его гипертрофия. При чрезмерной гипертрофии правого и левого желудочков сердце может достигать огромных размеров (бычье сердце).
|
Гипертрофия сердца может возникнуть при стойком повышении кровяного давления и при других заболеваниях, сопровождающихся повышенным препятствием движения крови в большом и малом круге кровообращения.
К числу рабочих гипертрофий, возникающих вследствие усиленной работы, следует отнести и викарные гипертрофии, при которых нарушение или выпадение функции одного из парных органов служит причиной возникновения гипертрофии другого.
• Викарная гипертрофия, характеризуется увеличением массы парного органа при удалении или атрофии одного из них.
Потеря одной почки ведет к увеличению объема и функции другой.

|
|
Однако викарная гипертрофия никогда не компенсирует на 100% деятельность выбывшего парного органа. Функция гипертрофированного легкого, надпочечника, почки, других парных органов только на 60–80% замещает изначальную нагрузку. Степень замещения (восстановление) функции зависит от многих факторов, в том числе от возраста больного животного. Так, удаление почки у молодой крысы ведет к 65% гипертрофии оставшейся, а у старой к 25%-ной.
• Механическая гипертрофия. Она не имеет компенсаторного значения и возникает без видимой функциональной необходимости. Механические и химические факторы могут служить толчком к развитию такой гипертрофии. Она возникает при длительном раздражении. Например, разрастание и ороговение эпителия кожи, образование мозолей при длительном трении, разрастание эпителия при длительном действии анилиновых красок. Сюда можно отнести гипертрофию слизистой кишечника при хроническом раздражении его грубой пищей, при частых запорах.
• Эндокринная или корреляционная гипертрофия. Эндокринная гипертрофия возникает в органах, функционально связанных между собой. Например, увеличение выработки адренокортикотропного гормона гипофизом ведет к гипертрофии и гиперплазии коры надпочечников, после удаления щитовидной железы происходит увеличение гипофиза.
• Регенерационная гипертрофия – увеличение оставшейся части органа после удаления некоторой его части. Отмечают этот вид гипертрофии в печени, поджелудочной железе, селезенке. Удаление у подопытного кролика более 50% ткани печени спустя 1–2 месяца приводит к полному восстановлению массы органа. Иногда наблюдается избыточная регенерация тканей. При этом вновь образующейся ткани возникает больше, чем требуется для заполнения дефекта, например, образование костной мозоли при заживлении переломов костей, избыточное образование грануляционной ткани при туберкулезе.
Выделяют также группу врожденных гипертрофий, связанных с различными нарушениями эмбрионального развития. К этим гипертрофиям могут быть отнесены общий и частичный гигантизм, врожденная гипертрофия рогового слоя эпидермиса кожи (врожденный ихтиоз).
Рабочая, викарная и регенерационная гипертрофии имеют компенсаторное значение. Под влиянием различных факторов процессы гипертрофии могут включаться относительно быстро. Выраженный тканевой рост уже наблюдают через несколько суток. Отмечается увеличение числа митозов. В зависимости от особенностей органа и существующих условий срок появления максимальной гипертрофии у животных наступает на 20–180 день.
Эксперименты показывают, что существенно на развитие гипертрофии влияют характер кормления животного и функция нервной и эндокринной систем. Например, значительная компенсаторная гипертрофия почки отмечается в результате повышенного потребления белка. При недостатке соматотропного гормона передней доли гипофиза или при тиреоидэктомии компенсаторная гипертрофия почки задерживается.
3.2. Гиперплазия (от греч. hyper – избыток, plasis – образование) – увеличение органа или ткани в объеме за счет размножения клеточных элементов.

|
Определяющими факторами в развитии гиперплазии являются повышенная функциональная активность органа, воспалительные и регенеративные процессы, гормональное влияние.
3.3. Регенерация (от лат. regeneration – возрождение).
Регенерация - восстановление клеток, тканей, органов, отдельных частей живых существ подвергшихся разрушению. Регенерация сопровождает жизнь живого организма с момента оплодотворения до завершения жизнедеятельности. У нормального здорового организма непрерывно разрушаются и воспроизводятся молекулы, ферментные системы, органоиды клетки, сами клетки. Постоянное разрушение и обновление тканей сопровождается важными для организма процессами образования таких секретов как молоко, желудочный и кишечный сок, соляная кислота, желчные пигменты и др.
Различают регенерацию физиологическую и патологическую.
• Физиологическая регенерация – это постоянное восстановление клеток, тканевых элементов, погибающих в нормальных условиях. Этот процесс происходит в течение всей жизни организма. Интенсивные процессы регенерации обнаруживаются при восстановлении клеток крови, слизистых оболочек. К физиологической регенерации относят также линьку млекопитающих и птиц. Рост резцов у грызунов и др.
• Патологическая (репаративная) регенерация – процесс восстановления поврежденных тканей, органов после действия чрезвычайных раздражителей. К патологической регенерации относят восстановление клеток, тканей при воспалении. В ответ на повреждение лучшую способность к регенерации проявляют низшие животные, и чем выше организация, тем регенерация слабее. Например, у простейших можно легко получить регенерацию целого животного из каждой половинки после перерезки его на две части. Весьма выраженной регенераторной способностью обладают гидры (кишечнополостные). Кусочек гидры в 1/200 от целого способен восстановиться в целое животное. Моллюски также сравнительно легко восстанавливают утраченные части тела. Насекомые (пауки) довольно легко регенерируют утраченные конечности, антенны, иногда глаза. У позвоночных животных процессы регенерации выражены значительно слабее по сравнению с беспозвоночными. Возрождение целых частей тела (хвост, конечности, глаза) возможно только у низших позвоночных (рыбы, амфибии, рептилии).
Тем не менее, у млекопитающих и птиц регенерируют после повреждения все тканевые структуры, но в разной степени. Значительной регенеративной способностью обладает эпителиальная ткань.
Регенерация эпителиальной ткани. Наивысшей способностью к регенерации, обусловленной травмой, обладает кожа. В ходе эволюции покровные ткани подвергались наивысшей травматизации со стороны внешней среды, поэтому быстрое заживление ран кожи – выражение приспособленности, морфологической адаптации животных к повреждающим факторам. Эпителий кожи восстанавливается за счет пролиферации клеток глубокого зародышевого слоя. Слизистая оболочка желудочно-кишечного тракта, дыхательных путей обладает выраженной способностью к репаративному восстановлению. При остро текущих катарах эпителий может слущиваться с больших площадей и сравнительно легко замещаться новым. Восстановление исходит из клеточных элементов крипт. Хорошо выраженной репаративной регенерацией обладают производные эпителиальной ткани – слюнные железы, печень, поджелудочная железа.
|
|
Регенерация соединительной ткани. Соединительная ткань способна к хорошо выраженной репаративной регенерации. Рыхлая клетчатка соединяет края ран, отгораживает очаг поражения от здоровых тканей, восполняет раневой дефект соединительным рубцом, закрывающим ворота инфекции. В заживлении переломов костей основное значение имеют остеобласты, пролиферация которых восстанавливает поврежденные структуры. Остеокласты обеспечивают резорбцию поврежденной костной ткани, подавление избыточно разросшейся. Сравнительно быстро регенерируют фасции и сухожилия. Слабой регенераторной способностью обладает хрящевая и жировая ткань.
Регенерация мышечной ткани. Мышечная ткань регенерирует значительно слабее эпителиальной и соединительной. Мышечные волокна скелетных мышц способны регенерировать после повреждения путем омитотического деления клеток, граничащих с поврежденным участком. Может быть восстановлена поперечнополосатая изчерченность. В восстановлении функции поврежденной скелетной мышцы основное значение все же имеет гипертрофия. Патологическая регенерация гладких мышц возможна за счет митотического деления мышечных клеток, но осуществляется относительно слабо.
Регенерация нервной ткани. Нервная ткань регенерирует неоднозначно. Повреждение клеток центральной нервной системы, нейронов спинного мозга, симпатических ганглиев завершается их гибелью. Регенерация аксонов коры головного мозга, подкорковых центров происходит весьма слабо или отсутствует. Аксоны нервных клеток обладают сильной способностью к регенерации.
Повреждение периферического нерва сопровождается атрофией конца нерва идущего к периферии. Регенерация начинается на конце аксона соединенного с нервной клеткой. Регенерирующий конец нерва врастает в трубочки, образованные клетками Шванна и способен восстановить иннервацию. Роль Швановских клеток, по-видимому, очень существенна, так как в головном и спинном мозге, где их опорная и трофическая функция заменена клетками глии, регенерация нервных волокон не происходит. Скорость регенерации аксонов весьма мала: 1-3 мм в сутки. Если центральные и периферические концы поврежденного нерва отодвинуты далеко друг от друга, регенерация аксонов не достигает Швановских клеток и полная регенерация не наступает. Если же аксон не совмещен с объектом врастания (не достигает Швановских клеток), то на его конце могут образовываться своеобразные утолщения – невромы, раздражение которых может причинить больному острую, труднопереносимую боль.
Конечный этап регенерации – заживление ран. Оно начинается с заполнения дефекта фибрином, скопления лимфоцитов, освобождения биологически активных веществ – стимуляторов роста. Они вызывают размножение, прежде всего эндотелиальных клеток, клеток адвентиции сосудов, малодифференцированных соединительнотканных элементов – фибробластов, являющихся источником коллагена, эластина. Заживление может осуществляться по пути первичного натяжения, например операционных ран или по пути вторичного натяжения, когда рана инфицирована или слишком обширна.
Домашние животные разных видов вне зависимости от силы, количества и природы раздражителя имеют свои особенности в регенерации поврежденных тканей. У парнокопытных животных (крупный рогатый скот, овцы, свиньи) и птиц происходит быстрая инкапсуляция, и заживление протекает преимущественно по первичному натяжению. У лошадей, других однокопытных заживление идет преимущественно вторичным натяжением.
Регенерация характеризуется образованием капилляров из клеток эндотелия, адвентиции, гистоцитов, фибробластов. Грануляционная ткань является структурным и функциональным барьером, ограждающим организм от инфекционного начала и токсикоза. Грануляционная ткань богата кровеносными сосудами и нервными окончаниями. При заживлении по вторичному натяжению эпителизация дефекта не происходит, на его месте образуется плотный соединительнотканный рубец.
Механизм регенерации. Регенерировать могут как взрослые дифференцированные клетки, так и менее дифференцированные (например, гистоциты рыхлой соединительной ткани). Регенерация у млекопитающих, однако, наблюдается в пределах только одного вида тканей, например, из рыхлой соединительной ткани может образоваться хрящевая и костная ткань, из эпителия выводных протоков слюнных желез – соответствующие секреторные клетки.
Процесс регенерации обуславливается рядом факторов:
1. Первым и важнейшим стимулом для регенерации является повреждение. Именно продукты поврежденной ткани (протеазы, полипептиды и низкомолекулярные белки) выполняют роль стимуляторов размножения клеток. Ранее они назывались «раневые гормоны».
2. Важным фактором заживления и регенерации являются лейкоциты и продукты их распада. Эти продукты имеют собирательное название – «Трефоны» (от греч. trophos – питаю).
3. На основании опытов установлено стимулирующее влияние одной растущей клетки данной ткани на другую. Предполагается, что это влияние определяется особыми веществами «десмонами» (от греч. desmos – ткань). Десмоны специфичны и не влияют на рост тканей другого вида (например, десмоны соединительной ткани не влияют на мышечную).
4. Большое влияние на регенерацию оказывает состояние питания организма и его регулирующих систем. При голодании регенерация хотя и происходит, но значительно ослаблена. Особое значение имеют полноценное белковое питание и витамины, в частности витамины А, Е, С.
5. С увеличением возраста регенерирующая способность всех тканей понижается. При этом особое значение имеет состояние реактивности организма.
6. Важная роль в регуляции регенерации принадлежит железам внутренней секреции. Так, тиреоидэктомия снижает регенерирующую способность тканей, а введение гормонов щитовидной железы стимулирует заживление ран. Удаление поджелудочной железы приводит к замедлению заживления ран, а кастрация замедляет заживление переломов. Минералокортикоиды (альдостерон) стимулирует, а гликокортикоиды (кортизол) угнетают регенерацию. Роль зобной железы в регенерации пока выяснена недостаточно.
6. Большое значение в качестве стимулятора регенерации имеет нервная система. Экспериментальное повреждение коры головного мозга у собак, кроликов, крыс задерживает процессы заживления ран. Особенно сильное влияние на регенерацию оказывает гипоталамус. Разрушение вентромедиальных ядер гипоталамуса вызывает угнетение заживления ран, задерживает приживление трансплантантов. Экспериментальная перерезка или травмы периферических нервов вызывают резкие нервно-дистрофические явления. Одним из ярких выражений этого влияния является образование незаживающих язв. Они образуются часто на месте случайной царапины, а иногда и без видимого повреждения. Нарушение обмена веществ в тканях, в частности в коже, приводит к ослаблению процессов регенерации эпидермиса. На поверхности кожи образуется дефект – язва. Она обычно окружена вялыми грануляциями, заживает очень долго, иногда несколько лет. После временного заживления она легко возобновляется. Замедление процессов регенерации в данном случае вызывается нарушением трофического влияния нервной системы и сосудодвигательными расстройствами в денервированной ткани.
Трансплантация
Трансплантация (от лат. trans – через, plantation – посадка). Пересадка органа или ткани в пределах организма или от одного организма к другому. В изучении проблемы трансплантации выдающиеся достижения принадлежат русским исследователям. М.А. Новинский впервые в мире осуществил гомо- и гетеротрансплантацию опухолей. Методы гомотрансплантации разработал В.П. Филатов, В.И. Демихов и А.Г. Лапчинский провели пересадку сердца собакам. Собаки, оперированные В.И. Демиховым, жили в отдельных случаях несколько лет. Трансплантация является патологическим процессом, так как пересаженная ткань в любом случае ставиться в неестественные по отношению к ее обычному месту существования условия. Организм, от которого взят материал для трансплантации, называется донором; организм которому трансплантируют ткань – реципиентом. Различают следующие виды трансплантации: аутотрансплантация, гомотрансплантация, гетеротрансплантация, аллопластика.
Аутотрансплантация – пересадка тканей с одного места на другое в пределах одного организма: например, пересадка кожи с одного участка на другой с целью лечения ожогов.
Гомотрансплантация – пересадка органов и тканей от одного животного другому в пределах вида. Пересаживают ограниченное количество тканей. В первую очередь это кожа и хрящ, характеризующиеся стойким приживлением. В настоящее время достаточно широкое распространение получили операции по пересадке почек, суставов, печени, костного мозга. Примером гомотрансплантации является переливание одногруппной крови. Однако гомотрансплантация встречает значительные трудности ввиду частой иммунологической несовместимости тканей донора и реципиента. Преодолеть иммунологическую несовместимость достаточно эффективно еще не удалось. Для этой цели применяются различные иммунодеприсанты (циклоспорин А, антилимфоцитарные сыворотки), угнетающие выработку антител против пересаженной ткани и подавляющее действие специфических Т–киллеров. Антилимфоцитарные сыворотки резко снижают количество лимфоцитов, которые являются источником иммунокомпетентных клеток, вырабатывающих антитела.
Гетеротрансплантация – пересадка органа или ткани от животного одного вида животному другого вида. Во всех случаях пересаженный орган или ткань не приживляется, а отторгается и рассасывается. Но делают это с целью неспецифической стимулирующей терапии. Так, при пересадке половых желез возникает временный стимулирующий эффект от действия гормонов, всасывающихся из разрушенной ткани.
Аллопластика – вживление в организм различных тканей, органов из синтетических материалов. В настоящее время широкое распространение имеет трансплантация искусственных клапанов сердца, сосудов, суставов.
Влияние организма реципиента на пересаженную ткань.
Каждая пересаженная ткань или целый орган попадают в организм реципиента в условиях почти полной денервации, резкого нарушения кровообращения и питания пересаженного органа, резкой клеточной и гуморальной иммунной реакции со стороны организма реципиента. Эти условия неизбежно вызывают тяжелые деструктивные изменения пересаженной ткани, органа и воспалительную реакцию со стороны окружающих трансплантат тканей.
Деструктивные и реактивные изменения в месте нахождения трансплантанта заключаются в следующем: через несколько дней наблюдается набухание эндотелия и базальных мембран сосудов, дистрофические и некробиотические изменения паренхиматозных элементов органа. Позже возникают фибринозный некроз и тромбоз крупных внутриорганных сосудов. С первых дней вокруг пересаженной ткани или органа развивается воспалительная инфильтрация, она возникает, прежде всего, вокруг кровеносных сосудов. Инфильтрат состоит из лимфоидных клеток, гистиоцитов, плазмоцитов. Соотношение этих клеток бывает различным в зависимости от вида трансплантируемой ткани и стадии развития отторжения трансплантанта.
В случаях гомо-, гетеро- и даже аутотрансплантации эти процессы приводят к гибели и отторжению трансплантанта. Реакция отторжения трансплантанта по своему типу и механизму относятся к аллергическим реакциям замедленного типа. В случае реакции отторжения трансплантант отмирает, а воспалительный процесс вызывает его отторжение. После отторжения в ткани происходит процесс рубцевания и эпителизации.
Влияние трансплантанта на организм реципиента
Питаются трансплантанты вначале за счет диффузии межтканевой жидкости реципиента. В дальнейшем из тканей реципиента врастают в трансплантат сосуды. Происходит восстановление питания его пластической части, и она начинает регенерировать. Центральная часть трансплантанта обычно отмирает из-за плохого питания. Чтобы трансплантированный орган не погиб от кислородного голодания, необходимо по возможности сшить его сосуды с сосудами окружающей ткани реципиента. Приживлению трансплантанта могут способствовать неспецифические биогенные стимуляторы белковой природы. Они накапливаются в тканях и активируют физиологические процессы организма, в том числе кроветворение, усиливая тем самым процессы регенерации. Однако эксперименты показали, что трансплантант способен вызывать у реципиента не только стимулирующий эффект, но и отрицательные явления. Если новорожденным животным трансплантировать клетки системы мононуклеарных фагоцитов взрослого животного (клетки селезенки, костного мозга, лимфатических узлов), то у реципиента развивается заболевание, характеризующееся отставанием роста и снижением массы животного. Одновременно наблюдают гипертрофию селезенки, печени и атрофию лимфоидного аппарата. У животного выпадают волосы, отслаиваются эпидермис, расстраивается пищеварение. Через 2–3 недели животное может погибнуть из-за того, что в ретикуло-макрофагальной системе преобладают гистиоциты донора. Последние проникают в лимфатическую систему и селезенку, разрушают лимфоидные и другие элементы реципиента и вырабатывают против них антитела. В значительной части реакция отторжения является иммунологическим процессом. В результате тканевой несовместимости донора и реципиента трансплантант отторгается. В организме реципиента клетки трансплантанта становятся антигенами и вызывают выработку антител и локализацию лимфоидных элементов. Антитела против трансплантанта относятся к комплементосвязывающим (агглютинины), появляются также гемагглютинины, преципитины и другие виды антител.
Клеточная защитная реакция организма реципиента состоит в мобилизации иммунокомпетентных клеток (гистиоцитов, макрофагов, плазматических клеток, лимфоидных элементов).
Для успешного осуществления трансплантации в организме реципиента создают явление толерантности (от лат. tolerantio) – терпимость иммунной системы организма к чужеродным для нее антигенам. При этом иммуннокомпетентная система не вырабатывает антител или иммунных лимфоцитов, или они вырабатываются, но не уничтожают антиген.
Толерантность может быть: патологическая, физиологическая, искусственная, лечебная.
Искусственная и лечебная толерантность создаются с помощью иммунодепрессантов, цитостаттиков, ионизирующего излучения. Они обуславливают лизис, торможение или блокаду деления, созревания клеток иммунно-компетентной системы.
Патологическая толерантность – это терпимость иммунной системы организма к чужеродным антигенам: бактерии, вирусы, грибки, паразиты, клетки злокачественных опухолей, трансплантанты. Это происходит потому, что нарушена функция иммуннокомпентной системы, т.е. имеет место иммунодефицитное состояние.
Иногда специфические иммуноглобулины взаимодействуют с антигенами, но не лизируют их, не убивают, т.е. экранируют чужеродные клетки (закрывают). Более того, экранированные иммуноглобулинами клетки способны интенсивно размножаться. Этот феномен в онкологии описан как феномен опухолевого роста при активации гуморального иммунитета.
Патологическая толерантность может развиваться при повышении активности Т и В лимфоцитов киллеров и плазматических клеток.
Физиологическая толерантность – толерантность к антигенам собственных белков и клеток организма (изоляционная толерантность). Это явление распространяется на антигены клеток тканей изолированных от иммунокомпетентных систем физиологическими барьерами (ткани мозга, семенников, щитовидной железы, глаз, которые изолированы гистогематическим, гематоэнцефалическим, гематоофтальмическим и другими барьерами).
Пути преодоления тканевой несовместимости
Преодоление тканевой несовместимости является важнейшей задачей в успешной пересадке тканей, органов. Существуют неспецифические и специфические методы преодоления тканевой несовместимости.
К неспецифическим методам относится подавление иммунологической реактивности организма реципиента с помощью различных иммунодепрессантов, таких как циклоспорин А, цитотоксические препараты, антилимфоцитарная сыворотка, облучение гамма–лучами, лучами Рентгена.
К специфическим методам подавления тканевой несовместимости относятся:
1. Подбор иммунологически совместимых пар донора и реципиента.
2. Приучивание реципиента к антигенам донора путем предварительных многократных взаимообменных переливаний крови донора и реципиента.
На успешность трансплантации влияют свежесть трансплантанта, генетическое родство донора и реципиента, их возраст, место пересадки (вид пересаживаемой ткани), общее состояние организма.
Date: 2015-06-11; view: 2490; Нарушение авторских прав