
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задания для самостоятельной работы. Дан кубик породы размером 10х10х10 см
|
|
Дан кубик породы размером 10х10х10 см. Определить дебиты (Q1),(Q2),(Q3),(Q4),(Q5)при:
1. равномерной субкапиллярной и неравномерно-проницаемой фильтрациях;
2. равномерной субкапиллярной и трещиноватой фильтрациях
и сравнить их для условий, представленных в таблице 3.1, имеющих следующие обозначения:
kпр – проницаемость при субкапиллярной фильтрации, мД;
m – вязкость жидкости, спз;
∆Р/L – перепад давления, атм/м;
Nк – число капилляров;
Dк – диаметр капилляра, мм;
Lтр – длина трещин, см;
hтр – высота трещины, мм;
Мтр – число трещин;
1,..., 120 – номер варианта.
Таблица 3.1
| B | |||||||||||
| kпр | |||||||||||
| m | 2,0 | 1,3 | 3,0 | 2,5 | 3,0 | 1,5 | 2,0 | 1,3 | 3,0 | 1,2 | 1,4 |
| ΔP/L | 0,3 | 0,26 | 0,31 | 0,32 | 0,33 | 0,35 | 0,3 | 0,36 | 0,31 | 0,28 | 0,26 |
| Nk | |||||||||||
| Dk | 0,18 | 0,2 | 0,22 | 0,24 | 0,25 | 0,16 | 0,3 | 0,27 | 0,28 | 0,24 | 0,16 |
| Lтр | |||||||||||
| hтр | 0,15 | 0,16 | 0,18 | 0,17 | 0,19 | 0,22 | 0,21 | 0,28 | 0,27 | 0,28 | 0,23 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 1,8 | 2,0 | 2,2 | 2,5 | 3,0 | 2,8 | 2,2 | 1,1 | 1,3 | 1,1 | 1,8 |
| ΔP/L | 0,3 | 0,24 | 0,22 | 0,23 | 0,26 | 0,25 | 0,3 | 0,36 | 0,26 | 0,27 | 0,24 |
| Nk | |||||||||||
| Dk | 0,15 | 0,22 | 0,23 | 0,24 | 0,33 | 0,28 | 0,26 | 0,3 | 0,18 | 0,19 | 0,21 |
| Lтр | |||||||||||
| hтр | 0,22 | 0,21 | 0,23 | 0,19 | 0,22 | 0,23 | 0,25 | 0,26 | 0,27 | 0,28 | 0,22 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 1,6 | 1,9 | 2,0 | 3,0 | 1,4 | 1,8 | 1,6 | 2,2 | 2,0 | 2,1 | 1,3 |
| ΔP/L | 0,2 | 0,22 | 0,24 | 0,25 | 0,31 | 0,32 | 0,28 | 0,24 | 0,25 | 0,28 | 0,31 |
| Nk | |||||||||||
| Dk | 0,22 | 0,23 | 0,25 | 0,26 | 0,27 | 0,28 | 0,3 | 0,31 | 0,29 | 0,28 | 0,18 |
| Lтр | |||||||||||
| hтр | 0,24 | 0,26 | 0,28 | 0,16 | 0,25 | 0,26 | 0,27 | 0,18 | 0,23 | 0,24 | 0,22 |
| Мтр |
Продолжение табл. 3.1
| B | |||||||||||
| kпр | |||||||||||
| m | 1,6 | 1,7 | 3,0 | 1,6 | 1,8 | 1,9 | 2,8 | 3,0 | 2,0 | 2,0 | 1,3 |
| ΔP/L | 0,4 | 0,28 | 0,35 | 0,37 | 0,39 | 0,4 | 0,22 | 0,28 | 0,3 | 0,28 | 0,24 |
| Nk | |||||||||||
| Dk | 0,22 | 0,26 | 0,3 | 0,31 | 0,28 | 0,29 | 0,26 | 0,2 | 0,25 | 0,18 | 0,2 |
| Lтр | |||||||||||
| hтр | 0,2 | 0,26 | 0,26 | 0,28 | 0,29 | 0,3 | 0,18 | 0,26 | 0,24 | 0,27 | 0,18 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 3,0 | 2,5 | 3,0 | 1,5 | 1,3 | 3,0 | 1,2 | 1,4 | 1,8 | 2,0 | |
| ΔP/L | 0,25 | 0,28 | 0,31 | 0,4 | 0,28 | 0,35 | 0,37 | 0,39 | 0,4 | 0,22 | 0,28 |
| Nk | |||||||||||
| Dk | 0,22 | 0,24 | 0,25 | 0,16 | 0,3 | 0,27 | 0,28 | 0,24 | 0,16 | 0,15 | 0,22 |
| Lтр | |||||||||||
| hтр | 0,23 | 0,24 | 0,22 | 0,2 | 0,26 | 0,26 | 0,28 | 0,29 | 0,3 | 0,18 | 0,26 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 2,2 | 2,5 | 3,0 | 2,8 | 2,2 | 1,1 | 1,3 | 1,1 | 1,8 | 1,6 | 1,9 |
| ΔP/L | 0,3 | 0,23 | 0,26 | 0,25 | 0,3 | 0,36 | 0,26 | 0,27 | 0,24 | 0,2 | 0,22 |
| Nk | |||||||||||
| Dk | 0,23 | 0,24 | 0,33 | 0,28 | 0,26 | 0,3 | 0,22 | 0,19 | 0,21 | 0,22 | 0,23 |
| Lтр | |||||||||||
| hтр | 0,24 | 0,15 | 0,16 | 0,18 | 0,17 | 0,19 | 0,18 | 0,21 | 0,28 | 0,27 | 0,28 |
| Мтр |
Продолжение табл. 3.1
| B | |||||||||||
| kпр | |||||||||||
| m | 2,0 | 3,0 | 1,4 | 1,8 | 1,6 | 2,2 | 2,0 | 2,1 | 1,3 | 1,6 | 1,7 |
| ΔP/L | 0,24 | 0,25 | 0,31 | 0,32 | 0,3 | 0,26 | 0,31 | 0,32 | 0,33 | 0,35 | 0,3 |
| Nk | |||||||||||
| Dk | 0,25 | 0,26 | 0,27 | 0,28 | 0,3 | 0,31 | 0,29 | 0,28 | 0,18 | 0,2 | 0,26 |
| Lтр | |||||||||||
| hтр | 0,23 | 0,22 | 0,21 | 0,23 | 0,19 | 0,22 | 0,23 | 0,25 | 0,26 | 0,27 | 0,28 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 2,8 | 2,2 | 1,1 | 1,3 | 1,1 | 1,8 | 1,6 | 1,3 | 2,5 | ||
| ΔP/L | 0,28 | 0,31 | 0,4 | 0,28 | 0,35 | 0,37 | 0,39 | 0,4 | 0,3 | 0,32 | 0,33 |
| Nk | |||||||||||
| Dk | 0,26 | 0,3 | 0,18 | 0,19 | 0,21 | 0,22 | 0,23 | 0,25 | 0,25 | 0,16 | 0,3 |
| Lтр | |||||||||||
| hтр | 0,23 | 0,24 | 0,22 | 0,2 | 0,26 | 0,26 | 0,28 | 0,29 | 0,21 | 0,28 | 0,27 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 1,5 | 1,3 | 1,2 | 1,4 | 1,8 | 2,2 | 2,8 | ||||
| ΔP/L | 0,35 | 0,3 | 0,36 | 0,31 | 0,28 | 0,26 | 0,3 | 0,24 | 0,22 | 0,23 | 0,3 |
| Nk | |||||||||||
| Dk | 0,27 | 0,28 | 0,24 | 0,16 | 0,15 | 0,22 | 0,23 | 0,24 | 0,33 | 0,28 | 0,18 |
| Lтр | |||||||||||
| hтр | 0,28 | 0,23 | 0,22 | 0,21 | 0,23 | 0,19 | 0,22 | 0,25 | 0,25 | 0,26 | 0,22 |
| Мтр |
Продолжение табл. 3.1
| B | |||||||||||
| kпр | |||||||||||
| m | 2,2 | 1,1 | 1,3 | 1,1 | 1,8 | 1,6 | 2,1 | 1,3 | 1,6 | 1,7 | |
| ΔP/L | 0,36 | 0,26 | 0,27 | 0,24 | 0,2 | 0,22 | 0,25 | 0,31 | 0,4 | 0,28 | 0,35 |
| Nk | |||||||||||
| Dk | 0,19 | 0,21 | 0,22 | 0,23 | 0,25 | 0,26 | 0,28 | 0,26 | 0,3 | 0,31 | 0,28 |
| Lтр | |||||||||||
| hтр | 0,24 | 0,26 | 0,28 | 0,16 | 0,28 | 0,25 | 0,18 | 0,28 | 0,29 | 0,3 | 0,18 |
| Мтр | |||||||||||
| B | |||||||||||
| kпр | |||||||||||
| m | 2,8 | 2,5 | 2,2 | 1,8 | 1,3 | ||||||
| ΔP/L | 0,26 | 0,26 | 0,23 | 0,3 | 0,28 | 0,22 | 0,4 | 0,35 | 0,28 | 0,25 | |
| Nk | |||||||||||
| Dk | 0,24 | 0,23 | 0,22 | 0,15 | 0,16 | 0,24 | 0,28 | 0,21 | 0,25 | 0,29 | |
| Lтр | |||||||||||
| hтр | 0,22 | 0,18 | 0,3 | 0,28 | 0,28 | 0,26 | 0,22 | 0,27 | 0,24 | 0,28 | |
| Мтр |
Состояние нефтяных газов в пластовых условиях
Теория к разделу
В пластовых условиях газы в зависимости от их состава, давления и температуры (термобарического режима в пласте) могут находиться в различных агрегатных состояниях – газообразном, жидком, в виде газожидкостных смесей.
Природные газы, добываемые из газовых, газоконденсатных и нефтяных месторождений, состоят из углеводородов (УВ) метанового ряда СН4-С4Н10: метана, этана, пропана, изобутана и н-бутана, а также неуглеводородных компонентов: H2S, N2, CO, CO2, H2, Ar, He, Kr, Xe и других.
Состав газовых смесей выражается в виде массовой или объемной концентрации компонентов в процентах и мольных долях:
 , (4.1)
, (4.1)
где Ni - масса i-го компонента;
Σ Ni - суммарная масса смеси.
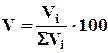 , (4.2)
, (4.2)
где Vi - объем i-го компонента в смеси;
Σ Vi - суммарный объем газа.
 , (4.3)
, (4.3)
где ni - число молей i-го компонента в смеси;
Σ ni - суммарное число молей газа в системе.
Уравнение состояния Клапейрона–Менделеева связывает давление, температуру и объем газа, представленного в виде физически однородной системы, при условиях термодинамического равновесия.
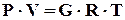 , (4.4)
, (4.4)
где Р – давление, Па;
V – объем газа, м3;
G – масса газа, кг;
R – газовая постоянная, Дж/(кг • К);
T – абсолютная температура, К.
Газовая постоянная R численно равна работе расширения 1 кг идеального газа в изобарическом процессе при увеличении температуры газа на 1 К.
Уравнение состояния Клапейрона–Менделеева справедливо для идеального газа и для нефтяных систем работает в области давлений, близких к атмосферному. При давлениях Р > 10 атм нефтяной газ из идеальной системы переходит в неидеальную и описывается уравнением Клайперона-Менделеева с коэффициентом сжимаемости z, который учитывает отклонение реальных газов от законов сжатия и расширения идеальных газов.
Ниже записано уравнение состояния смеси газов в пластовых условиях, выраженное через мольные доли компонентов:
 . (4.5)
. (4.5)
Коэффициент сжимаемости газа z функционально зависит от приведенных давлений и температур, z = f (Tприв, Рприв).
С приближением давления и температуры к их критическим значениям свойства газовой и жидких фаз становятся одинаковыми, поверхность раздела между ними исчезает и плотности их уравниваются.
Критическая температура (Ткр) – максимальная температура, при которой свойства газовой и жидкой фаз находятся в равновесии.
Критическое давление (Ркр) – давление паров вещества при критической температуре.
Среднекритические (псевдокритические) параметры смеси газов определяются по правилу аддитивности:
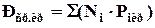 , (4.6)
, (4.6)
 . (4.7)
. (4.7)
Приведенными параметрамисмеси газов называются безразмерные величины, показывающие, во сколько раз действительные параметры состояния газа: температура, давление, объем, плотность и другие больше или меньше среднекритических.
 , (4.8)
, (4.8)
 . (4.9)
. (4.9)
В соответствии с законом Авогадро один моль газа занимает объем при нормальных условиях 22,414 л, а при стандартных условиях 24,055л.
Нормальным условиям (н.у.) соответствуют абсолютная температура 273,15 К и абсолютное давление 0,1 МПа.
Стандартным условиям (с.у.) соответствуют температура 20°С (293,15 К) и абсолютное давление 0,1 МПа.
Объем газа в пластовых условиях определяется из соотношения Бойля-Мариотта:
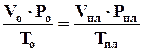 , (4.10)
, (4.10)
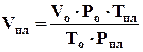 , (4.11)
, (4.11)
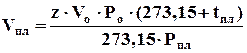 . (4.12)
. (4.12)
Объемный коэффициент газа оценивается отношением объема газа в пластовых условиях к объему, занимаемому газом при н.у.:
 , (4.13)
, (4.13)
 . (4.14)
. (4.14)
Типовая задача
Дана исходная таблица. Используя ее, мы определяем коэффициенты сжимаемости (z) и объемный коэффициент газа (b), занимающего первоначальный объем (Vо) 1000 м3 при нормальных условиях для пластовых условий: Рпл = 100 атм, tпл = 50°С, следующего состава (Vi,%) (табл. 4.1):
Таблица 4.1
| Компонент, Vi | % |
| метан (СН4) | |
| этан (С2H6) | |
| пропан (C3H8) | 5,1 |
| изобутан (i-C4H10) | 0,8 |
| н-бутан (n-C4H10) | 1,7 |
| изопентан (i-C5H12) | 0,6 |
| н-пентан (n-C5H12) | 0,3 |
| гексаны (C6H12) | 0,5 |
Решение:
1) Рассчитываем приведенное давление по формуле:
 . (4.15)
. (4.15)
Для расчета Рпр и Tпр используем критическое давление и критическую температуру смеси газов. Данные для каждого компонента представлены в таблице 4.2.
Таблица 4.2
| Компонент | Ni, доли | Pкр, атм | Ткр, К | Ni • Pi кр, атм | Ni • Ti кр, К |
| СН4 | 0,82 | 47,32 | 38,80 | 156,62 | |
| С2H6 | 0,09 | 49,78 | 4,48 | 27,45 | |
| C3H8 | 0,051 | 43,38 | 2,21 | 18,87 | |
| i-C4H10 | 0,008 | 38,25 | 0,31 | 3,26 | |
| n-C4H10 | 0,017 | 38,74 | 0,66 | 7,23 | |
| i-C5H12 | 0,006 | 33,89 | 0,20 | 2,77 | |
| n-C5H12 | 0,003 | 34,1 | 0,10 | 1,41 | |
| C6H12 | 0,005 | 30,52 | 0,15 | 2,54 | |
| S = 46,92 | S = 220,14 |
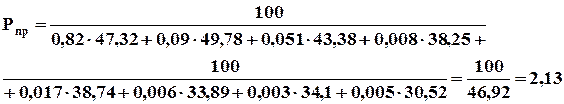
2) Рассчитываем приведенную температуру по формуле:
 . (4.16)
. (4.16)
Для расчета Tпр используем критические температуры компонентов Тi кр. Данные для каждого компонента представлены в таблице 4.2.
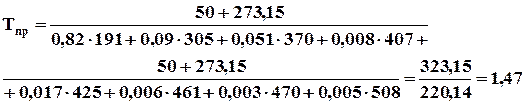
3) Определяем z по графикам z = f (P) при Т = const (рис.4.1), (Оркин К. Г. стр. 90, Гиматудинов Ш.К. стр. 97, Амикс Дж. cтр. 237). Для нашего случая z = 0,81.
4) Объем газа в пластовых условиях определяем, используя закон Бойля–Мариотта (формула 4.12):
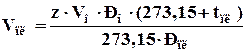 ,
,
 .
.
5) Объемный коэффициент газа оценивается отношением объемов газа в пластовых условиях к объему при н.у. (формула 4.14):
 ,
,
 .
.

Рис. 4.1.Графики зависимости коэффициента сверхсжимаемости Z углеводородного газа от приведенных псевдокритических давления Рпр и температуры Тпр (по Г.Г. Брауну). Шифр кривых – значения Тпр
Date: 2016-05-24; view: 1218; Нарушение авторских прав