
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основные аминокислоты
|
|
|
|
1. 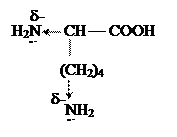 Лизин (лиз)
Лизин (лиз)
|
|
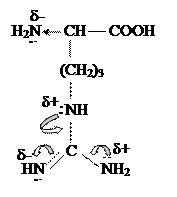 Аргинин (арг)
Аргинин (арг)
3. Гистидин (гис)
 | |||||
| |||||
| |||||
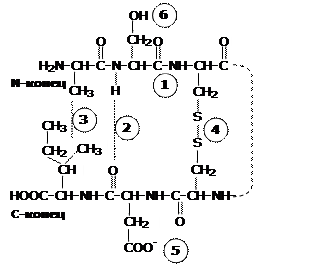 1 – пептидная (амидная)
1 – пептидная (амидная)
2 – водородная
3 – гидрофобное взаимодействие
4 – бисульфидный мостик
5 – вероятность ионной
6 – вероятность сложно- или простой эфирной связей
Схема 1. Типы связей в полипептидной цепи
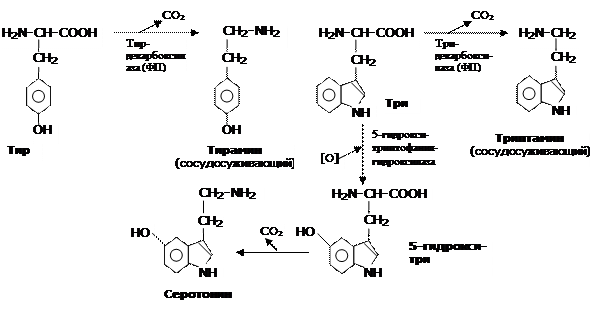
Рис.1. Декарбоксилирование аминокислот

Глу, асп – кислые аминокислоты, наличие у них отрицательного заряда позволяет взаимодействовать с НАД+, т.е. подвергаться вначале окислению с последующим дезаминированием:
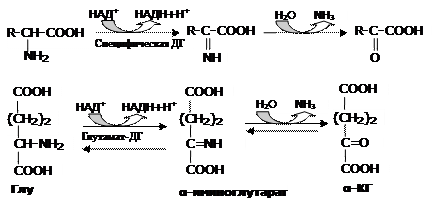
Рис.2. Реакции прямого дезаминирования
Трансаминирование (переаминирование, непрямое дезаминирование) – перенос аминогруппы с аминокислоты на 2-оксокислоту без промежуточного образования аммиака.
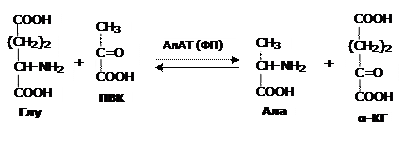
Роль кофермента выполняет активная (фосфорилированная) форма витамина В6 (пиридоксол), который может находиться в двух формах: альдегида и амина.
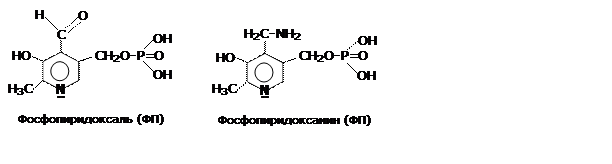
В основе реакции лежит способность альдегидов и аминов взаимодействовать по механизму «присоединения-отщепления» (АN).

Примечание: ФП – фосфопиридоксол, Е – энзим; S-Е-комплекс – субстрат-ферментный комплекс
Рис.3. Механизм переаминирования аминокислот
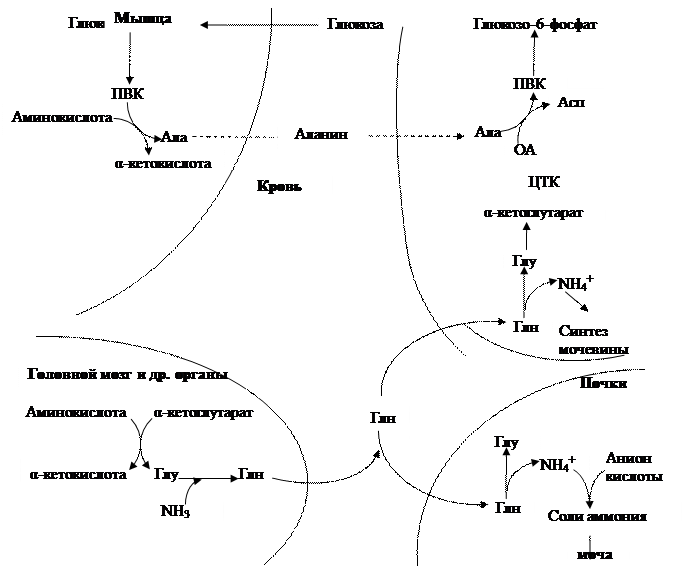
Рис.4. Глюкозо-аланиновый и орнитиновый циклы
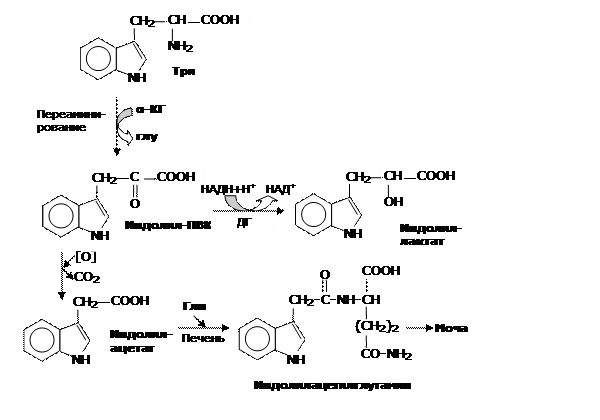
Примечание: α-КГ – альфа-кетоглутарат
Рис.5. Преобразование триптофана неспецифическим путем

Рис.6. Катаболизм цистеина
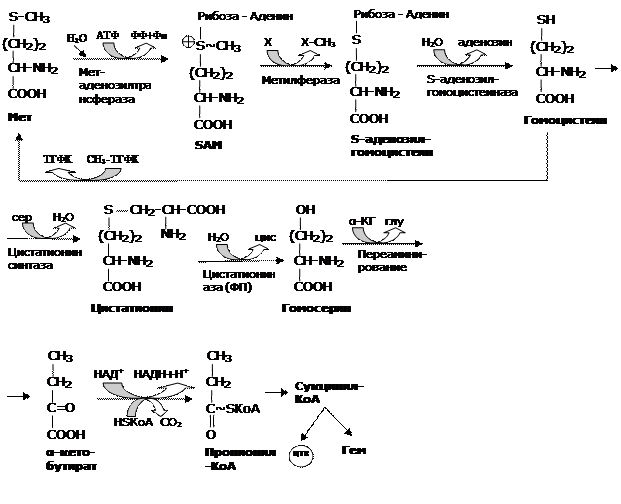
Примечание: Х – вещество, подвергающееся метилированию; Х-СН3 – продукт метилирования; ФП – активная форма витамина В6
Рис.7. Катаболизм метионина
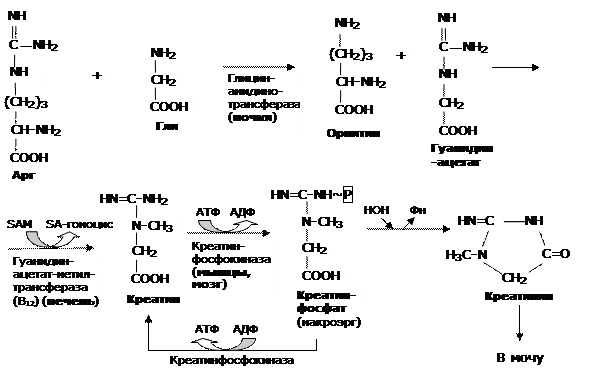
Рис.8. Обмен креатина

Рис.9. Распад фенилаланина и тирозина
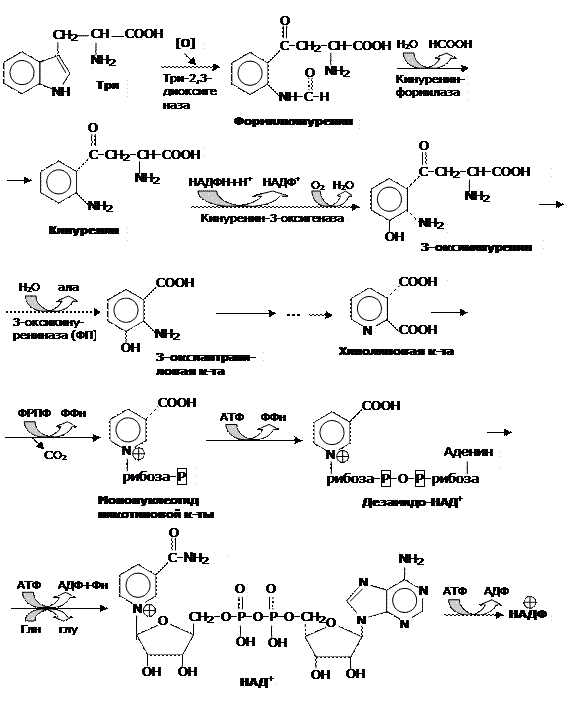
Примечание: ФРПФ – фосфорибозилпирофосфат
Рис.10. Специфический (кинурениновый) путь распада триптофана
Date: 2015-05-22; view: 960; Нарушение авторских прав