
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Состав и характеристики атомных ядер. Ядро атома состоит из частиц, называемых нуклонами
|
|
Ядро атома состоит из частиц, называемых нуклонами. К нуклонам относятся частицы двух типов: протоны и нейтроны. Протон р имеет положительный заряд, значение которого в точности равно элементарному электрическому заряду е. Нейтрон п является нейтральной частицей. Число Z протонов в ядре какого-либо атома равно порядковому номеру элемента в таблице Менделеева. Это число называется зарядовым числом. Таким образом, ядро с порядковым номером Z обладает зарядом + Ze.
В качестве единицы массы в ядерной физике используется атомная единица массы (сокращенно а.е.м.), равная 1/12 массы атома углерода 126 С:
1 a.e.м. = 1,6605 · 10-27 кг .
Массу ядра принято обозначать буквой М. Целое число А, ближайшее к численному значению массы М какого-либо атомного ядра, выраженному в атомных единицах массы, называется массовым числом. Число А есть число нуклонов в ядре. При этом число N нейтронов в ядре равно
N = A – Z
Состав ядра какого-либо химического элемента определяется значением массового числа А, которое пишут слева вверху около символа X, обозначающего этот элемент, и значением зарядового числа Z - слева внизу:
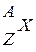
Атомы, ядра которых имеют одинаковый заряд + Z е, но различные массы, называются изотопами. Примерами изотопов одного элемента являются три изотопа водорода:
протий 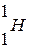 , дейтерий
, дейтерий 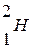 и тритий
и тритий 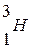
Масса нейтрона тп = 1,00866 а.е.м. превосходит массу протона тр = = 1,00728 а.е.м. более чем на две массы электрона те = 5,49-10 -4 а.е.м. Точные измерения масс атомных ядер показали, что масса любого ядра меньше суммы масс входящих в него нуклонов:
M<Zmp+Nmn. (23.1)
Величина
Δ m = Zmp + Nmn - M (23.2)
называется дефектом массы ядра.
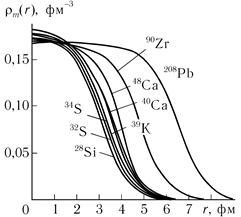
Атомные ядра имеют почти сферическую форму. Радиус ядра определяется приближенной формулой
R = R 0 A 1/3
где Ro= 1,3 · 10-15 м .
Date: 2015-05-19; view: 774; Нарушение авторских прав