
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основные теоретические положения. Спектры атомов подразделяют на спектры испускания и спектры поглощения
|
|
Спектры атомов подразделяют на спектры испускания и спектры поглощения. Для получения спектра испускания водорода его необходимо разогреть до высокой температуры и излучение пропустить через оптическую систему, состоящую из коллиматора и призмы. При этом на экране, размещенном за призмой, можно наблюдать тонкие цветные линии, образующие спектральную серию, называемую серией Бальмера. Частоты 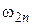 спектральных линий серии Бальмера определяются из формулы:
спектральных линий серии Бальмера определяются из формулы:
 ,
, 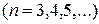 , (2.1)
, (2.1)
где 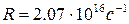 – постоянная Ридберга.
– постоянная Ридберга.
Кроме одной спектральной серии, расположенной в видимой части спектра, у водорода имеется одна спектральная серия в ультрафиолете, называемая серией Лаймана:
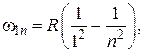
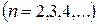 , (2.2)
, (2.2)
а также спектральные серии в инфракрасной части спектра:
 , (n = 4, 5, 6… – серия Пашена), (2.3)
, (n = 4, 5, 6… – серия Пашена), (2.3)
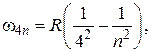 (n = 5, 6, 7… – серия Брэкета), (2.4)
(n = 5, 6, 7… – серия Брэкета), (2.4)
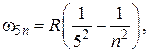 (n = 6, 7, 8… – серия Пфунда).
(n = 6, 7, 8… – серия Пфунда).  (2.5)
(2.5)
В низкочастотной области спектр атома водорода простирается вплоть до радиодиапазона. В настоящее время в спектре межзвездного водорода обнаружены спектральные линии, соответствующие длинам волн 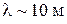 .
.
Таким образом, спектр атома водорода разбивается на группы – спектральные серии, каждая из которых представляет собой совокупность спектральных линий с характерной закономерностью в своей последовательности и сходящихся к некоторому пределу – границе серии. Если обратить внимание на структуру соотношений (2.1) – (2.5), то видно, что все они могут быть представлены в общем виде:
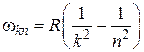 , (2.6)
, (2.6)
где 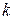 и
и  целые числа, причем
целые числа, причем 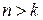 . Соотношение (2.6) называют обобщенной формулой Бальмера.
. Соотношение (2.6) называют обобщенной формулой Бальмера.
Спектр поглощения водорода можно получить при пропускании через него электромагнитного излучения с непрерывным спектром. Тогда после прохождения через коллиматор и призму излучение на экране разворачивается в спектр, представляющий собой радугу, на фоне которой заметны тонкие черные полоски. Черным полоскам соответствуют частоты, определяемые формулой (2.6). Таким образом, спектр излучения и спектр поглощения водорода взаимно дополняют друг друга до радуги.
Атом каждого химического элемента обладает своим уникальным спектром. Поэтому на исследовании спектрального состава излучения основан важнейший метод химического анализа. Наличие в смеси того или иного химического элемента может быть установлено по присутствию в спектре излучения его характерных спектральных линий.
Из анализа спектральных линий может быть получена и другая важная информация, например, о температуре и концентрации вещества в смеси. Данный метод исследования особенно широко применяется в астрофизике, поскольку вещество удаленных космических объектов недоступно для других методов химического анализа. В настоящее время исследование спектров излучения позволило установить химический состав звезд, межзвездной среды и целого ряда других космических объектов.
Изучение атомных спектров послужило ключом к пониманию строения атома. Оказалось, что все попытки объяснения особенностей атомных спектров в рамках классической физики не увенчались успехом. Удовлетворительная теория атома водорода, основанная на положениях, выходящих за рамки классических представлений, была создана в 1913 году датским физиком Нильсом Бором. Данная теория основана на следующих постулатах:
1. Электрон в атоме может находиться лишь на некоторых орбитах, называемых стационарными. Находясь на стационарной орбите, электрон не излучает и не поглощает электромагнитную энергию.
2. При переходе с одной стационарной орбиты на другую электрон излучает или поглощает квант электромагнитной энергии, равный разности энергий соответствующих стационарных состояний:
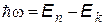 , (2.7)
, (2.7)
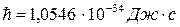 – приведенная постоянная Планка.
– приведенная постоянная Планка.
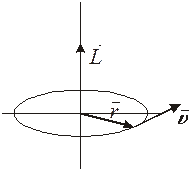
Из всех орбит электрона в атоме водорода оказываются возможными только те, на которых момент импульса L электрона принимает значения, кратные постоянной Планка. Тогда, считая орбиту круговой, запишем:
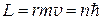 ,
, 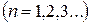 . (2.8)
. (2.8)
Равенство (2.8) называется условием квантования орбит.
Определим радиусы 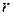 стационарных орбит. Для электрона, движущегося по круговой орбите вокруг протона, запишем второй закон Ньютона:
стационарных орбит. Для электрона, движущегося по круговой орбите вокруг протона, запишем второй закон Ньютона:

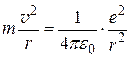 , (2.9)
, (2.9)
где 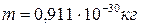 – масса электрона,
– масса электрона,  – заряд электрона,
– заряд электрона, 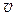 – скорость электрона,
– скорость электрона, 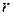 – радиус орбиты.
– радиус орбиты.
Используя боровское условие квантования (2.8) и исключая из (2.9) 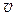 , находим:
, находим:
 ,
, 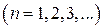 . (2.10)
. (2.10)
Энергия электрона, находящегося на орбите с номером  , определяется соотношением:
, определяется соотношением:
 , (2.11)
, (2.11)
где первое слагаемое в правой части представляет собой кинетическую, а второе – потенциальную энергию взаимодействия электрона с ядром. Из (2.11) с использованием (2.10) и (2.8) находим:
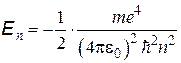 . (2.12)
. (2.12)
Используя второй постулат Бора, получаем:
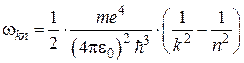 . (2.13)
. (2.13)
Сравнивая (2.13) с (2.6), видим, что множитель, стоящий перед скобками в правой части (2.13), представляет собой постоянную Ридберга. Таким образом:
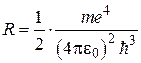 . (2.14)
. (2.14)
Теоретическое и экспериментальное значения 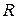 совпадают с высокой степенью точности, что свидетельствует о справедливости основных положений теории Бора.
совпадают с высокой степенью точности, что свидетельствует о справедливости основных положений теории Бора.
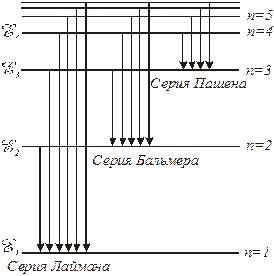 Становится очевидной также природа спектральных серий атома водорода. На рис. 2.2 схематически представлены энергетические уровни атома водорода. Серия Лаймана (2.2) образована в результате излучения квантов электромагнитной энергии при переходе электрона с более высоко лежащих энергетических уровней на уровень с
Становится очевидной также природа спектральных серий атома водорода. На рис. 2.2 схематически представлены энергетические уровни атома водорода. Серия Лаймана (2.2) образована в результате излучения квантов электромагнитной энергии при переходе электрона с более высоко лежащих энергетических уровней на уровень с 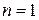 , серия Бальмера (2.1) – при переходе на уровень с
, серия Бальмера (2.1) – при переходе на уровень с 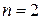 , серия Пашена (2.3) – при переходе на уровень с
, серия Пашена (2.3) – при переходе на уровень с 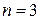 и т. д.
и т. д.
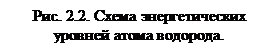 Спектр поглощения образуется при переходах электронов в атомах водорода снизу вверх. При этом электрон поглощает квант электромагнитной энергии, и атом оказывается в возбужденном состоянии.
Спектр поглощения образуется при переходах электронов в атомах водорода снизу вверх. При этом электрон поглощает квант электромагнитной энергии, и атом оказывается в возбужденном состоянии.
Объединенная формула Бальмера (2.6) позволяет по известной частоте (длине волны) спектральной линии определить постоянную Ридберга:
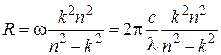 . (2.15)
. (2.15)
Соотношение (2.14) позволяет определить по известному значению постоянной Ридберга постоянную Планка:
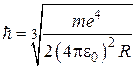 . (2.16)
. (2.16)
Date: 2015-05-19; view: 906; Нарушение авторских прав