
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

До квантовые модели атома (Томсон, Резерфорд, Бор)
|
|
Развитие исследований радиоактивного излучения, с одной стороны, и квантовой теории — с другой, привели к созданию квантовой модели атома Резерфорда — Бора. Но созданию этой модели предшествовали попытки построить модель атома на основе представлений классической электродинамики и механики. В 1904 г. появилась публикация о строении атома, принадлежащая английскому физику Д. Д. Томсону.
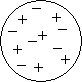 В атоме Томсона положительное электричество «размазано» по сфере, в которую вкраплены, как изюм в пудинг, электроны. В простейшем атоме водорода электрон находится в центре положительно заряженной сферы. При смещении из центра на электрон действует квазиупругая сила электростатического притяжения, под действием которой электрон совершает колебания. Частота этих колебаний определяется радиусом сферы, зарядом и массой электрона, и если радиус сферы имеет порядок радиуса атома, частота этих колебаний совпадает с частотой колебания спектральной линии атома. В многоэлектронных атомах электроны располагаются по устойчивым конфигурациям, рассчитанным Томсоном. Томсон считал каждую такую конфигурацию определяющей химические свойства атомов. Он предпринял попытку теоретически объяснить периодическую систему элементов Д. И. Менделеева. Отметив, что теория Томсона оказалась несовместимой с опытными фактами, Бор тем не менее считал, что эта теория «содержит много оригинальных мыслей и оказала большое влияние на развитие атомной теории».
В атоме Томсона положительное электричество «размазано» по сфере, в которую вкраплены, как изюм в пудинг, электроны. В простейшем атоме водорода электрон находится в центре положительно заряженной сферы. При смещении из центра на электрон действует квазиупругая сила электростатического притяжения, под действием которой электрон совершает колебания. Частота этих колебаний определяется радиусом сферы, зарядом и массой электрона, и если радиус сферы имеет порядок радиуса атома, частота этих колебаний совпадает с частотой колебания спектральной линии атома. В многоэлектронных атомах электроны располагаются по устойчивым конфигурациям, рассчитанным Томсоном. Томсон считал каждую такую конфигурацию определяющей химические свойства атомов. Он предпринял попытку теоретически объяснить периодическую систему элементов Д. И. Менделеева. Отметив, что теория Томсона оказалась несовместимой с опытными фактами, Бор тем не менее считал, что эта теория «содержит много оригинальных мыслей и оказала большое влияние на развитие атомной теории».
Такой статической моделью был атом Кельвина — Томсона. И эта модель была общепринятой по причинам, указанным Вином.
Модель атома Резерфорда (Ядерная или Планетарная модель атома)
Рассеяние отдельных α-частиц на большие углы Резерфорд объяснил тем, что положительный заряд в атоме не распределен равномерно в шаре радиусом 10-10м, как предполагали ранее, а сосредоточен в центральной части атома в области значительно меньших размеров. Расчеты Резерфорда показали, что для объяснения опытов по рассеянию α-частиц нужно принять радиус атомного ядра равным примерно 10-15м.
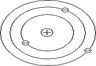 Резерфорд предположил, что атом устроен подобно планетарной системе. Как вокруг Солнца на больших расстояниях от него обращаются планеты, так электроны в атоме обращаются вокруг атомного ядра. Радиус круговой орбиты самого далекого от ядра электрона и есть радиус атома. Такая модель атома была названа планетарной моделью, которая объясняет основные закономерности рассеяния заря
Резерфорд предположил, что атом устроен подобно планетарной системе. Как вокруг Солнца на больших расстояниях от него обращаются планеты, так электроны в атоме обращаются вокруг атомного ядра. Радиус круговой орбиты самого далекого от ядра электрона и есть радиус атома. Такая модель атома была названа планетарной моделью, которая объясняет основные закономерности рассеяния заря 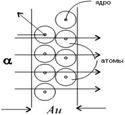 женных частиц.
женных частиц.
При столкновениях с отдельными электронами быстрые заряженные частицы испытывают рассеяние на очень большие углы, так как масса электрона мала. Однако в тех редких случаях, когда быстрая заряженная частица пролетает на очень близком расстоянии от одного из атомных ядер, под действием силы электрического поля атомного ядра может произойти рассеяние заряженной частицы на любой угол до 180°.
Квантовые постулаты Бора
Датский физик Нильс Бор (1885-1962) обосновал планетарную модель атома Резерфорда. Свои представления об особых свойствах атомов (устойчивости атома и спектральных закономерностей его излучения) Бор сформулировал в виде постулатов следующего содержания:
1. Электрон в атоме может находиться только в определенных устойчивых состояниях, называемых стационарными или квантовыми, каждому из которых соответствует определенная энергия En. В этих состояниях атом не излучает электромагнитных волн.
Момент импульса электрона, движущегося по стационарной орбите, имеет квантовые значения, удовлетворяющие условию: meυr = nħ (n = 1,2,3,…), где n – главное квантовое число, me – масса покоя электрона, υ – скорость электрона, r – радиус орбиты, ħ – постоянная Планка.
2. При переходе атома из одного стационарного состояния в другое испускается или поглощается квант энергии ΔE = hν.
Излучение фотона происходит при переходе атома из состояния с большей энергией в состояние с меньшей энергией. При обратном переходе происходит поглощение кванта энергии: hν = En - Em, где n и m – номера состояний.
Все стационарные состояния, кроме одного, являются стационарными лишь условно. Бесконечно долго каждый атом может находиться лишь в стационарном состоянии с минимальным запасом энергии. Это состояние атома называется основным. Все остальные стационарные состояния атома называются возбужденными.
Date: 2015-05-19; view: 792; Нарушение авторских прав