
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Понятие энтропии. Свойства энтропии. Размерность
|
|
Понятие энтропии было впервые введено в 1865 году Рудольфом Клаузиусом. Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение изменения общего количества тепла ΔQ к величине абсолютной температуры T:
. 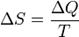
Рудольф Клаузиус дал величине S имя «энтропия», от греческого «энтропос» - возвращение, поворот. Данное равенство относится к изменению энтропии, не определяя полностью саму энтропию.
Эта формула применима только для изотермического процесса (происходящего при постоянной температуре).
Её обобщение на случай произвольного квазистатического процесса выглядит так:
в интегральной форме 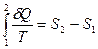
или в дифференциальной форме 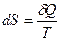 , Þ
, Þ  .,где dS — приращение (дифференциал) энтропии, а δQ — бесконечно малое приращение количества теплоты.
.,где dS — приращение (дифференциал) энтропии, а δQ — бесконечно малое приращение количества теплоты.
Каждое состояние тела характеризуется определенным значением энтропии 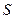 .
.
Тождество Клаузиуса( 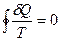 ) говорит, что при замкнутых обратимых процессах энтропия не меняется.
) говорит, что при замкнутых обратимых процессах энтропия не меняется.
Энергия сохраняется, поэтому она не может указывать направление процессов. Все реальные процессы необратимы, поэтому в замкнутых системах они идут в направлении возрастания энтропии. Т.о. энтропия указывает направление реальных процессов. Рост энтропии означает все большую недоступность превращения тепла в работу. Максимум энтропии соответствует состоянию равновесия.
Энтропия экстенсивная величина, она пропорциональна количеству вещества. 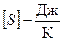 .
.
Энтропия обладает свойством аддитивности: энтропия системы равна сумме энтропий тел, входящих в систему. Этим свойством так же обладают внутренняя энергия, масса, …. Не обладают этим свойством давление, температура. Физический смысл имеет не сама энтропия, а ее изменение.
Обратимые адиабатические процессы, для которых 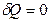 , характеризуются постоянной энтропией
, характеризуются постоянной энтропией 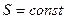 , поэтому их можно назвать изоэнтропийные.
, поэтому их можно назвать изоэнтропийные.
Энтропия изолированной системы при протекании необратимых процессов возрастает.
Энтропия идеального газа является функцией 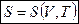 .
.
Выражение для энтропии - функции состояния одного моля идеального газа: 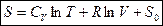 , где
, где 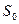 - уровень отсчета энтропии.
- уровень отсчета энтропии.
Date: 2015-05-09; view: 1047; Нарушение авторских прав