
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Опыт 2. Зависимость скорости реакции от природы реагирующих веществ
|
|
В основе опыта лежит взаимодействие мела с соляной и уксусной кислотами:
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;
CaCO3 + 2СН3СООН = (СН3СОО)2 Ca + H2O + CO2↑.
Реактивы и материалы: порошок мела, фильтровальная бумага, 1 М раствор соляной кислоты, 1 М раствор уксусной кислоты.
Посуда и принадлежности: пробирки; микрошпатель.
Методика проведения опыта. Шпателем насыпьте в две пробирки одинаковое количество порошка мела. В одну пробирку налейте 1-2 мл раствора соляной кислоты, в другую – такой же объем раствора уксусной кислоты. Сравните результаты наблюдений в обеих пробирках.
Напишите выражения скоростей проведенных реакций, используя закон действующих масс.
В выводе объясните причины различия скоростей обеих реакций.
Опыт 3. Зависимость скорости реакции от концентрации реагирующих веществ при постоянной температуре (полумикро-метод)
В основе опыта лежит реакция, протекающая по уравнению:
Na2S2O3 + H2SO4 = Na2SO4 + H2O + SO2 + S↓.
Образующаяся в реакции сера выделяется в виде мутного осадка. Время от начала реакции до появления первых следов помутнения при постоянной температуре зависит от концентрации реагирующих веществ.
Реактивы: 2 Н раствор серной кислоты, 1 Н раствор тиосульфата натрия, дистиллированная вода.
Посуда и принадлежности: микропробирки, пипетки, секундомер.
Методика проведения опыта. Для проведения опыта в четырех пробирках приготовьте равные объемы растворов тиосульфата натрия (Na2S2O3) различной концентрации. Для этого в каждую пробирку внесите пипеткой по каплям раствор тиосульфата натрия и воду в количествах, указанных в таблице 1.5.
Приняв относительную концентрацию раствора в первой пробирке (4 капли Na2S2O3 + 8 капель H2O) за единицу, заполните колонку 6 таблицы 1.5 соответствующими значениями относительной концентрации Na2S2O3 для остальных пробирок.
В пробирку № 1 внесите каплю раствора серной кислоты, одновременно включите секундомер и отметьте время, прошедшее от сливания растворов до появления помутнения. Аналогично поступайте и с другими пробирками, стараясь каждый раз зафиксировать время достижения одинаковой степени помутнения. Рассчитайте относительную практическую скорость реакции для каждого случая, зная исходную относительную концентрацию раствора тиосульфата натрия в каждом случае.
Таблица 1.5 – Зависимость скорости реакции от концентрации веществ
| Номер про-бирки | Количество капель | Общее число капель | Относи-тельная концент-рация (с) Na2S2О3 | Время появле-ния мути, τ | Относительная скорость
реакции
V =  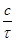 
| ||
| Na2S2O3 | H2O | H2SO4 | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| – |
Зависимость между концентрацией раствора тиосульфата натрия и скоростью реакции изобразите графически, откладывая на оси абсцисс концентрацию раствора, а на оси ординат – скорость реакции. Какой линией выражается найденная зависимость? Напишите выражение скорости проведенной реакции по расходу реагентов и ее скорости по накоплению продуктов, используя закон действующих масс.
Сделайте вывод о зависимости скорости реакции от концентрации тиосульфата натрия и объясните, почему эта зависимость существует.
Date: 2015-05-08; view: 967; Нарушение авторских прав