
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Адиабатические и изотермические процессы
|
|
Мы установили, как зависит давление газа от температуры, если объем остается неизменным. Теперь посмотрим, как меняется давление некоторой массы газа в зависимости от занимаемого ею объема, если температура остается неизменной. Однако, прежде чем перейти к этому вопросу, надо выяснить, как поддерживать температуру газа неизменной. Для этого надо изучить, что происходит, с температурой газа, если объем его меняется настолько быстро, что теплообмен газа с окружающими телами практически отсутствует.
Произведем такой опыт. В закрытую с одного конца толстостенную трубку из прозрачного материала поместим ватку, слегка смоченную эфиром, и этим создадим внутри трубки смесь паров эфира с воздухом, взрывающуюся при нагревании. Затем быстро вдвинем в трубку плотно входящий поршень. Мы увидим, что внутри трубки произойдет маленький взрыв. Это значит, что при сжатии смеси паров эфира с воздухом температура смеси резко повысилась. Это явление вполне понятно. Сжимая газ внешней силой, мы производим работу, в результате которой внутренняя энергия газа должна была увеличиться; это и произошло—газ нагрелся.
Теперь предоставим газу расширяться и производить при этом работу против сил внешнего давления. Это можно осуществить. Пусть в большой бутыли находится сжатый воздух, имеющий комнатную температуру. Сообщив бутыль с внешним воздухом, дадим воздуху в бутыли возможность расширяться, выходя из небольшого. отверстия наружу, и поместим в струе расширяющегося воздуха термометр или колбу с трубкой. Термометр покажет температуру, заметно более низкую, чем комнатная, а капля в трубке, присоединенной к колбе, побежит в сторону колбы, что также будет указывать на понижение температуры воздуха в струе. Значит, когда газ расширяется и при этом совершает работу, он охлаждается и внутренняя энергия его убывает. Ясно, что нагревание газа при сжатии и охлаждение при расширении являются выражением закона сохранения энергии.
Если мы обратимся к микромиру, то явления нагревания газа при сжатии и охлаждения при расширении станут вполне ясными. Когда молекула ударяется о неподвижную стенку и отскакивает от нее, скорость, а следовательно, и кинетическая энергия молекулы, в среднем такова же, как и до удара о стенку. Но если молекула ударяется и отскакивает от надвигающегося на нее поршня, ее скорость и кинетическая энергия больше, чем до удара о поршень (подобно тому как скорость теннисного мяча увеличивается, если его ударить во встречном направлении ракеткой). Надвигающийся поршень передает отражающейся от него молекуле дополнительную энергию. Поэтому внутренняя энергий газа при сжатии возрастает. При отскакивании от удаляющегося поршня скорость молекулы уменьшается, ибо молекула совершает работу, толкая отходящий поршень. Поэтому расширение газа, связанное с отодвиганием поршня или слоев окружающего газа, сопровождается совершением работы и приводит к уменьшению внутренней энергии газа.
Итак, сжатие газа внешней силой вызывает его нагревание, а расширение газа сопровождается его охлаждением. Это явление в некоторой мере имеет место всегда, но особенно резко заметаю тогда, когда обмен теплотой с окружающими телами сведен к минимуму, ибо такой обмен может в большей или меньшей степени компенсировать изменение температуры.
Процессы, при которых передача теплоты настолько ничтожна, что ею можно пренебречь, называют адиабатическими.
Возвратимся к вопросу, поставленному в начале главы. Как обеспечить постоянство температуры газа, несмотря на изменения его объема? Очевидно, для этого надо непрерывно передавать газу теплоту извне, если он расширяется, и непрерывно отбирать от него теплоту, передавая ее окружающим телам, если газ сжимается. В частности, температура газа остается достаточно постоянной, если расширение или сжатие газа производится очень медленно, а передача теплоты извне или вовне может происходить с достаточной быстротой. При медленном расширении теплота от окружающих тел передается газу и его температура снижается так мало, что этим снижением можно пренебречь. При медленном сжатии теплота, наоборот, передается от газа к окружающим телам, и вследствие этого температура его повышается лишь ничтожно мало.
Процессы, при которых температура поддерживается неизменной, называют изотермическими.
Закон Бойля — Мариотта
Перейдем теперь к более подробному изучению вопроса, как меняется давление некоторой массы газа, если температура его остается неизменной и меняется только объем газа. Мы уже выяснили, что такой изотермический процесс осуществляется при условии постоянства температуры тел, окружающих газ, и настолько медленного изменения объема газа, что температура газа в любой момент процесса не отличается от температуры окружающих тел.
Мы ставим, таким образом, вопрос: как связаны между собой объем и давление при изотермическом изменении состояния газа? Ежедневный опыт учит нас, что при уменьшении объема некоторой массы газа давление его увеличивается. В качестве примера можно указать повышение упругости при накачивании футбольного мяча, велосипедной или автомобильной шины. Возникает вопрос: какименно увеличивается давление газа при уменьшении объема, если температура газа остается неизменной?
Ответ на этот вопрос дали исследования, произведенные в XVII столетии английским физиком и химиком Робертом Бойлем (1627—1691) и французским физиком Эдемом Мариоттом (1620—1684).
Опыты, устанавливающие зависимость между объемом и давлением газа, можно воспроизвести: на вертикальной стойке, снабжённой делениями, находятся стеклянные трубки А и В, соединенные резиновой трубкой С. В трубки налита ртуть. Трубка В сверху открыта, на трубке А имеется кран. Закроем этот кран, заперев таким образом некоторую массу воздуха в трубке А. Пока мы не сдвигаем трубок, уровень ртути в обеих трубках одинаков. Это значит, что давление воздуха, запертого в трубке А, такое же, как и давление окружающего воздуха.
Будем теперь медленно поднимать трубку В. Мы увидим, что ртуть в обеих трубках будет подниматься, но не одинаково: в трубке В уровень ртути будет все время выше, чем в А. Если же опустить трубку В, то уровень ртути в обоих коленах понижается, но в трубке В понижение больше, чем в А.
Объем воздуха, запертого в трубке А, можно отсчитать по делениям трубки А. Давление этого воздуха будет отличаться от атмосферного на величину давления столба ртути, высота которого равна разности уровней ртути в трубках А и В. При. поднятии трубки В давление столба ртути прибавляется к атмосферному давлению. Объем воздуха в А при этом уменьшается. При опускании трубки В уровень ртути в ней оказывается ниже, чем в А, и давление столба ртути вычитается из атмосферного давления; объем воздуха в А соответственно увеличивается.
Сопоставляя полученные таким образом значения давления и объема воздуха, запертого в трубке А, убедимся, что при увеличении объема некоторой массы воздуха в определенное число раз давление его во столько же раз уменьшается, и наоборот. Температуру воздуха в трубке при наших опытах можно считать неизменной.
Подобные же опыты можно" произвести и с другими газами. Результаты получаются такие же.
Итак, давление некоторой массы газа при неизменной температуре обратно пропорционально объему газа (закон Бойля—Мариотта).
Для разреженных газов закон Бойля — Мариотта выполняется с высокой степенью точности. Для газов же сильно сжатых или охлажденных обнаруживаются заметные отступления от этого закона.
Формула, выражающая закон Бойля — Мариотта.
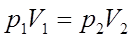 (2)
(2)
В физике и в технике часто пользуются графиками, показывающими зависимость давления газа от его объема. Начертим такой график для изотермического процесса. Будем по оси абсцисс откладывать объем газа, а по оси ординат—его давление (Рисунок 1)[11].

|

|
Рисунок 1-График, выражающий закон Бойля — Мариотта
Возьмем пример. Пусть давление данной массы газа при объеме 1 м3 равно 3,6 кГ/см2. На основании закона, Бойля — Мариотта рассчитаем, что при объеме, равном 2 м3, давление равно 3,6*0,5 кГ/см2= 1,8 кГ/см2. Продолжая такие расчеты,, получим следующую табличку:
Таблица 1- Расчеты на основании закона Бойля — Мариотта
| V(в м3) | ||||||
| P (в кГ1см2) | 3,6 | 1,8 | 1,2 | 0,9 | 0,72 | 0,6 |
Нанося эти данные на чертеж в виде точек, абсциссами которых являются значения V, а ординатами — соответствующие значения Р, получим кривую линию— график изотермического процесса в газе (Рисунок 1).
Зависимость между плотностью газа и его давлением
Вспомним, что плотностью вещества называется масса, заключенная в единице объема. Если мы как-нибудь изменим объем данной массы газа, то изменится и плотность газа. Если, например, мы уменьшим объем газа в пять раз, то плотность газа увеличится в пять раз. При этом увеличится и давление газа; если температура не изменилась, то, как показывает закон Бойля — Мариотта, давление увеличится тоже в пять раз. Из этого примера видно, что при изотермическом процессе давление газа изменяется прямо пропорционально его плотности.
Обозначив плотности газа при давлениях  и
и  буквами
буквами  и
и  , можем написать:
, можем написать:
 (3)
(3)
Этот важный результат можно считать другим и более существенным выражением закона Бойля — Мариотта. Дело в том, что вместо объема газа, который зависит от случайного обстоятельства — оттого, какая выбрана масса газа,— в формулу (3) входит плотность газа, которая, также как и давление, характеризует состояние газа и вовсе не зависит от случайного выбора его массы[12].
Date: 2015-11-13; view: 628; Нарушение авторских прав