
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Основы химической термодинамики
|
|
(№ 43 – 71)
43. Не производя расчетов, определите и объясните знак изменения энтропии в реакциях:
2NH3(г) = N2(г) + 3H2(г),
СН4(г) + 2О2(г) = СО2(г) + 2Н2О(ж).
44. Не производя расчетов, определите и объясните знак изменения энтропии в реакции:
2Mg(к) + О2(г) = 2MgO(к).
Ответ подтвердите расчетом.
45. Не производя расчетов, определите знак изменения энтропии реакции, протекающей в нейтрализаторах автомобилей:
CO(г) +½ O2(г) 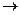 CO2 (г).
CO2 (г).
46. В каких из приведенных ниже реакциях происходит уменьшение энтропии:
а) K2CO3(тв) + H2SO4(ж)= K2SO4 (ж) +CO2(г) 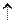 +H2O(ж);
+H2O(ж);
б) 2SO2(г) + O2(г) = SO3(г);
в) 2H2S(г) +O2(г) = 2H2O(ж) + 2S(к).
47. Вычислите стандартное изменение энтропии реакций:
а) 4NH3(г) + 5O2(г) = 4NO(г) + 6H2O(ж);
б) 4NH3(г) + 3O2(г) = 2N2(г) + 6H2O(ж).
48. Укажите, в каком направлении в стандартных условиях может протекать реакция:
4HCl(г) + О2(г) = 2Сl2(г) + 2Н2О(ж).
Ответ подтвердите расчетом.
49. Укажите, в каком направлении в стандартных условиях может протекать реакция:
CO(г) + H2O(г) «CO2(г) + H2(г).
Ответ подтвердите расчетом (зависимостью энтальпии и энтропии реакции от температуры можно пренебречь).
50. Рассчитайте константу равновесия (Кр) реакции
СO2(г) + H2(г) ↔ СО(г) + H2O(г)при T=500 K.
51. Укажите, в каком направлении может протекать реакция HCl(г) + NH3(г) =NH4Cl(к) при Т=400 оС? Ответ подтвердите расчетом (зависимостью энтальпии и энтропии реакции от температуры можно пренебречь).
52. Определите количество теплоты, выделяющейся при сгорании 5,6 л водорода (объем измерен при нормальных условиях) с образованием H2O(ж).
53. Рассчитайте, сколько молей этилового спирта С2Н5ОН необходимо сжечь по реакции:
С2Н5ОН(г) + 3О2(г) = 2СО2(г) + 3Н2О(г),
чтобы получить 2556 кДж теплоты.
54. Рассчитайте, сколько теплоты выделится при полном сгорании 8 г метана (СН4, газ) с образованием СО2(г)и Н2О(г).
55. Рассчитайте количество теплоты, выделяющееся при полном сгорании 1 кг этилена (С2Н4), взятого в газообразном состоянии, если в результате реакции образуется углекислый газ и Н2О(г).
56. При полном сгорании этилена (С2Н4, газ) по реакции:
С2Н4(г) + 3О2(г) = 2СО2(г) + 2Н2О(ж)
выделилось 4358,2 кДж теплоты. Рассчитайте объем вступившего в реакцию кислорода, измеренный при нормальных условиях.
57. Для плавления 1,8 г льда потребовалось 567 Дж теплоты. Рассчитайте молярную теплоту плавления льда (∆Н о, кДж/моль).
58. Рассчитайте, какое количество теплоты выделится при сгорании 10 г цинка при стандартных условиях, если стандартная энтальпия образования оксида цинка ZnO ∆Н о298=−350,6 кДж/моль.
59. Рассчитайте, сколько теплоты выделится при полном сгорании 1 м3 пентана (С5Н12), взятого в газообразном состоянии при н.у., если в результате реакции образуется углекислый газ и Н2О(г).
60. Рассчитайте, какое количество теплоты выделится при сжигании 5 г магния в стандартных условиях, если стандартная энтальпия образования оксида магния ∆Н о298MgO(тв)=−601,8 кДж/моль?
61. Рассчитайте, какое количество теплоты выделится при получении 2 моль этанола, согласно термохимическому уравнению
C2 H4(г) + H2O(ж) = C2 H 5OH (ж).
62. Рассчитайте количество теплоты, выделяемое при полном
сгорании 1 м3 метана (СН4), взятого в газообразном состоянии, если в результате реакции образуется углекислый газ СО2(г) и Н2О(г).
63. Рассчитайте количество теплоты, выделяемое при сгорании 16 г серы, если энтальпия образования оксида серы (IV) равна –296,9 кДж/моль.
64. Рассчитайте количество теплоты, выделяющееся при полном сгорании 100 л н-гептана (С7Н16), взятого в газообразном состоянии при н.у., если в результате реакции образуется СО2(г) и Н2О(г).
65. Какое количество теплоты выделится при окислении 150 г глюкозы кислородом до углекислого газа и Н2О(ж).
66. Сколько теплоты выделится при сгорании газовой смеси 5,6 л кислорода и 11,5 л водорода при р =101,3 кПа и Т =298,15 К?
67. При какой температуре в стандартном состоянии установится равновесие реакции:
N2(г) + 3H2(г)  2NH3(г).
2NH3(г).
68. При какой температуре в стандартном состоянии установится равновесие реакции:
2CO(г)  C(графит) + СО2(г).
C(графит) + СО2(г).
69. Вычислите температуру, при которой в стандартном состоянии установится равновесии реакции:
2 NO2(г)  N2O4(г),
N2O4(г),
если известны: ∆Н ореакции=−55,3 кДж; ∆S ореакции=−175,8 Дж/К.
70. Рассчитайте стандартное изменение энергии Гиббса реакции сгорания изо -октана
изо -С8Н18(г) + 12,5О2(г) = 8СО2(г) + 9Н2О(ж)
двумя способами – по табличным значения ∆G o298и по значениям ∆Н о298и S о298.
71. Рассчитайте, сколько теплоты выделится при полном сгорании 16 г метана (СН4, газ) с образованием СО2(г)и Н2О(г).
Date: 2015-10-19; view: 1050; Нарушение авторских прав