
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Концентрации
|
|
Необходимым условием того, чтобы между частицами (молекулами, ионами) исходных веществ произошло химическое взаимодействие, является их столкновение друг с другом (соударение). Точнее говоря, частицы должны сблизиться друг; с другом настолько, чтобы атомы одной из них испытывали бы действие электрических полей, создаваемых атомами другой. Только при этом станут возможны те переходы электронов и перегруппировки атомов, в результате которых образуются молекулы новых веществ — продуктов реакции. Поэтому 'скорость реакции пропорциональна числу соударений, которые претерпевают молекулы реагирующих веществ.
Число соударений, в свою очередь, тем больше, чем выше концентрация каждого из исходных веществ или, что то же самое, чем больше произведение концентраций реагирующих веществ
Рассмотрим зависимость скорости 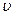 от концентрации. Предположим, имеем реакцию А+В+2D=F+L. Надо найти зависимость скорости от концентрации реагентов
от концентрации. Предположим, имеем реакцию А+В+2D=F+L. Надо найти зависимость скорости от концентрации реагентов
u = f(CA, CB, CD) =?
Измерим скорость при каких либо концентрациях, а потом увеличим СА вдвое и еще раз измерим скорость. Пусть она возросла вдвое. Это значит, что скорость 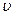 пропорциональна концентрации СА в первой степени. Увеличим СВ вдвое. Предположим, что это не повлияло на скорость – вполне реальная ситуация. Если растворять NO2 в воде для получения азотной кислоты, то очевидно, что скорость реакции не будет зависеть от количества воды. В таком случае можно сказать, что скорость реакции
пропорциональна концентрации СА в первой степени. Увеличим СВ вдвое. Предположим, что это не повлияло на скорость – вполне реальная ситуация. Если растворять NO2 в воде для получения азотной кислоты, то очевидно, что скорость реакции не будет зависеть от количества воды. В таком случае можно сказать, что скорость реакции 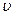 зависит от СВ в нулевой степени. Пусть теперь мы обнаружили, что от СD скорость зависит как СD 2. Тогда общее уравнение скорости реакции запишется как
зависит от СВ в нулевой степени. Пусть теперь мы обнаружили, что от СD скорость зависит как СD 2. Тогда общее уравнение скорости реакции запишется как
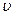 = kCACB 0 CD 2 (1.3)
= kCACB 0 CD 2 (1.3)
где k — коэффициент пропорциональности, называемый константой скорости данной реакции
Это уравнение называется кинетическим уравнением реакции. Величина константы скорости k зависит от природы реагирующих веществ, от температуры и от присутствия катализаторов, но не зависит от концентраций веществ.
Показатели степеней при концентрациях в кинетическом уравнении называется порядками реакции по данному веществу, а их сумма – общим порядком реакции. Порядки реакции устанавливаются экспериментально, а не по стехиометрическим коэффициентам. Существует совсем немного реакций, где порядок совпадает с суммой стехиометрических коэффициентов.
N2O5= 2NO2+ 1/2O2 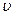 = kC(N2O5) реакция 1 порядка
= kC(N2O5) реакция 1 порядка
(H2)+(J2) = 2(HJ) 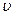 = kC(H2)C(J2) реакция 2 порядка
= kC(H2)C(J2) реакция 2 порядка
(Cl2) +2(NO) = 2(NOCl) 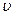 = kC(Cl2)C(NO)2 реакция 3 порядка
= kC(Cl2)C(NO)2 реакция 3 порядка
Наиболее часто встречаются реакции первого, второго, иногда‑третьего порядка.
H2 + Br2 = 2HBr
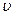 = kCH2CBr2 1/2
= kCH2CBr2 1/2
Иными словами, порядок может быть и дробным. Почему, рассмотрим ниже.
Реакции обычно идут по стадиям, поскольку невозможно представить себе одновременное столкновение большого числа молекул.
Предположим, что некая реакция идет по стадиям:
A + 2B = C + D
1) А + В = АВ
2) АВ + В --> C +D
Тогда, если первая реакция идет медленно, а вторая быстро, то скорость определяется первой стадией (пока она не пройдет, не может идти вторая), т.е. накопление частиц АВ. Тогда и 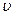 = kCACB.
= kCACB.
Скорость реакции для последовательных реакций определяется самой медленной стадией. Отсюда различие между порядком реакции и стехиометрическими коэффициентами. Например, реакция разложения перекиси водорода
2H2O2 = 2H2O+O2
На самом деле реакция первого порядка, т.к. она лимитируется первой стадией H2O2 = H2O+O, а вторая стадия O+O = O2 идет очень быстро.
Может быть самой медленной не первая, а вторая или другая стадия и тогда мы получаем иногда дробный порядок, выражая концентрации интермедиатов (промежуточных соединений) через концентрации начальных веществ.
Скорость реакции в момент t - мгновенная скорость - подчиняется закону действующих масс, который был экспериментально открыт и теоретически обоснован в середине ХIX столетия и получил свое название от термина «действующая масса» - синонима современного понятия «концентрация».
Закон действующих масс (К. Гульдберг, П.Вааге, 1867г. Норвегия):
скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.
aA + bB +... ®...
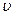 = k • [A]a • [B]b •... (1.4)
= k • [A]a • [B]b •... (1.4)
Константа скорости реакции k зависит от природы реагирующих веществ, температуры и катализатора, но не зависит от значения концентраций реагентов.
Физический смысл константы скорости заключается в том, что она равна скорости реакции при единичных концентрациях реагирующих веществ.
Скорость реакции первого порядка:
Рассмотрим химическую реакцию первого порядка – это обычно реакции разложения или диссоциации.
H2 à 2H
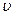 =k*C
=k*C



принимая для времени t=0 C = C0, получим
 (1.5)
(1.5)
тогда

 . (1.6)
. (1.6)
Концентрация реагентов и скорость реакции первого порядка уменьшаются во времени по экспоненциальному закону.
Прологарифмируем уравнение (1.4), получим

 , тогда
, тогда
 (1.7)
(1.7)
Константа скорости реакции первого порядка измеряется [с-1]

Рисунок 2 – Изменение концентрации реагирующих веществ
для реакций первого порядка
 |
(1.8)
Период полураспада (t ½)-время, в течение которого концетрация реагента уменьшается вдвое по сравнению с начальной концетрацией.
Подставим С=С0/2 подставим в (1.6), тогда получим
 . (1.9)
. (1.9)
Период полураспада реагента в случае реакции первого порядка не зависит от начальной концетрации, а определяется константой скорости реакции.
Скорость реакции 2-го порядка.
Например, рассмотрим реакцию второго порядка:
2HJ = H2+J2
 ,
, 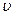 = kС2
= kС2
Используя уравнения для скоростей реакций и разделяя переменные, получим

Принимая в начальный момент
C = C0
получим
 . (1.10)
. (1.10)
 . k, [л/моль*с] (1.11)
. k, [л/моль*с] (1.11)
 . (1.12)
. (1.12)
 . (1.13)
. (1.13)
 |
Рисунок 3 - Изменение концентраций исходных веществ во
времени для уравнений реакций второго порядка.
Date: 2015-10-19; view: 422; Нарушение авторских прав