
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Стандартная энергия Гиббса образования
|
|
некоторых веществ при 298К (25ºС)
| Вещество | 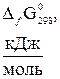
| Вещество | 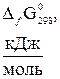
| Вещество | 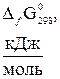
|
| Al2O3(к) | –1582 | FeO(к) | –239,3 | NH4Cl(к) | –203,2 |
| BeCO3(к) | –944,8 | Fe2O2(к) | –740,3 | NO(г) | –86,6 |
| BeO(к) | –581,6 | Fe3O4(к) | –1017 | NO2(г) | –51,5 |
| CH4(г) | –50,8 | HF(г) | –272,8 | NiO(к) | –216,4 |
| C2H2(г) | +208,4 | HCl(г) | –94,8 | PbO(к) | –188,2 |
| С2H4(г) | +68,2 | HBr(г) | –51,2 | PbO2(к) | –217,6 |
| СО(г) | –137,1 | Hl(г) | +1,8 | SO2(г) | –300,2 |
| СО2(г) | –394,4 | H2O(г) | –228,6 | SO3(г) | –371,2 |
| СаСО3(к) | –599,4 | H2O(ж) | –237,2 | SnO(к) | –257,3 |
| CaCO3(к) | –1129 | MgO(к) | –569,6 | SnO2(к) | –519,7 |
| CuO(к) | –129,7 | NH3(г) | –16,7 | ZnO(к) | –319,0 |
Константы нестойкости комплексных ионов
| Уравнение диссоциации | Кн |
[Ag(CN)2]–  Ag+ + 2CN– Ag+ + 2CN–
| 2,0·10-22 |
[Ag(NH3)2]+  Ag+ + 2NH3 Ag+ + 2NH3
| 5,9·10-8 |
[Cd(CN)4]2–  Cd2+ + 4CN– Cd2+ + 4CN–
| 7,7·10-18 |
[CdI4]2+  Cd2+ + 4I– Cd2+ + 4I–
| 7,9·10-7 |
[Cd(NH3)4]2+  Cd2+ + 4NH3 Cd2+ + 4NH3
| 2,8·10-7 |
[Cu(NH3)4]2+  Cu2+ + 4NH3 Cu2+ + 4NH3
| 9,3·10-13 |
[Hg(CN)4]2–  Hg2+ 4CN– Hg2+ 4CN–
| 3,0·10-42 |
[HgI4]2–  Hg2+ + 4I– Hg2+ + 4I–
| 1,4·10-30 |
[Zn(CN)4]2–  Zn2+ + 4CN– Zn2+ + 4CN–
| 1,0·10-16 |
[Zn(NH3)4]2+  Zn2+ + 4NH3 Zn2+ + 4NH3
| 2,0·10-9 |
Константы диссоциации слабых кислот
| Кислота | K1 | K2 |
| H2C2O4 | 5,6·10-2 | 5,1·10-5 |
| H2SO3 | 1,7·10-2 | 6,3·10-8 |
| HF | 6,6·10-4 | — |
| H2CO3 | 4,5·10-7 | 4,8∙10-11 |
| H2S | 1,1·10-7 | 1,0∙10-14 |
| HCN | 7,9·1010 | — |
Величины стандартных электродных потенциалов
| Электрод | Потенциал
 , В , В
| Электрод | Потенциал
 , В , В
| Электрод | Потенциал
 , В , В
|
| Li+ / Li | –3,02 | Zn2+ / Zn | –0,76 | Bi3+ / Bi | +0,22 |
| K+ /K | –2,92 | Cr3+ / Cr | –0,74 | Cu2+ / Cu | +0,34 |
| Ca2+ / Ca | –2,87 | Fe2+ / Fe | –0,44 | Hg22+/2Hg | +0,79 |
| Na+ /Na | –2,71 | Cd2+ / Cd | –0,40 | Ag+ / Ag | +0,80 |
| Mg2+ /Mg | –2,36 | Co2+ / Co | –0,28 | Hg2+ / Hg | +0,85 |
| Be2+ /Be | –1,85 | Ni2+ / Ni | –0,25 | Pt2+ / Pt | +1,19 |
| Al3+ /Al | –1,66 | Sn2+ / Sn | –0,14 | Au3+ / Au | +1,50 |
| Ti2+ /Ti | –1,63 | Pb2+ / Pb | –0,13 | ||
| Mn2+ /Mn | –1,18 | 2H+ / H2 |
Date: 2015-09-24; view: 920; Нарушение авторских прав