
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Применение!
|
|
3. Процесс окисления проводили на серебряном катализаторе, нанесенного на пемзу, при температуре 250-500 °С. Побочными продуктами данного процесса могут выступать: уксусная кислота, углекислый газ (СО2), угарный газ, этан. Процесс окисления проводят в кварцевом реакторе с полкой для катализатора. Установка для проведения процесса показана на рис.
1- баллон с азотом; 2 - печь (испаритель); 3 - реактор; 4 - холодильник кварцевый; 5 – прямой холодильник; 6, 7 - приемники; 8, 9 - абсорберы
Рис. – Установка получения ацетальдегида окислением этилового спирта
Исходное сырье (этанол) заливается в емкость с капельной воронкой и боковым отводом, предназначенным для создания одинакового давления в емкости и системе. В крышке емкости имеется отверстие для подачи азота из баллона. Это необходимо для того, чтобы создавалось дополнительное давление на реакционное сырье. Данное сырье по каплям проходит по аллонжу, соединенного с капилляром, который имеет два отвода. В верхний отвод подается исходное реакционное сырье, в нижний – азот на реакцию окисления. В данном случае, азот в систему подается из баллона 1 через расходомер, регулируемый зажимом. После смешения реакционная масса направляется в испаритель 2,температура которого 220 °С.
Испаритель изготовлен из кварцевого стекла. Он состоит из двух частей: внутренней трубки для испарения сырья и внешней рубашки, предназначенной для подвода тепла. В средней части испарителя расположена обмотка, соединенная с латером для подачи и регулирования тепла. В зазоре между трубкой и рубашкой испарителя помещается термопара, соединенная с прибором, который показывает устанавливаемую температуру. Для устранения тепловых потерь испаритель обматывают асбестовой нитью и стеклотканью.
Пары исходного сырья в потоке азота поступают из испарителя в нижнюю часть реактора окисления 3, где имеется нижний боковой отвод для подачи кислорода. Воздух поступает в нижнюю часть реактора через пузырьковой расходомер из компрессора. Расход воздуха регулируется зажимом.
Реактор 3 изготовлен из кварца, так как в реакционной зоне может развиться высокая температура. Он состоит из двух зон: нижней, предназначенной для смешения и подогрева реакционной массы с кислородом воздуха, и верхней, где проходит реакция окисления, и располагается слой катализатора и насадки. Внутри реактора зоны разделены решеткой. В качестве катализатора используется серебро, нанесенное на пемзу, а в качестве насадки – измельченное кварцевое стекло. На решетку
загружается слой: насадка – катализатор – насадка. В верхней части реактора расположены две обмотки. Внизу реактора находится отверстие для введения термопар. В данном случае используется две термопары. Одна из них измеряет температуру верха реактора, а вторая – низа реактора. Как и в случае испарителя, реактор обматывают асбестовой нитью и стеклотканью для устранения тепловых потерь.
Реактор соединяется с холодильником 4 через угловой переходник, который изготавливается из кварца ввиду высокой температуры выходящих паров. Переходник обматывается асбестовой нитью и стеклотканью.
Материалом для прямого холодильника является кварцевое стекло. Внутренняя трубка холодильника загружается насадкой. Используется насадка из стекла цилиндрической формы. Холодильник необходим для конденсации паров образующихся продуктов. Сконденсировавшиеся пары стекают в приемник 6. После холодильника 4 расположен прямой холодильник 5 для конденсации паров образующихся продуктов. Сконденсировавшиеся пары также стекают в приемник 7. Приемники, в свою очередь, охладим, погрузив их в охлаждающую смесь из равных количеств измельченного льда или снега. Несмотря на все эти меры предосторожности, пары этаналя все же частично улетучиваются. Так как этаналь имеет неприятный резкий запах и ядовит, опыт нужно проводить в вытяжном шкафу или на открытом воздухе.
Далее уносимые пары поступают в абсорберы 8 и 9 последовательно. В первый абсорбер 8 заливается 100 мл воды, а во второй абсорбер 9 заливается 50 мл воды и щелочи (NaOH) для лучшего улавливания газообразных продуктов. В течение процесса абсорберы, также как и приемники охлаждают льдом для уменьшения потерь.
В данной работе воздух и азот подается в систему через пузырьковые расходомеры. Их используют для измерения объемного расхода невзрывоопасного газа, не содержащего пары и механические частицы, для калибровки (градуировки) и поверки пробоотборных устройств (аспираторов), а также для регулировки (настройки) расхода газов и газовых смесей перед подачей в приборы.
4. Окисление – это наиболее распространенный метод получения кисло- родсодержащих соединений из углеводородного сырья. В этом процессе совмещены экзотермическая реакция окисления этанола:
С2Н5ОН + 0,5О2 = С2Н4О + Н2О + Q1
и эндотермическая реакция его дегидрирования:
С2Н5ОН = С2Н4О + Н2 - Q2 Одновременно с основными реакциями протекают побочные реакции глубокого окисления, а также реакция гидрирования, приводящие к образованию смеси продуктов:
С2Н5ОН + Н2 = С2Н4 + Н2О
Процесс окислительного дегидрирования проводится при температуре 500—600 °С и времени контактирования около 0,02 с. В этих условиях выход ацетальдегида в расчете на пропущенное сырье составляет 80—85 % при степени контактирования 0,85—0,90 с.
Также в системе протекает целый ряд побочных превращений:
С2Н5ОН + 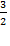 О2 → СО2 + 2Н2О
О2 → СО2 + 2Н2О
С2Н4О + 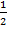 О2 → СН3–СООН
О2 → СН3–СООН
СН3–СООН + 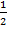 О2 → СО2 + Н2О
О2 → СО2 + Н2О
СН3–СООН → СО + 2Н2О
С2Н4О → СО +Н2
2С2Н4О + Н2О → С2Н5ОН + СН3–СООН
Н2 + 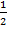 О2 → Н2О
О2 → Н2О
2С2Н5ОН + С2Н4О → СН2(ОС2Н5)2 + Н2О
СО + 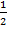 О2 → СО2
О2 → СО2
2СО → СО2 + С
Для анализа хода процесса и определения его эффективности существуют технико-экономические показатели процесса.
Конверсия сырья показвает долю сырья от поданного прерватившегося в данном ХТП, численно измеряется от 0 до 1, или в %. Чем больше степень превращения, тем большая часть исходного сырья вступила в реакцию, тем полнее прошел процесс. На нее оказывает влияние такие показатели, как температура, давление, соотношение реагентов и и их концентраций, время пребывания.
Селективность процесса характеризует долю сырья от превращенного, пошедшего на целевую реакцию. На нее оказывают влияние температура, давление, состав сырья, концентрация исходных веществ, катализатор. В большинстве случаев при повышении температуры конверсия растет, а селективность падает.
Хроматографический метод повзоляет определить концентрацию веществ в анализируемой смеси, на основании этого мы определим конверсиюв смеси продуктов окисления этанола, а селективность через выход целевого продукта.
5. Моделирование и расчёт технологической схемы окислительной конверсии этилового спирта в ацетальдегид производился с помощью программы HYSYS. Моделирование в программе HYSYS провели при различных соотношениях кислорода к этанолу. Из графика видим зависимость конверсии и селективности процесса от соотношения кислорода:этанолу при температуре 300 °С.
Наиболее оптимальным соотношением является 1:0,45. Для него характерны максимальная степень коверсии этанола 50,15 %. Максимальная селективность 63,71 % характерна для соотношения 1:015 моль. Также не менее важным является выход продукта. Так выход ацетальдегида в жидком состоянии увеличичвается с увеличением мольного соотношения кислорода и максимальное его значение составляет 0,2703 мольных долей.
6. Как видно из графиков, конверсия возрастает при увеличении температуры и при увеличении мольного соотношения подаваемого кислорода. Макисмальная конверсия наблюдается при использовании катализатора чистого серебра – 53,16 %, для которой селективность составляет 47,20 %.
7. Как видим из графиков при увеличении температуры селективность плавно снижается с 68,56 до 47, 20 % для чистого серебра. А при увеличении мольного соотношения подаваемого кислорода селективность возрастает до 0,25 моль, а затем убывает.
8. Максимальный выход ацетальдегида наблюдается при температуре 300 °С – 28,88 %, а при 400°С наблюдаем минимальный выход ацетальдегида – 22,33 % (на сферическом).
9. Также провели опыты с медным катализатором. Как видно из рис. значения выхода ацетальдегида с кислородом значительно выше, чем при окислении этанола на меди без кислорода. С 30 минуты происходит плавное снижение выхода ацетальдегида (α = 8,53 °С). Выгружаемая после реакции медь находилась в коагулированном состоянии, трудно подвергающемся разрушению. Но видимых склеивающихся веществ не обнаружили и она быстро к тому же разрушалась. Возможно характерен процесс дезактивации катализатора. Таким образом можно сделать вывод о том, что медь очень быстро дезактивируется засчет отложения кокса на его поверхности.
10. В данной дипломной работе была создана лабораторная установка процесса синтеза ацетальдегида. В основу получения синтеза ацетальдегида положен процесс окисления этанола на серебряном катализаторе. Изучение процесса окисления этанола в уксусный альдегид кислородом воздуха на серебряном катализаторе в кварцевом реакторе позволило определить оптимальные параметры процесса.
Были проведены опыты по окислению этанола кислородом воздуха при нескольких различных температурах и мольных соотношениях подаваемого кислорода с целью определения влияния этих параметров процесса на конверсию, селективность и выход целевого продукта. При этом, в первом случае должно быть постоянным мольное соотношение кислорода к этанолу, а во втором – температура. Провели реакции при пяти температурах от 250 до 450 ºС с шагом в 50 ºС при соотношении О2:С2Н5ОН = 0,35:1 и при мольных соотношениях О2:С2Н5ОН = (0,15; 0,25; 0,35; 0,45):1 с температурой 300 ºС.
Таким образом, проведя опыты установили, что самая оптимальная температура процесса 400 °С и мольное соотношение О2:С2Н5ОН = 0,45:1. Также использование чистого серебра дает немного выше значения конверсии, селективности процесса и выхода ацетальдегида. Это объясняется тем, что чистое серебро на сферическом серебре обладает лучшими способностями к окислительному дегидрированию этанола.
Была изучена кинетика процесса синтеза ацетальдегида с использованием медного катализатора, и установлено, что медь очень быстро дезактивируется засчет отложения кокса на его поверхности.
Date: 2015-09-05; view: 350; Нарушение авторских прав