
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Алкогольное поражение сердечно-сосудистой системы
|
|
Действие однократного введения алкоголя в средней дозе, если ему не предшествует хроническая алкогольная интоксикация, уже в течение первого часа проявляется прежде всего снижением нагрузки на левый желудочек, что связано с уменьшением периферического сопротивления. Одновременно идет небольшое снижение сократимости, происходит нарастание дефицита энергообеспечения сократительного акта. При этом ни продолжительность сердечного цикла, ни диастолы не меняются. Острое воздействие ацетальдегида в тех же условиях оказывает совершенно иной эффект. Вследствие высвобождения норадреналина снижение периферического сопротивления происходит более выражено. Если продолжать систематическое употребление алкоголя, то его токсическое воздействие на сердце ведет к прогрессивному нарастанию дистрофических изменений мышечных клеток, вплоть до появления в них микро- и даже макронекрозов. Уже в самом начале систематического приема алкоголя в сердце обнаруживаются изменения, которые, с одной стороны, должны препятствовать проникновению этанола в ткани, а с другой - одновременно затруднять снабжение сердца кислородом. Речь идет об образовании вокруг капилляров аморфных масс. В местах их отложения отмечается выраженная деструкция миокардиальной ткани и со временем увеличение количества лизосом с разрыхленной или с разрушенной мембраной, вследствие чего развивается гипоксия. В поздние сроки заболевания изменения стенок капилляров становятся более выраженными. Вместе со значительным утолщением стенок мелких артерий и разрастанием в них и вокруг соединительной ткани происходит расширение сосудов и замедление тока крови, что приводит к застою и отеку. В дальнейшем отек переходит в склероз.
Алкогольное поражение системы иммунной защиты организма
При хроническом употреблении алкоголя наряду с другими страдает и иммунная система. Фагоцитоз относится к числу важнейших защитных антиинфекционных механизмов организма. С его помощью в организме разрушаются и удаляются частицы размером менее 3мк, к которым относятся и микробы. При систематическом злоупотреблении спиртными напитками спустя довольно длительный срок наблюдается заметное снижение фагоцитоза, мобилизация фагоцитов остается сниженной. Лизоцим - белок, содержащийся во многих секретах человека: в слюне, слезах, тканях различных внутренних органов, скелетных мышцах и т. д. В условиях хронической интоксикации организма алкоголем уровень лизоцима понижается. Также наблюдается недостаток лимфоцитов. Следующей причиной лежащей в основе иммунных нарушений лежит снижение барьерной функции печени. Таким образом, систематическое употребление алкоголя ведет к снижению защиты организма.
Алкогольное поражение органов дыхания
Изменения в системе дыхания связаны с двумя основными моментами. Первое — это способность легких выделять в неизмененном виде как сам этанол, так и его метаболит—ацетальдегид. Второе — это повышенная вероятность аспирации различных количеств пищи. Этанол и ацетальдегид, выделяясь в альвеолы, оказывают на клетки легочной ткани токсическое действие. В пораженной ткани наблюдаются гибель отдельных клеток. Повреждающее действие этанол и его метаболиты оказывают не только на альвеолу, но и на стенки воздухоносных путей - бронхи и трахею. Указанные изменения проявляются в нарушении функции дыхания, которое составляют снижение жизненной емкости и максимальной вентиляции легких, уменьшение длительности задержки дыхания на вдохе и выдохе. При этом у лиц, злоупотребляющих алкоголем, почти всегда присутствуют воспаления бронхов и трахеи. Указанные изменения становятся благоприятным фоном для развития инфекционных воспалительных процессов. Нарушение перистальтики пищевода, акта глотания и возникновение рвоты приводят к аспирации пищи, которая является источником инфекции во многих случаях возникновения пневмоний у злоупотребляющих алкоголем.
Нарушение иммунной защиты приводит к тому, что острая пневмония часто приобретает затяжное течение. Кроме того, для нее характерно развитие таких осложнений, как плеврит. Тяжелое течение, свойственное этим пневмониям, нередко приводит к летальному исходу.
Алкогольное поражение выделительной системы
При приеме необычно больших доз алкоголя, когда речь идет об алкогольном отравлении, последствия более серьезные—может развиться некронефроз. Эта форма заболевания бывает связана только с алкогольным эксцессом. Поражаются канальцы почек, клубочковый аппарат не изменяется. В эпителии канальцев происходят дистрофические изменения вплоть до развития некрозов, слущивание клеток эпителия в просвет канальцев.
Алкогольная болезнь может сопровождаться инфекцией мочевых путей и развитием пиелонефрита. Это поражение развивается в связи со снижением функции иммунной защиты под воздействием алкоголя.
Алкогольное поражение системы крови
Об изменении лейкоцитов было сказано в связи с алкогольным поражением иммунной системы. Другие клеточные элементы крови также меняются при хроническом употреблении алкоголя. При алкогольном макроцитозе макроциты составляют большинство эритроцитов. При этом в мембранах таких эритроцитов обнаруживается повышенное содержание холестерина. Частота встречаемости этого феномена при злоупотреблении алкоголем составляет более 80%. Это явление и медленная (в течение 2—4 мес.) нормализация размеров эритроцитов после прекращения приема алкоголя позволяют отнести макроцитоз эритроцитов к маркерам алкогольной болезни.
Следующий ряд изменений эритроцитов наступает в связи с развитием алкогольного поражения печени. Извращение синтеза липидов в ней приводит к нарушению липидного состава плазмы крови, что, в свою очередь, вызывает повышенное отложение холестерола и фосфолипидов на мембране эритроцитов. Вместе с тем трансформация формы эритроцитов ухудшает их фильтруемость, что способствует более быстрому их разрушению и развитию анемии. Изменения липидного состава могут происходить и в мембранах тромбоцитов. Следствием является разрушение части их, а также ухудшение их адгезивной способности. Поэтому капиллярные кровотечения и кровоподтеки нередко являются внешними проявлениями систематического употребления алкоголя.
Алкогольное поражение нервной системы
Алкогольная болезнь может проявляться множеством неврологических симптомов, в основе которых лежат описанные метаболические нарушения мозга, ведущие помимо прочего к дистрофии и некрозу нервных клеток: повышенная секреция жидкости под воздействием алкоголя сосудистыми сплетениями желудочков мозга и в результате увеличение внутричерепного давления.
Абстинентный синдром. Разрегулирующее действие алкоголя проявляется в том, что в организме накапливается избыток норадреналина и дофамина. Другим проявлением нарушения метаболизма является задержка продукции тормозного медиатора — γ -аминомасляной кислоты (ГАМК), снижение уровня ацетилхолина и нарушения других важных медиаторов. Выход из состояния опьянения в условиях очень большого дефицита ГАМК с потерей в это время компенсирующего действия самого этанола ведет к развитию возбуждения многих структур, что проявляется тяжелой вегетативной дисфункцией, а в более тяжелых случаях — бессонницей, галлюцинациями, судорогами.
Синдром лобной атрофии. Атрофический процесс захватывает всю кору головного мозга. Постепенно уменьшается количество нервных клеток. Лобная кора наиболее ранима. Развитию атрофических процессов способствует повышение внутричерепного давления. Атрофия клеток лобных долей проявляется «лобным синдромом» — алкогольной деградацией личности.
Синдром мозжечковой деградации. Атрофические процессы развиваются и в мозжечке. В нем тоже есть область, в которой в наибольшей степени прогрессирует процесс дегенерации и гибели нервных клеток. Это червь и прилегающие части полушарий мозжечка. Вследствие такой топографии поражения мозжечка развивается неустойчивая походка с широко расставленными ногами, часты падения, атаксия.
Миопатический синдром. Дистрофические процессы в мышцах после приема чрезмерных доз алкоголя могут приводить к развитию острых некрозов. При хронической алкогольной интоксикации дистрофические изменения в мышцах нарастают постепенно. С ними связано развитие болей, отеков, а затем и атрофии. Главным образом страдают мышцы плечевого пояса, туловища и таза, иногда дистальных областей конечностей.
Сочетание перечисленных синдромов, различающихся выраженностью составляющих их симптомов, создает на практике огромное разнообразие проявлений алкогольного поражения центральной нервной системы.
Алкогольное поражение других органов изучено еще недостаточно. Проявления их нарушений находят объяснение или в связи с универсальными изменениями метаболизма всего организма, возникающими под воздействием обмена этанола, или в связи с поражением других органов. Сведения о более тонких механизмах, охватывающих особенности проявления влияния алкоголя на процессы, связанные со специфической функцией этих органов, в настоящее время весьма отрывочны.

 Алкогольная болезнь печени
Алкогольная болезнь печени
Эпидемиология. Связь употребления алкоголя с развитием цирроза печени впервые установлена M. Baillie в 1793 г. Несмотря на открытие в последние десятилетия многообразных этиологических факторов поражения печени, по сегодняшний день одним из ведущих среди них остается алкоголь. По данным G.A. Zeldin и A.M. Diehl, в 1988 г. среди умерших от цирроза, в 44% случаев причиной заболевания печени явился алкоголь. Следует учитывать, что не у всех лиц, злоупотребляющих спиртными напитками, развивается поражение печени: среди данной группы частота выявления цирроза на вскрытии не превышает 10-15%, в то время как у 30% изменения печени вообще отсутствуют.
Критическая доза алкоголя. Большинство исследователей сходится во мнении, что риск поражения печени значительно увеличивается при употреблении более 80 г чистого этанола в день на протяжении не менее 5 лет. В то же время данная доза может рассматриваться как критическая, преимущественно по отношению к мужчинам. Для женщин, несмотря на очевидно большую чувствительность к алкоголю, подобные данные обычно не приводятся, хотя некоторые авторы указывают в качестве безопасной дозы 20 г этанола в день.
Развитие алкогольной болезни печени (АБП) не зависит от типа спиртных напитков, следовательно, при расчете суточной дозы алкоголя у конкретного больного необходимо учитывать только общую концентрацию этанола.
Постоянное употребление алкоголя наиболее опасно, поэтому риск АБП ниже у лиц, употребляющих спиртные напитки с перерывами не менее двух дней в неделю.
Термины “АБП” и “алкоголизм” не являются синонимами, последний применяется в наркологии для обозначения состояния, характеризующегося психической и физической зависимостью от алкоголя. Более того, по данным A.D. Wodak и соавторов (1983 г), у большинства больных АБП наблюдается слабо выраженная зависимость от алкоголя. У них редко возникает тяжелый похмельный синдром, что позволяет им употреблять спиртные напитки в больших количествах на протяжении многих лет.
Факторы, способствующие развитию АБП. Пол. Женщины более чувствительны к токсическому действию алкоголя, что в определенной степени можно объяснить меньшей активностью алкогольдегидрогеназы слизистой оболочки желудка, что обусловливает более активный печеночный метаболизм этанола.
Генетический полиморфизм метаболизирующих этанол ферментов (см. ниже).
Питание. Этанол нарушает кишечную абсорбцию и депонирование питательных веществ, а также приводит к снижению аппетита за счет высокой собственной калорийности. В результате возникает хронический дефицит белка, витаминов и минералов.
Инфекция гепатотропными вирусами. Инфицирование вирусами гепатитов В и С, нередко наблюдающееся у лиц, злоупотребляющих алкоголем, ведет к прогрессированию поражения печени.
Токсичность ксенобиотиков (см. ниже).
Метаболизм алкоголя. Основным местом метаболизма этанола является печень. До 85% этанола окисляется цитозольным ферментом алкогольдегидрогеназой (АДГ) до ацетальдегида.
1. С2Н5ОН + НАД+  СН3СНО + НАД·Н + Н+ СН3СНО + НАД·Н + Н+
| |
| Этанол | Ацетальдегид |
Ацетальдегид, в свою очередь, при помощи митохондриального фермента альдегидегидрогеназы (АлДГ) подвергается дальнейшему окислению до ацетата через стадию ацетил-СоА.
| АлДГ | |||
2. С2Н4О + НАД+  СН3СООН + НАД·Н + Н+ СН3СООН + НАД·Н + Н+
| |||
| Ацетальдегид | Ацетат |
В обеих реакциях в качестве кофермента участвует никотинамиддинуклеотид (НАД), который, присоединяя протон, восстанавливается до НАД · Н.
Различия в скорости элиминации алкоголя в значительной мере обусловлены генетическим полиморфизмом ферментных систем. АДГ кодируется пятью различными локусами на хромосоме 4. Преобладание наиболее активного изофермента АДГ 2, чаще всего встречающееся у представителей монголоидной расы, обусловливает повышенную чувствительность к спиртным напиткам, проявляющуюся тахикардией, потливостью, гиперемией лица. В случае продолжения употребления алкоголя риск развития поражения печени у них выше вследствие усиленного образования ацетальдегида.
АлДГ кодируется четырьмя локусами на четырех различных хромосомах. У 50% китайцев и японцев основной изофермент АлДГ 2 находится в неактивном состоянии, что служит причиной накопления ацетальдегида и повышения риска поражения печени.
Около 10-15% этанола метаболизируется в микросомах гладкого эндоплазматического ретикулума микросомальной этанол-окислительной системой (МЭОС). Входящий в систему цитохром Р450 2Е1 участвует в метаболизме не только алкоголя, но и ряда лекарственных препаратов, в том числе парацетамола (ацетаминофена). При повышении нагрузки МЭОС проявляет свойства самоиндукции, что в значительной степени обусловливает повышение толерантности к алкоголю на определенном этапе хронического злоупотребления спиртными напитками. Усиленная работа МЭОС ведет к повышенному образованию токсичных метаболитов лекарств, что может явиться причиной поражения печени при применении даже терапевтических доз медикаментов.
Роль каталазной системы, локализованной в пероксисомах цитоплазмы и митохондриях, в метаболизме этанола у человека незначительна.
Патогенез. Токсическое действие ацетальдегида. Ацетальдегид, образующийся в печени под воздействием АлДГ и МЭОС, обусловливает значительную часть токсических эффектов этанола. Основными из них являются:
· усиление перекисного окисления липидов,
· нарушение электронно-транспортной цепи в митохондриях,
· подавление репарации ДНК,
· нарушение функции микротрубочек,
· образование комплексов с белками,
· стимуляция продукции супероксида нейтрофилами,
· активация комплемента,
· стимуляция синтеза коллагена.
Одним из важнейших гепатотоксических эффектов ацетальдегида, проявляющегося в результате усиления перекисного окисления липидов и формирования стойких комплексных соединений с белками, является нарушение функции основного структурного компонента клеточных мембран - фосфолипидов. Это ведет к повышению проницаемости мембран, нарушению трансмембранного транспорта, изменениям функционирования клеточных рецепторов и мембраносвязанных ферментов.
Образование ацетальдегид-белковых комплексов нарушает полимеризацию тубулина микротрубочек, что находит отражение в патоморфологическом феномене, носящим название алкогольного гиалина или телец Мэллори. Ввиду того, что микротрубочки участвуют во внутриклеточном транспорте и секреции белков, нарушение их функции ведет к задержке белков и воды с формированием баллонной дистрофии гепатоцитов.
На экспериментальных моделях показано, что подавление репарации ДНК при хроническом употреблении этанола ведет к усилению апоптоза - программированной смерти клеток.
Нарушение липидного обмена. Окисление этанола обусловливает повышенный расход кофермента НАД+ и увеличение соотношения НАД · Н/НАД. Это приводит к сдвигу вправо реакции:
Дегидроксиацетонфосфат + НАД · Н + Н+  глицеро-3-фосфат + НАД+
глицеро-3-фосфат + НАД+
Последствием повышенного синтеза глицеро-3-фосфата является усиление этерификации жирных кислот и синтеза триглицеридов, что служит начальным этапом развития гиперлипидемии и жировой дистрофии печени. Наряду с этим, нарастание концентрации НАД · Н сопровождается снижением скорости окисления жирных кислот, что также способствует их отложению в печени.
Нарушение функции митохондрий. Хроническое употребление алкоголя способствует снижению активности митохондриальных ферментов и разобщению окисления и фосфорилирования в электронно-транспортной цепи, что, в свою очередь, приводит к уменьшению синтеза АТФ. В роли непосредственных “виновников” указанных нарушений выступают ацетальдегид и жирные кислоты. Развитие микровезикулярного стеатоза печени, представляющего собой одно из наиболее тяжелых осложнений АБП, связывают с повреждением ДНК митохондрий продуктами перекисного окисления липидов.
Повышение клеточного редокс-потенциала. Увеличение соотношения НАД · Н/НАД ведет к повышенному синтезу лактата из пирувата, что обусловливает развитие лактат-ацидоза, наиболее резко выраженного при тяжелых формах острого алкогольного гепатита.
Гипоксия и фиброз. Высокая потребность гепатоцитов в кислороде обусловливает прогрессирующее уменьшение его концентрации в печеночной дольке от зоны 1 (окружение портальной венулы и печеночной артериолы) к зоне 3 (окружение центральной вены). Следовательно, гепатоциты, локализованные в зоне 3, наиболее подвержены последствиям гипоксии - некрозу. Более того, максимальное количество цитохрома Р450 2Е1, в составе МЭОС участвующего метаболизме этанола, обнаруживается именно в зоне 3.
Механизмы этанол-индуцированного фиброгенеза до конца не расшифрованы, однако установлено, что при АБП формирование цирроза может происходить путем прогрессирования фиброза в отсутствие выраженного воспаления. Важным звеном фиброгенеза является активация при гипоксии цитокинов, среди которых особое внимание уделяется трансформирующему фактору роста β (ТФР, ТGF). Происходит трансформация жиронакапливающих клеток Ито в фибробласты, продуцирующие преимущественно коллаген 3-го типа. Другим стимулятором коллагенообразования являются продукты перекисного окисления липидов.
Иммунные механизмы. Реакции клеточного и гуморального иммунного ответа не только играют существенную роль в повреждении печени при злоупотреблении алкоголем, но и в значительной степени могут объяснить случаи прогрессирования заболевания печени после прекращения употребления спиртных напитков. В то же время выраженные иммунологические сдвиги у больных АБП в большинстве случаев обусловлены иными причинами, нежели непосредственное действие этанола, в частности, инфекцией гепатотропными вирусами.
Участие гуморальных механизмов проявляется в первую очередь в повышении уровня сывороточных иммуноглобулинов, преимущественно за счет IgA, и в отложении IgA в стенке печеночных синусоидов. Кроме того, в невысоком титре выявляются сывороточные антитела к компонентам ядра и гладкой мускулатуре, а также антитела к неоантигенам (алкогольному гиалину и ацетальдегид-белковым комплексам).
Отражением клеточных механизмов служит циркуляция цитотоксических лимфоцитов у больных острым алкогольным гепатитом. CD4 и CD8-лимфоциты обнаруживаются также в воспалительных инфильтратах в ткани печени, наряду с повышенной мембранной экспрессией молекул HLA I и II классов. В роли антигенов-мишеней в данном случае, по-видимому, также выступают продукты взаимодействия метаболитов этанола и клеточных структур. Это подтверждается корреляцией количества ацетальдегид-белковых комплексов в биоптатах печени с показателями активности заболевания.
У больных АБП выявляют повышенные концентрации сывороточных провоспалительных цитокинов: интерлейкина-1(ИЛ-1), ИЛ-2, ИЛ-6, тумор-некротизирующего фактора α (ТНФ), которые участвуют во взаимодействии иммунокомпетентных клеток. Кроме того, ТНФ- и ИЛ-8 (фактор хемотаксиса нейтрофилов) через стимуляцию продукции активных форм кислорода и оксида азота вызывают повреждение клеток-мишеней, обусловливая картину полиорганной недостаточности при остром алкогольном гепатите.
На стадии цирроза, в качестве мощного стимулятора перечисленных цитокинов, присоединяется бактериальный эндотоксин. Его проникновение в избыточных количествах в системную циркуляцию обусловлено повышенной проницаемостью кишечной стенки.
Морфология. Жировая дистрофия (стеатоз печени). Жировые включения локализуются преимущественно в гепатоцитах 2 и 3 зон печеночного ацинуса, в более тяжелых случаях капли жира распределяются в ткани печени диффузно (рис. 1). В большинстве случаев включения имеют крупные размеры (крупнокапельное ожирение или макровезикулярный стеатоз). Микровезикулярный стеатоз (мелкокапельное ожирение) ассоциирован с повреждением митохондрий, поэтому наблюдается уменьшение количества митохондриальной ДНК в гепатоцитах.
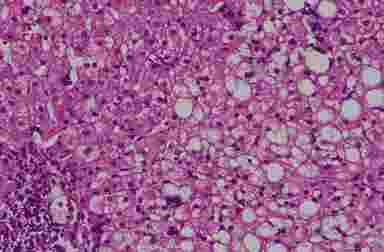
Рис. 1. Жировой гепатоз (биоптат печени, окраска г/э, х200). Диффузная крупнокапельная дистрофия гепатоцитов
Алкогольный гепатит. При развернутой картине острого алкогольного гепатита гепатоциты находятся в состоянии баллонной и жировой дистрофии; практически обязательное присутствие последней послужило поводом для введения термина “алкогольный стеатогепатит” (рис. 2).
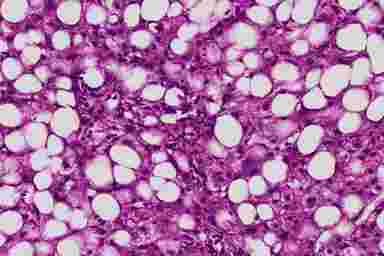
Рис. 2. Алкогольная болезнь печени (биоптат печени, окраска г/э, х200). Алкогольный гепатит на фоне диффузного крупнокапельного ожирения гепатоцитов. Фиброз
В цитоплазме гепатоцитов выявляется алкогольный гиалин (тельца Мэллори), который представляет собой эозинофильные включения, состоящие из конденсированных промежуточных микрофиламентов цитоскелета. Тельца Мэллори характерны для алкогольного поражения печени, однако, также могут встречаться при ПБЦ, болезни Вильсона-Коновалова, раке печени и т.д.
Имеется в той или иной степени выраженный перивенулярный и перисинусоидальный фиброз преимущественно вокруг центральных вен, очаговая инфильтрация долек нейтрофилами с некрозом гепатоцитов в зоне инфильтрации. В различной степени выраженные фиброзные изменения и воспалительная клеточная инфильтрация наблюдаются также в портальных трактах.
Цирроз печени. В начальной стадии цирроз обычно микронодулярный. Формирование узлов происходит относительно медленно вследствие ингибирующего действия алкоголя на регенерацию печени. В ряде случаев выраженного воспаления не наблюдается, что позволяет предположить возможность развития цирроза через стадию перицеллюлярного и септального фиброза (рис. 3).
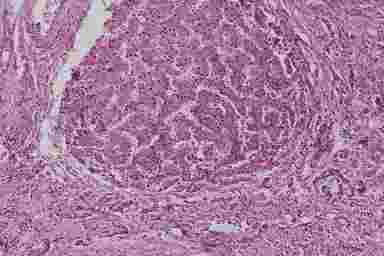
Рис. 3. Алкогольный монолобулярный цирроз печени (секционный случай, окраска г/э, х200). Ложная долька, окруженная прослойкой фиброзной ткани
На поздних стадиях цирроз нередко приобретает черты макронодулярного, что ассоциировано с повышением риска развития гепатоцеллюлярной карциномы (ГЦК).
Для АБП характерно умеренное отложение гемосидерина в гепатоцитах и клетках Купфера, обусловленное повышенным всасыванием железа в кишечнике, высоким содержанием его в некоторых спиртных напитках, гемолизом, портокавальным шунтированием.
Date: 2015-09-02; view: 1012; Нарушение авторских прав