
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Домашнее задание по теме: Номенклатура, структурные изомеры
|
|
Назовите соединения в двух номенклатурах:
СН3 - СН2 - СН - СН - СН=О СН2 - СН - СН2 - СН - С = О
l l l l
ОН NH2 NH2 OH
O = СН - СН2 - СН2 - СН - СН = О СН2 - СН2 - СН - СН2 - С = О
l l l l
OH OH CH3 OH
СН = СН - СН - СН2 - СН = О СН3 - СН - СН2 - СН - С = О
l l l l
CН3 СН3 Cl ОН
СН3 - СН - СН - С = О СН3 - СН - СН = СН - С = О
l l l l l
ОН СН3 ОСН3 СН3 ОН
СН2 = СН - С - СН - СН3 СН3 - СН - СН2 СН = СН2
ll l l
О СН3 ОН
СН3 - СН2 - СН = СН - С = О О = СН2 - СН - СН2 - СН - CН = О
l l l
ОС2Н5 Cl NH2
O = C - CН - СН3
l l
CН3 Br
Вывести формулы всех простых эфиров и изомерных им спиртов, отвечающих формуле С4Н10О Назвать их.
Вывести формулы всех простых эфиров и изомерных им спиртов, отвечающих формуле С4Н8О
Назвать их.
Вывести формулы всех циклических соединений, отвечающих формуле С4Н8О. Назвать их.
Вывести формулы изомерных альдегидов и кетонов, отвечающих формуле С5Н10О. Назвать их.
Вывести формулы непредельных альдегидов и кетонов, отвечающих формуле С5Н8О. Назвать их.
Вывести формулы кетонов, отвечающих формуле С6Н12О. Назвать их.
Вывести формулы изомерных кетонов, отвечающих формуле С5Н8О. Назвать их.
Вывести формулы изомерных спиртов, отвечающих формуле С5Н11О. Назвать их.
Вывести формулы изомерных кислот, отвечающих формуле С6Н12О2. Назвать их.
Вывести формулы изомерных кислот, отвечающих формуле С5Н10О2. Назвать их.
Вывести формулы изомерных дигалогенпроизводных, отвечающих формуле С4Н8Cl2. Назвать их.
Вывести формулы изомерных дигалогенпроизводных, отвечающих формуле С5Н10I2. Назвать их.
Вывести формулы изомерных альдегидов, отвечающих формуле С6Н12О. Назвать их.
Методическое указание для студентов по теме: «Номенклатура органических соединений»
Цель: развить у студентов умение называть органические соединения и строить формулы по названию органических соединений.
I. Основные правила построения названий органических соединений по двум номенклатурам.
Для многих соединений остались тривиальные названия, которые используются в наше время. Например: ацетон, уксусная кислота, муравьиная кислота, этиловый спирт, метиловый спирт и т.д. Эти названия используются и в современной номенклатуре.
1) Выбор главной цепи:
Выбирается цепь, по возможности самая длинная, с наибольшим числом заместителей и функциональных групп.
2) Нумерация цепи:
Цепь нумеруется от старшего заместителя к младшему.
Ряд старшинства:
карбокси оксо, альдо оксо, кето гидрокси
-СООН > производные карбоновых кислот > 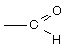 >
> 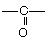 > -ОН >
> -ОН >
нитро амино алкокси фтор,хлор,бром этил,метил
> -NO2 > 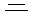 >
>  > -NH2 > -OR > галогены > алкилы
> -NH2 > -OR > галогены > алкилы
Заместители называют от младшего к старшему (кроме кратных связей).
3) Построение названия:
Название строиться по грамматическому правилу (приставка, корень, суффикс и окончание), главная цепь – это предельный углеводород(корень слова), в котором окончание «ан» заменяют на «ен» если есть двойная связь, или на «ин» если есть тройная связь. Суффиксом или окончанием является только одна или две одинаковые старшие функциональные группы. Приставкой слова всегда являются: углеводородные радикалы, галогенные, нитро группы, алкокси группы. Остальные группы могут быть приставкой или окончанием. В зависимости от этого они имеют разные названия.
II. Названия соединений.
Алканы
| CnH2n+2 | Названия алканов | CnH2n+2 | Названия алканов |
| CH4 | Метан | C6H14 | Гексан |
| C2H6 | Этан | C7H16 | Гептан |
| C3H8 | Пропан | C8H18 | Октан |
| C4H10 | Бутан | C9H20 | Нонан |
| C5H12 | Пентан | C10H22 | Декан |
Радикалы
| CnH2n+1 | Название радикалов | CnH2n+1 | Название радикалов |
| CH3- | Метил | (CH3)3C- | Третично-бутил |
| CH3-CH2- | Этил | 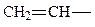
| Винил |
| CH3-CH2-CH2- | Пропил | 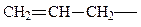
| Аллил |
| (CH3)2-CH- | Изопропил | 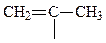
| Изопропенил |
| CH3(CH2)CH2- | Н-бутил | 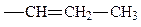
| Пропенил |
| (CH3)2CHCH2- | Изобутил | 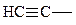
| Ацетиленил |
| CH3CH2CHCH3- | Вторично-бутил |
Спирты
| CnH2n+1OH | ИЮПАК | Тривиальные названия |
| CH3OH | Метанол | Метиловый спирт |
| CH3CH2OH | Этанол | Этиловый спирт |
| CH3(CH2)2OH | Пропанол | Пропиловый спирт |
| (CH3)2-CH-OH | Пропанол-2 | Изопропиловый спирт |
| CH3-(CH2)3-OH | Бутанол | Бутиловый спирт |
| (CH3)2-CH-CH2-OH | 2-метилпропанол | Изобутиловый спирт |
| (CH3)3C-OH | 2-метилпропанол-2 | Третбутиловый спирт |
| CH3-CH2CH(CH3)OH | Бутанол-2 | Вторичнобутилоывй спирт |
| CH2=CH-CH2-OH | 2-пропен-1-ол | Аллиловый спирт |
| HO-CH2-CH2-OH | Этандиол-1,2 | Этиленгликоль |
| OH-CH2-CH(OH)-CH2-OH | Пропантриол-1,2,3 | Глицерин |
Карбоксильные соединения
| СnH2n | ИЮПАК | Тривиальные названия |
| CH2O | Метаналь | Формальдегид |
| CH3CHO | Этаналь | Уксусный альдегид |
| CH3CH2CHO | Пропаналь | Пропионовый альдегид |
| CH3(CH2)2CHO | Бутаналь | Масляный альдегид |
| CH2=CH-CHO | 2-пропеналь | Акролеин |
| CH3CO-CH2-CH3 | Бутанон-2 | Метилэтилкетон |
| CH3CO-CH=CH2 | 3-бутен-он-2 | метилвинилкетон |
Карбоновые кислоты
Одноосновные кислоты
| CnH2nO2 | ИЮПАК | Тривиальные названия кислот |
| HCOOH | Метановая | Муравьиная |
| CH3COOH | Этановая | Уксусная |
| CH3CH2COOH | Пропановая | Пропионовая |
| CH3(CH2)2COOH | Бутановая | Масляная |
| CH3(CH2)3COOH | Пентановая | Валерьяновая |
| CH3(CH2)4COOH | Гексановая | Капроновая |
| CH2=CHCOOH | Пентен-2-овая | Акриловая |
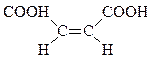
| Цис-бутен-2-диовая | Малеиновая |
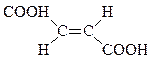
| Транс-бутен-2-диовая | Фумаровая |
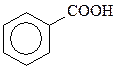
| фенилкарбоновая | бензойная |
Двухосновные кислоты
| ИЮПАК | Тривиальные названия кислот | |
| HOOC-COOH | Этандиовая | Щавелевая |
| HOOC-CH2-COOH | Пропандиовая-1,3 | Малоновая |
| HOOC-(CH2)2-COOH | Бутандиовая-1,4 | Янтарная |
| HOOC-(CH2)3-COOH | Пентандиовая-1,5 | Глутаровая |
| HOOC-(CH2)4-COOH | Гександиовая-1,6 | Адипиновая |
Высшие жирные кислоты
| ИЮПАК | Тривиальные названия | |
| C15H31COOH | - | Пальмитиновая |
| C17H35COOH | - | Стеариновая |
| C17H33COOH | - | Олеиновая |
| C17H31COOH | - | Ленолевая |
| C17H29COOH | - | Леноленовая |
Названия функциональных групп в порядке уменьшения старшинства
| Группа | Префикс | Суффикс |
| -COOH | карбокси | овая кислота |
| -SO3H | сульфо | сульфоновая кислота |
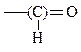
| оксо | аль |
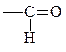
| формил | карбальдегид |
| -(C)=O | оксо | он |
| -OH | гидрокси | ол |
| -SH | меркапто | тиол |
| -NH2 | амино | амин |
| Двойная связь | --- | ен |
| Тройная связь | --- | ин |
| I, Br, Cl, F | иод,бром, хлор, фтор | ---- |
| Alkyl | алкил | ---- |
III. Упражнения на тему:
1. Напишите изомеры соединения C5H11Br, содержащие галоген при вторичном или третичном атоме углерода. Назовите их.
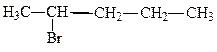 2-бромпентан
2-бромпентан
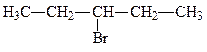 3-бромпентан
3-бромпентан
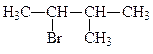 2-бром-3-метилбутан
2-бром-3-метилбутан
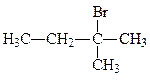 2-бром-2-метилбутан
2-бром-2-метилбутан
2. Назовите соединения, где можно в двух номенклатурах.
а)
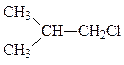 1-хлор-2-метилпропан
1-хлор-2-метилпропан
хлористый изобутил (изобутилхлорид)
б)
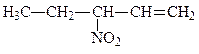 3-нитропентен-1
3-нитропентен-1
этилвинилнитрометан
в)
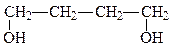 бутендиол-1,4
бутендиол-1,4
тетраметиленгликоль
г)
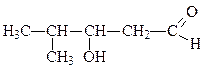 3-гидрокси-4-метилпентаналь
3-гидрокси-4-метилпентаналь
β-гидрокси-изокапроновый альдегид
д)
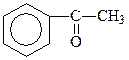 1-фенилэтанон-1
1-фенилэтанон-1
метилфенилкетон
е)
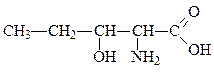 2-амино-3-гидроксипентановая кислота
2-амино-3-гидроксипентановая кислота
α-амино-β-гидроксивалериановая кислота
ж)
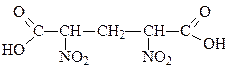 2,4-динитропентандиовая кислота
2,4-динитропентандиовая кислота
α,α’-динитроглутаровая кислота
3. Напишите структурные формулы следующих соединений, назвать в другой номенклатуре.
а) метилвинилхлорметан
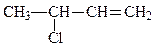 3-хлорбутен-1
3-хлорбутен-1
б) α,β-диметил-α-нитроэтилен
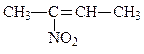 2-нитробутен-2
2-нитробутен-2
в) бутин-3-ол-2
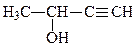 метилацетиленилкарбинол
метилацетиленилкарбинол
г) α-аминоянтарный альдегид
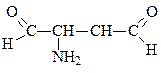 2-аминобутандиаль
2-аминобутандиаль
д) метилизопропиламин
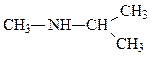 2-N-метиламинопропан
2-N-метиламинопропан
е) метилэтилкетон
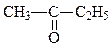 бутанон-2
бутанон-2
ж) β-фенилпропионовый альдегид
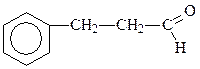 3-фенилпропаналь
3-фенилпропаналь
з) монометиловый эфир янтарной кислоты
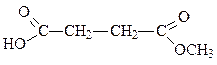
и) винилацетиленилнитрометан
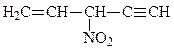 3-нитропентен-1-ин-4
3-нитропентен-1-ин-4
Пример тестового контроля:
А. В двух номенклатурах
в)
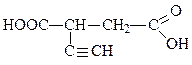 2-ацетиленилбутандиаль
2-ацетиленилбутандиаль
α-ацетиленилянтарный альдегид
г)
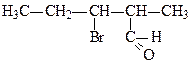 3-бром-2-метилпентаналь
3-бром-2-метилпентаналь
α-метил-β-бромвалериановая кислота
Б. Напишите формулы соединений и назовите их в другой номенклатуре.
в) метилвиниламин
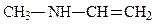 (N-метиламиноэтен)
(N-метиламиноэтен)
г) 3-метилгександиол-3,4
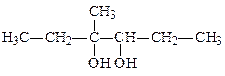 (α-метил-α,β-диэтилэтиленгликоль)
(α-метил-α,β-диэтилэтиленгликоль)
IV. Подготовка к следующему занятию.
1) Каждый студент получает индивидуальные примеры, которые должен выполнить дома.
2) Рекомендуемая литература:
1. Лекции по теме.
2. Н.А. Тюкавкина, Ю.В.Бауков «Биоорганическая химия» изд.Дрофа
3. И.И.Грандберг «Органическая химия», «Практические работы и семинарские занятия по органической химии».
4. Т.П,Сурикова, В.Н.Захарченко «Курс органической химии».
3) Уборка лаборатории. Староста назначает дежурного.
Домашнее задание.
Задание по теме: “Конформация простых молекул,цис,транс-изомерия.”
1Написать все возможные цис,транс-изомеры для соединений:
1.1-бромпентен-1 2-бромпентен-2 2-бромпентадиен-1,3
2.2-бромпентен-2 2-бромпентен-1 2-бромпентадиен-1,4
3. 1-аминобутен-1 2-аминобутен-2 1-аминобутадиен-1,3
4.2-метилпентен-2 4-метилпентен-2 2-метилпентадиен-1,3
5. 2-хлорпентен-2 2-хлорпентадиен-1,3 4-хлорпентадиен-1,3
6.2-метилгексен-2 2-метилгексен-3 2-метилгексадиен-1,4
72-нитропентен-2 1-нитропентадиен-1,4 2-нитропентадиен-1,4
8. 2-метилгексен-1 2-метилгексадиен-2,4 2-метилгексадиен-2,4
9.1-аминобутен-2 2-аминобутен-1 2-аминобутадиен-1,3
10. 2-метилпентен-2 2-метилпентен-1 2-метилпентадиен-1,3
11.1-метоксипентен-2 2-метоксипентен-1 1-метоксибутадиен-1,3
12. 1-бромпентен-2 1-бромпентадиен-1,3 1-бромпентадиен-2,4
11 Написать предпочтительные конформации для соединений:
1 Этандиол
2.1-хлорпропан(С1-С2)
3. 1,2-дихлорэтан
4. Бутандиовая кислота (С1-С2)
5. 2-Бромэтанол
6. 1-Амино-2-бромэтан
7.Этандиамин-1,2
8. 2-хлорпропан(С1-С2)
9.1,2 -Динитроэтан
10. Бутандиаль(С2-С3)
1.1-Бромпропанол -2(С1-С2)
12. 3-хлорбутанол-2 (С1-С2)
13. 3-аминобутантиол-2 (С1-С2)
Тема: Пространственная изомерия органических соединений. Цис-транс изомерия. Конформация.
Цель занятия: приобрести развить знания конформации и конфигурации (на примере цис-транс изомеров) как основных элементов пространственного строения органических соединений, необходимое для понимания их реакционной способности.
План занятия:
1. Теоретический опрос и упражнения (практическое занятие по теме).
Содержание практического и лабораторного занятий.
Программа для самоподготовки.
- Понятие пространственной изомерии.
- Поворотная изомерия. Конформация простых молекул.
- Способы изображения конформаций. Рисунки, проекции Ньюмена.
- Способы обозначения конформаций.
- Понятие предпочтительной конформации. Факторф. Влияющие на стабилазацию предпочтительной конформации.
- Условия возникновения цис-транс изомеров, имеющих нециклическое строение. Понятие «конфигурация».
- Способы изображения конфигурации цис-транс изомеров, типы изомеров, обозначение конфигурации.
- Зависимость свойств цис-транс изомеров от конфигурации.
Упражнения
- Изобразить в проекциях Ньюмена все конформации 2-хлорбутана вдоль связи С2-С3, обозначить (назвать) их и указать предпочтительную.
- Изобрапзить в проекции Ньюмена предпочтительную конформацию 2-аминоэтанола-1 и указать факторы, влияющие на ее стабилазацию.
- Изобразить качественно на диаграмме зависимость энергии молекулы 1,2-дихлорэтана от конформации.
- Какие из следующих соединений существуют в виде цис-транс изомеров? Напишите проекционные формулы и обозначьте конфигурацию изомеров: а). пентен-1 б). пентен-2 в). пентадиен-1,3 г). пентадиен-1,4 д). 2-хлорбутен-2 е). гексадиен-2,4.
Подготовка к занятию:
1. лекция
2. Грандберг И.И., Дрофа, 2001, стр. 178-179.
Оптическая изомерия. Домашнее задание.
по теме: «Оптическая изомерия»
I. Напишите проекционные формулы соединения, обладающего оптической изомерией. Укажите число изомеров, их соотношение.
1) 2, 3 дигидроксибутаналь
2) 2,3-дигидроксибутановая кислота
3) 3-метилпентадиол-2
4) 2-бромпентанол-3
5) 2,3-диметилбутандиовая кислота
6) гександиол-3,4
7) 3,4-динитропентен-1
8) 3-бромбутанол-2
9) 2,3-дихлорпентан
10) 2,3-дихлорбутандиаль
11)2,3-диаминобутаналь
II. Для соединений написать предпочтительную конформацию:
1) эритро-2,3 - дихлорпентан
2) трео /2,3 - динитропентандиаль
3) эритро-бутандиол-2, 3
4) трео 3 - аминобутанол -2
5) эритро-2 - амино,- 3 -метилпентановая кислота
6) трео-2, 3 -диаминобутановая кислота
7) эритро-3 -аминобутанол- 2
8) трео2, 3 -дибромпентан
9) эритро-2 -амино-3 -гидроксибутановая кислота
10)трео-2 -амино-3 -гидроксипентановая кислота
11)эритро-2 -нитро-3 -хлорбутаналь
III. Напишите структурные формулы изомеров, для которых возможна пространственная изомерия. Укажите тип изомерии, проекционные формулы.
1) 2-метил-1-хлорциклопропан
2) 2-этилциклобутанол-1
3) 1,2-диэтилциклопентан
4) 1,2-динитроциклобутан
5) 2-метилциклопентанкарбальдегид
6) циклобутан –1,3-дикарбоновая кислота
7) 1,3-диизопропилциклобутан
8) 1,1,2-триэтилциклопропан
9) 1-этил-3-метилциклопентан
10)3-метилциклопентен-1
1.2-дибромциклопропан.
Тема: " Пространственная изомерия. Оптическая изомерия.
Цель занятия: приобрести знание основных положений стереохимии об оптической изомерии как одном из видов пространственной изомерии, а также о зависимости свойств изомеров от конфигурации, необходимые для понимания механизма биологического действия природных соединений; научить изображать пространственное строение оптических изомеров с помощью проекционных и перспективных формул, строить пространственные модели простых молекул и составлять названия изомеров с учетом их конфигурации.
Цель лабораторной работы: ознакомиться с о перегонкой как методом очистки жидкостей и приобрести навыки выполнения простой перегонки низкокипящего растворителя; получить представления об определении температуры кипения, плотности и показателя преломления для оценки "химической чистоты" вещества.
План занятия:
1. Теоретический опрос и упражнения (практическое занятие по теме).
2. Тестовый контроль (по всем типам стереоизомерии).
Содержание практического и лабораторного занятий.
Программа для самоподготовки.
1. Условия возникновения оптических изомеров. Понятие асимметрического атома углерода.
2. Число изомеров. Типы (энантиомеры. диастереомеры, мезоформа). Рацемат. Сравнение свойств изомеров и мезоформы с рацематом.
3. Способы изображения оптических изомеров. Проекционные формулы Фишера (правила проекции молекулярной модели на плоскость и правила пользования проекционными формулами).
4. Переход от проекций Ньюмена к проекциям Фишера и установление соотношения изомеров.
5. Переход от проекций Фишера к проекциям Ньюмена (проедпочтительная конформация).
6. Способы обозначения конфигурации оптических изомеров. Понятие об L, D, "трео" и "эритро"-изомерах. Стереохимическая R,S-номенклатура.
7. Названия оптических изомеров с учетом конфигурации.
Подготовка к занятию:
1. лекция 2. Грандберг И.И., Дрофа, 2001, стр. 430-446.
6. Упражнения:
I. Какие из перечисленных соединений существуют в виде оптических изомеров? Укажите число изомеров и их соотношение.
а. 2,3-дихлорпентан
б. 2,4-дихлорпентан
в. 3-бромбутен-1
г. а-аминомасляная кислота
д. а-амино-в-гидроксимасляная кислота
II. Назовите соединения (в) и (г) из предыдущего упражнения с учетом R,S-конфигурации.
III. Для соединения (а) из предыдущего упражнения сделайте перевод проекционных формул Фишера в проекции Ньюмена (предпочтительную конформацию).
IV. Переведите проекции Ньюмена в проекции Фищера и установите соотношение стереоизомеров:
а.
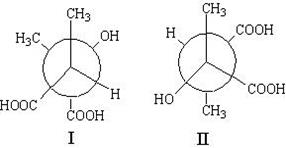
б.
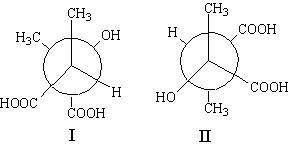
Пример тестового контроля.
1. Какой тип изомерии (без учета конформационной) характерен для следующего соединения (укажите число изомеров, проекционные формулы, тип изомерии): а,а-дигидроксиянтарная кислота.
2. Перевести проекции Фишера в проекции Ньюмена (предпочтительную конформацию):
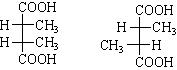
3. Перевести проекции Ньюмена в проекции Фишера и указать соотношение стереоизомеров:
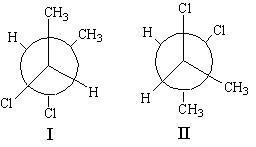
Ответы:
- Оптическая, три (энантиомеры и мезоформа):
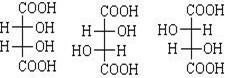
2.
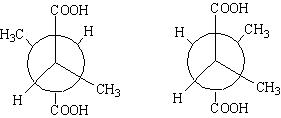
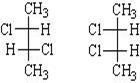
- Диастереомеры
Органическая химия Методические указания для студентов к
(отд мед бф ) занятию
Типы связей в орган.соединениях.
Домашнее задание по теме: «Типы связей. Электронные эффекты.»
1. Обозначить электронные эффекты и написать набор резонансных структур (где это возможно):
2-гидроксипропаналь; 1-нитропентадиол-2,3; метоксиэтен;
2-аминобутен-1; пропен-2-овая кислота; 4-бромбутен-1;
1-хлорбутен-2; 1-хлорбутен-1; 1-хлорциклогексадиен-1,3;
пентен-3-он-2; 1,1-дифторэтен; 1-бромбутен-2;
1-аминопропен-1; 3-аминопропен-1; 1,3-дихлорпропен-1;
2-метилциклопентен-1-карбоновая кислота; 1-хлорциклопентен-1;
3-хлорциклопентен;
пентадиен-1,3; 2-нитропропен-1; этановая кислота;
3-N-метил-1-пропенамин; 1-N-метилпропен-1-амин, пропен-2-аль-1;
пентен-2-аль-1; пентен-3-аль-1; N-метил-N-этилэтенамин;
4-нитро-1-гидроксибензол; метилбензол; хлорбензол;
пентен-2-овая кислота; пентен-3-овая кислота; пропоксиэтен
гексадиен-2,5-аль; этановая кислота; 1-хлорциклопентен-1;
гексен-2-аль; 1- метилциклопентадиен-1,3; 3-метилбутаналь.
2. Сравнить кислотность следующих соединений:
этандиовая кислота; пропановая кислота; пропандиовая кислота;
пропан-2-овая кислота; этановая кислота; 3-хлорпропен-2-овая кислота;
2-хлорпропановая кислота; 2-метилпропановая кислота; 3-хлорпропановая кислота;
этановая кислота; гидроксибензол; 2-метилгидроксибензол;
этановая кислота; метановая кислота; хлорэтановая кислота;
2,2,2-трихлорметановая кислота; 2-нитроэтановая кислота; этановая кислота;
пропанол-2; пропанол-1; гидроксибензол;
2-бромэтановая кислота; 2-бромпропановая кислота; 2,2-дибромэтановая кислота;
бутанол-1; 2-метилпропанол-2; 2-метилпропанол-1;
гидроксибензол; п-нитрогидроксибензол; п-метоксигидроксибензол;
пропановая кислота; 2,2-диметилпропановая кислота; 3-хлорпропановая кислота;
2-нитробутановая кислота; 2-метилбутановая кислота; 2 -гидроксибутановая кислота.
ТЕМА:»Типы связей. Электронные эффекты заместителей в органической химии. Влияние их на свойства органических соединений».
ЦЕЛЬ ИЗУЧЕНИЯ ТЕМЫ: сформировать знания основных положений теории химических связей в органической химии с учетом электронного влияния различных функциональных групп, умения обозначать электронные эффекты и на этой основе уметь оценивать распределение электронной плотности в органической молекуле.
ПЛАН ЗАНЯТИЯ:
1.Практическое занятие по теме.
2.Тестконтроль.
СОДЕРЖАНИЕ ЗАНЯТИЯ:
1.Типы связей в органической химии. Ковалентная связь, гибридизации и геометрия молекулы. Характер гибридных орбиталей. σ - и π – Связи, их свойства.
2. Донорно-акцепторный механизм образования ковалентной связи. Примеры соединений с такой связью.
3. Ковалентная связь, полярная и неполярная. Водородная связь, ее особенности, влияние на свойства соединений.
4.Электронные эффекты заместителей: индуктивный и мезомерный, обозначение. Передача индуктивного и мезомерного эффектов.
5.Индуктивный эффект. Электроотрицательность и сила индуктивного эффекта Примеры.
6.Мезомерный эффект. Условия проявления мезомерного эффекта. Основные заместители, проявляющие +- М эффект. Обозначение М- эффекта. Резонансные структуры и мезомерная формула.
7.Сопоставление мезомерного и индуктивного эффектов.. Понятие об электронодонорных и электроноакцепторных заместителях.
8.Влияние электронных эффектов на свойства органических соединений. Сравнение кислотных и основных свойств органических соединений, устойчивости радикалов, катионов и анионов.
ПОДГОТОВКА К ЗАНЯТИЮ:
1. Работа над лекциями.
2. И.И.Грандберг, Н.Л.Нам, Органическая химия, Дрофа, М., 200 9, стр.29-62, 68-77.
3. Т.П.Сурикова и В.Н.Захарченко, Курс органической химии, М., 2006г, стр.3-20.
ВЫПОЛНЕНИЕ УПРАЖНЕНИЙ:
1)Охарактеризовать типы связей в следующих соединениях: а) этанол б) этилнатрий,
в) бутан, г) нитрометан
2) Из следующих соединений выбрать те, в которых возможна водородная связь?
А) пропанол б) пропаналь в) пропионоая кислота г) пропанамин д) этандиол-1,2
3) Опишите молекулы этана, бутена -2, бутина-2 по теории ВС.
4) Сравните отнoсительную силу индуктивного эффектов заместителей
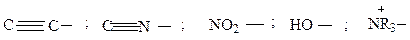
5)Сравните относительную силу мезомерного эффекта заместителей:
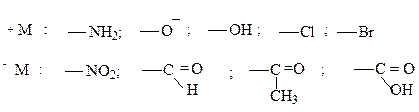
6) В каких соединениях заместители проявляют мезомерный эффект?
Обозначьте его, напишите резонансные структуры и мезомерную формулу.
а) бутин-3-овая кислота
б) бутен-2-овая кислота
в)3-нитропопен-2-аль
г) 3-хлорпропен-1
д) 2-хлорпропен-1
7) Сравнить силу кислот: этановая, этандиовая хлорэтанова, трихлорэтановая
8) Сравнить основность соединений: этанол, этоксиэтаен, этанамин, пропанол-2
ПРИМЕР ТЕСТОВОГО КОНТРОЛЯ:
1.Обозначить электронные эффекты, написать набор резонансных структур (где возмажно):
а)
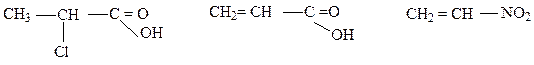
а б в
2.Сравнить кислотность соединений: этанол, этановая кислота, пропанол-2, пропандиол-1,2.
3) Сравнить относительную силу + М – эффекта заместителей?
- NH2, - OCH3 - OH - Cl

ОТВЕТ:
2) 1 > 4 >2 >3
3) - NH2 > - OCH3 > OH > Cl
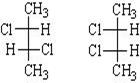
Домашнее задание по теме: «Углеводороды».
Задание: Закончить реакции и объяснить механизм с учетом их стереоспецифичности.
Назвать продукты:
I.
| 2,3 - диметилбутан | + Cl2/hν | → | |
| 2,3 - диметилбутан | + Br2/hν | → | |
| 2,3 - диметилбутан | + O2/hν | → | |
| 3 - метилбутен -2 | + Br2/hν | → | |
| 3 - метилбутен -2 | + O2/hν | → | |
| 2 - метилбутан | + Cl2/hν | → | |
| 2 - метилбутан | + Br2/hν | → | |
| Бутен - 1 | + O2/hν | → | |
| Бутен - 1 | + Br2/hν | → | |
| 2,2,4 - триметилпентан | + O2/hν | → | |
| 2,2,4 - триметилпентан | + Br2/hν | → | |
| 2- метилпентан | + Br2/hν | → | |
| 4,4 - диметилпентен-2 | + O2/hν | → | |
| пентен -1 | + Br2/hν | → | |
| гексен - 3 | + O2/hν | → | |
| 3- метилгексан | + Br2/hν | → | |
| пропен | + O2/hν | → |
II.
| Z-бутен-2-аль | + | Br2→ | (+HCl→) | |
| Е-1,1,1-трифторбутен-2 | + | Br2→ | (+HBr→) | |
| Z- Бутен-2-овая кислота | + | Br2→ | (+H2O(H+)→) | |
| Е-1-метоксибутен-1 | + | Br2→ | (+HCl→) | |
| Z-1-нитро–З-хлорпропен-1 | + | Br2→ | (+HBr→) | |
| Е-3-нитропропен-2-ая кислота | + | Br2→ | (+H2O(H+)→) | |
| Z-3-нитропропен - 2-ол-1 | + | Br2→ | (+HCl→) | |
| Z-1-метоксибутен-1 | + | Br2→ | (+H2O(H+)→) | |
| Е-бутен-2-аль | + | Br2→ | (+HBr→) | |
| Е-3-нитропропен-2-ол-1 | + | Br2→ | (+HBr→) | |
| Z-1,1,1-трифторбутен-2 | + | Br2→ | (+HCl→) | |
| Z-метилпропениловый эфир | + | Br2→ | (+H2O(H+)→) | |
| Е-бутен-2-аль | + | Br2→ | (+HBr→) | |
| Z-1-нитробутен-1 | + | Br2→ | (+H2O(H+)→) | |
| Е-1-нитропентен-2 | + | Br2→ | (+HCl→) | |
| Z–бутен-2-аль | + | Br2→ | (+H2O(H+)→) | |
| E-1-метоксипропен-1 | + | Br2→ | (+H2O(H+)→) |
Date: 2015-09-02; view: 10693; Нарушение авторских прав