
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Решение. Сгорает индивидуальное химическое соединение в конденсированном состоянии
|
|
Сгорает индивидуальное химическое соединение в конденсированном состоянии.
1. Составляем уравнение реакции горения ацетона в воздухе:
С3Н6О + 4(О2 + 3,76 N2) = 3 CО2 + 3 Н2О + 4×3,76 N2.
2. Объём воздуха, необходимый для сгорания 1 кг ацетона, рассчитываем по формуле (7), учитывая при этом, что масса одного киломоля ацетона составляет 58 кг/кмоль:
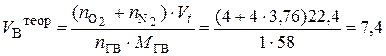 (м3/кг).
(м3/кг).
3. Действительный объём воздуха, пошедшего на сгорание 1 кг ацетона, рассчитывается с учётом коэффициента избытка воздуха a:
 (м3/кг).
(м3/кг).
4. Избыток воздуха составит:
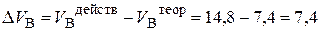 (м3/кг).
(м3/кг).
5. Теоретический объём продуктов горения рассчитываем по формуле (14):
 (м3/кг).
(м3/кг).
6. Действительный объём продуктов горения составит:
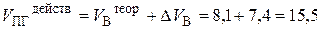 (м3/кг).
(м3/кг).
7. Объём воздуха, теоретически необходимого для сгорания 100 кг ацетона, составит соответственно 740 м3 (7,4 × 100), при этом выделится 1 550 м3 продуктов сгорания.
8. Процентное содержание углекислого газа рассчитывается по формуле, %
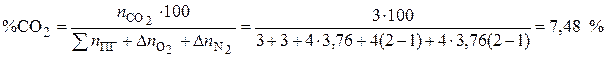
Ответ: При сгорании 100 кг ацетона объём воздуха при нормальных условиях составит 1480 м3, а объём продуктов горения – 1550 м3, процентное содержание углекислого газа в продуктах горения составило 7,48 %.
Примечание. Если в процессе горения были заданы условия, отличные от нормальных (Т ¹273 К, Р ¹101,3 кПа), то объём продуктов горения и воздуха рассчитывается с учётом объёма, который занимает один кмоль газа при заданной температуре:
 , (25)
, (25)
где Р 0 =101,3 кПа; Т0 = 273 К; Т и Р заданные температура и давление.
ПРИМЕР: Рассчитать количество толуола (С7Н8), которое сгорело в закрытом помещении объёмом 100 м3, если содержание кислорода в продуктах горения составило 12 %. Условия нормальные.
Date: 2015-08-15; view: 1901; Нарушение авторских прав