
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Активация протеолитических систем плазмы крови. К протеолитическим системам плазмы крови относятся системы комплемента, калликреин-кининовая, а также фибринолитическая и свертывания крови
|
|
К протеолитическим системам плазмы крови относятся системы комплемента, калликреин-кининовая, а также фибринолитическая и свертывания крови. Все они играют определенную роль в физиологических процессах, а также участвуют в развитии некоторых компенсаторных приспособительных реакций организма при действии на него различных повреждающих факторов. И только в случаях, когда активация этих систем становится неоптимальной, несоответствующей данным конкретным условиям, они превращаются в патогенный фактор, обусловливающий развитие патологического процесса.
Калликреин-кининовая система. Активация этой системы приводит к образованию кининов.
Кинины — группа биологически активных нейровазоактивных полипептидов. Наиболее изученными являются калликреин-кининовая система плазмы крови и один из кининов — нонапептид брадикинин.
Физиологическое значение кининов основано на том, что они оказывают непосредственное влияние на тонус и проницаемость сосудистой стенки, вызывая расширение прекапиллярных сосудов и увеличивая проницаемость капилляров. В связи с этим кинины играют особую роль в органах, периодически экскретирующих значительные количества жидкости (слюнные железы, поджелудочная железа, потовые железы, желудок, кишечник).
Активация калликреин-кининовой системы происходит при действии на организм различных повреждающих факторов, нарушающих целостность клеток и тканей и приводящих, как правило, к активации фактора Хагемана. Это — травмы, токсины, облучение, накопление продуктов обмена веществ (например, кристаллов мочекислого натрия), ишемия и др. Обычно в результате местных повреждающих воздействий развивается воспаление. В его развитии определенную роль играет увеличение содержания кининов, которые через изменение сосудистой реакции оказывают влияние на интенсивность и характер воспаления, а также участвуют в формировании чувства боли. Участвуют кинины и в развитии общих реакций организма на повреждение, причем главным образом в формировании компенсаторно-приспособительных механизмов, и только в случаях неадекватного их образования кинины могут стать патогенетическим фактором различных расстройств.
Одно из таких компенсаторно-приспособительных влияний выявляется в генерализованном действии на гемодинамику. При определенной концентрации кинины уменьшают периферическое сопротивление сосудов малого и большого кругов кровообращения, что увеличивает возврат крови к сердцу, а это, в свою очередь, увеличивает ударный объем обоих желудочков сердца. Этот механизм может включаться при срочных или длительных адаптивных реакциях организма в условиях действия на него различных факторов в виде эмоциональных или физических нагрузок, тепла, гипоксии и др. При острой ишемии и инфаркте миокарда компенсаторная роль увеличенного образования кининов сводится к расширению сосудов миокарда и увеличению сердечного выброса, а также к развитию гипотензии, что облегчает работу сердца и вызывает перераспределение крови. Неадекватность активации калликреин-кининовой системы может стать патогенетическим фактором развития фатальной гипотензии, шока, болевого эффекта (кардиогенный шок).
Кинины принимают участие в развитии реакций при аллергической альтерации тканей. Аллергическое воспаление, как и обычное, также сопровождается увеличением концентрации кининов.
Их обнаруживают в довольно значительной концентрации в экссудате суставов при ревматоидном артрите. Кроме того, увеличение их содержания в крови и спинно-мозговой жидкости выявляется у собак с экспериментальным аллергическим энцефаломиелитом, в миокарде и плазме крови кроликов с экспериментальным аллергическим миокардитом.
Установлено 10–15-кратное увеличение содержания кининов в крови больных людей во время обострения бронхиальной астмы. Очевидно, кинины играют определенную роль в развитии бронхоспазма, так как обладают способностью вызывать при определенной концентрации спазм гладкой мускулатуры бронхиол. Сокращение гладкомышечных клеток при взаимодействии кининов со специфическими мембранными рецепторами приводит к активации кальциевых каналов и поступлению кальция в цитоплазму, где он и стимулирует процесс сокращения. Это действие усиливается на фоне снижения активности β-адренергических рецепторов, что, в частности, имеет место у больных бронхиальной астмой. В такой ситуации концентрация кининов, недостаточная для индукции бронхоспазма у здорового человека, способна вызвать его у больного, имеющего пониженную активность β-адренергических рецепторов.
Активация калликреин-кининовой системы обнаружена при шоках различной этиологии, ревматизме, нефритах, артритах, карциноидном и демпинг-синдромах, атеросклерозе, гипертонической болезни и ряде других заболеваний. Соотношение защитного и патогенного компонентов в каждом конкретном случае различно. Применяя ингибиторы протеолиза, можно ограничить активность калликреин-кининовой системы, а следовательно, выраженность соответствующих симптомов и интенсивность развития патологического процесса.
Комплемент — система функционально связанных сывороточных белков (Cl, C2 и т.д.), активация которых приводит к образованию биологически активных веществ, участвующих в защитных реакциях организма. Различают два пути активации комплемента: классический и aльтepнaтивный.
Классический путь активируется комплексом «антиген+антитело» (рис. 14-14). В процессе активации происходит расщепление ряда компонентов комплемента (С) с образованием активных продуктов. Некоторые из них удаляются из цепи активации, другие объединяются. Конечным этапом активации является образование комплекса С5-9, оказывающего цитотоксическое действие на клетки-мишени (клетки тканей, микробы с фиксированными на них антителами). Если проанализировать эффекты различных компонентов С, то окажется, что все они участвуют в развитии того или иного компонента воспалительной реакции. Поэтому сложилось представление, что биологический смысл активации С заключается в подключении к иммунной (специфической) реакции неспецифических механизмов защиты — фагоцитоза, воспаления, при помощи которых образовавшийся комплекс фиксируется и фагоцитируется.
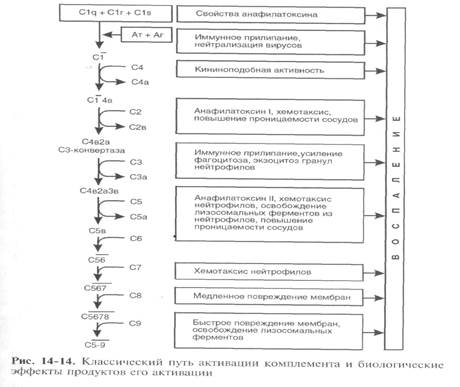
Альтернативный путь активации С является важнейшим механизмом противоинфекционной защиты и активируется бактериальными полисахаридами. Он включается быстро и без участия иммунных механизмов. В отличие от классического пути активация начинается с расщепления С с участием ряда дополнительных факторов. Процессы активации комплемента контролируются ингибиторами различных звеньев этой системы. Наиболее изучены С1- и СЗ-ингибиторы. С1-ингибитор эстеразы блокирует спонтанную активацию С1. Кроме того, он ограничивает активность калликреин-кининовой и фибринолитической систем.
Неконтролируемая активация комплемента приводит к развитию патологических процессов. Возможны генетически детерминированные дефициты отдельных ингибиторов, передающиеся по аутосомно-рецессивному типу. Так, при дефиците С1-ингибитора различные, даже не очень выраженные повреждения запускают начальную цепь классического пути активации комплемента до СЗ, которая обрывается СЗ-ингибитором. В результате формируется врожденный ангионевротический отек в связи с образованием С2 в фрагмента, обладающего кининоподобной активностью. При дефиците СЗ-ингибитора усиливается действие СЗ и нарушается функционирование альтернативного пути активации, что приводит к снижению противоинфекционной защиты с развитием тяжелых бактериальных инфекций (пневмония, отиты, гаймориты, менингиты).
Встречаются случаи дефицитов отдельных компонентов системы С. Они обычно передаются также по аутосомно-рецессивному типу и служат причиной бактериальных инфекций и волчаночно-подобных синдромов.
Избыточная активация того или иного компонента комплемента является патогенетическим фактором ряда патологических процессов. Она лежит в основе многих случаев неиммунологических аллергических реакций (псевдоаллергических) на лекарственные препараты, принимает в той или иной степени участие в развитии некоторых видов шока, особенно септического. Последнее связано с выраженными активирующими свойствами эндотоксина. Эндотоксин является универсальным активатором ряда протеолитических систем (рис. 14-15) плазмы крови. И если эта активация не носит лавинообразного характера, то только потому, что она ограничивается различными ингибиторами и механизмами обратной связи.
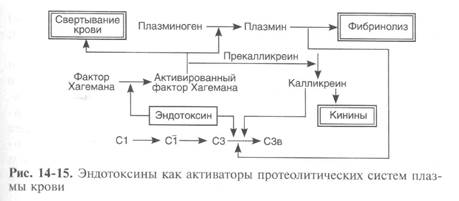
Активирующим действием обладают и некоторые эндогенно образующиеся ферменты. Так, трипсин, плазмин, калликреин могут запускать альтернативный путь активации комплемента. Все эти энзимы обычно активируются при различных повреждающих воздействиях.
Общий белок.
В плазме крови человека содержится около 100 различных белков. По подвижности при электрофорезе их можно грубо разделить на пять фракций: альбумин, α1-, α2-, β- и γ-глобулины. Разделение на альбумин и глобулин первоначально основывалось на различии в растворимости: альбумины растворимы в чистой воде, а глобулины — только в присутствии солей.
Определение уровня общего белка является одним из важнейших лабораторных показателей, т.к. белки плазмы крови играют важную физиологическую роль в организме:
- поддерживают вязкость, текучесть крови;
- определяют объем крови в сосудистом русле;
- удерживают форменные элементы крови во взвешенном состоянии;
- осуществляют транспорт многочисленных экзо- и эндогенных веществ (гормонов, минеральных компонентов, липидов, пигментов и др. биологически важных соединений);
- регулируют постоянство рН крови;
- являются факторами свертывания крови;
- участвуют в иммунных реакциях (иммуноглобулины, опсонины, белки острой фазы).
Основная масса белков плазмы синтезируется в печени. Клетки печени (гепатоциты) участвуют в синтезе альбуминов, фибриногена, α- и β-глобулинов, компонентов свертывающей системы. Большая часть β- и γ-глобулинов синтезируется в клетках иммунной системы (лимфоцитах).
Содержание общего белка в сыворотке (плазме) крови можно охарактеризовать понятиями «нормо-», «гипер-» и «гипопротеинемия», по которыми подразумеваются состояния, сопровождающиеся нормальной (не выходящей за пределы физиологических колебаний), повышенной и пониженной его концентрацией в крови.
Изменения уровня общего белка плазмы крови и отдельных фракций может быть обусловлено многими причинами, причем это касается как количественного, так и качественного состава белков. Эти изменения не являются специфическими, а отражают общий патологический процесс (воспаление, некроз, новообразования), динамику и тяжесть заболевания. С их помощью можно оценить эффективность лечения.
Изменения концентрации общего белка могут быть физиологическими, относительными и абсолютными.
Физиологическая гипопротеинемия может наблюдаться у детей раннего возраста, у женщин во время беременности (особенно в третьем триместре), при лактации, при длительном постельном режиме.
Относительные изменения содержания белка наблюдаются при увеличении (уменьшении) объема циркулирующей крови. Так, гидремия (нагрузка водой, «водное» отравление) приводит к относительной гипопротеинемии, а дегидратация (обезвоживание) – к относительной гиперпротеинемии.
Абсолютная гипопротеинемия - наблюдается при:
- Недостаточности поступления белков в организм вследствие голодания, недоедания, сужения (стриктуры) пищевода, нарушения целостности и функции желудочно-кишечного тракта, при продолжительных воспалительных процессах в стенке кишечника и других состояниях, сопровождающихся ухудшением переваривания и всасывания белков.
- Нарушении синтеза белков в организме вследствие нарушения белковосинтетической функции печени (циррозы, гепатиты, карцинома и метастазы опухолей в печень, токсическое поражение)
- Повышенных потерях белка организмом вследствие острых и хронических кровотечений, обширных ожогов, хронических заболеваний почек с нефротическим синдромом
- Усиленном катаболизме (распаде) белка вследствие продолжительной гипертермии, термических ожогов, тиреотоксикоза, длительных физических нагрузок, онкологических заболеваний
- Перераспределении белка (выход белка из сосудистого русла и образование экссудатов и транссудатов)
Абсолютная гиперпротеинемия – сравнительно редкое явление, наблюдается при:
- Острых и хронических инфекционных заболеваниях (за счет глобулинов)
- Аутоиммунной патологии (системная красная волчанка, ревматоидный артрит, ревматизм и т. д)
- Онкологических заболеваниях с гиперпродукцией патологических белков - парапротеинемия (миеломная болезнь (плазмоцитома), макроглобулинемия Вальденстрема)
Date: 2015-08-07; view: 723; Нарушение авторских прав