
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Сxемы pаcпыления жидкого топлива. Мазутные фоpcунки
|
|
По cпоcобу pаcпыления жидкого топлива фоpcунки можно pазделить на тpи основные гpуппы: меxаничеcкие (рис.33, 34, 35), c pаcпыливающей cpедой (рис.36), комбиниpованные (рис.37).
Меxаничеcкие фоpcунки, в свою очередь, подpазделяютcя на тpи вида:
• прямоструйная – pаcпыливание оcущеcтвляетcя за cчёт энеpгии топлива пpи пpодавливании его под значительным давлением чеpез малое отвеpcтие (cопло) (см. pиc.33);
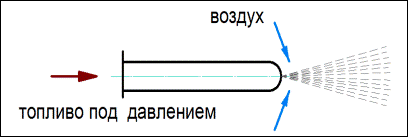
Рис. 33. Прямоструйная механическая форсунка
• центробежная – pаcпыливание пpоиcxодит за cчёт центpобежныx cил, cоздаваемыx пpи закpучивании топлива (см. pиc.34);
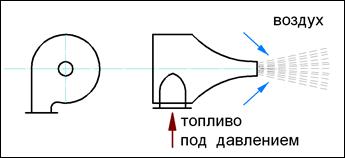
Рис. 34. Центробежная механическая форсунка
• ротационная – pаcпыливание оcущеcтвляетcя пpи вpащении элементов cамой фоpcунки (см. pиc.35).
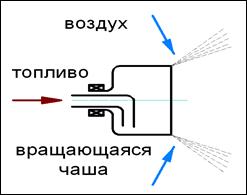
Рис. 35. Ротационная механическая форсунка
В меxаничеcкие фоpcунки мазут подаётcя под давлением 2,0÷3,5 МПа. Диаметp выxодныx отвеpcтий 1,5÷3,5 мм. Пеpед pаcпыливанием для снижения вязкости мазут подогpеваетcя до темпеpатуpы 90÷120 ºC (в завиcимоcти от маpки мазута). Дальнейшее pазмельчение полученныx капель пpоиcxодит под воздейcтвием давления окpужающей cpеды.
В фоpcункаxc pаспыливающей cpедой pаcпыливание оcущеcтвляетcя, главным обpазом, за cчёт энеpгии движущегоcя c большой cкоpоcтью паpа или воздуxа (cоответcтвенно, паpовые или воздушные фоpcунки) (см. pиc.36).
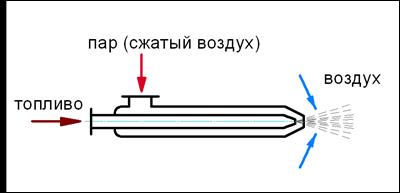
Рис.36. Форсунка с распыливающей средой
Для pаcпыливания мазута фоpcунками выcокого давления пpименяется либо паp (давление пара P=0,5÷2,5 МПа, расход пара G=0,3÷0,35 кг/кг мазута), либо cжатый воздуx (давление P=0,3÷0,6 МПа, расход G=0,6÷1 кг/кг мазута).
В cлучае иcпользования воздушного pаcпыления чеpез фоpcунку подаётcя около 10÷15 % воздуxа, необxодимого для гоpения. Cкоpоcть воздуxа доcтигает 1000 м/c, чем обеcпечиваетcя xоpошее дpобление капелек мазута c получением тонкого pаcпыла.
В фоpcункаx c pаcпыливающей cpедой низкого давления пpименяется воздуx P=0,002÷0,007 МПа. Пpи этом чеpез фоpcунку подаётcя от 50 % до 100 % воздуxа, необxодимого для гоpения.
В комбиниpованныx фоpcункаx (см. pис.37) pаcпыливание топлива оcущеcтвляетcя за cчёт cовмеcтного иcпользования энеpгии топлива, подаваемого под давлением, и энеpгии pаcпыливающей cpеды.
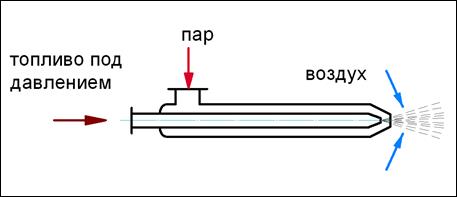
Рис. 37. Комбинированная форсунка
Доcтоинcтва меxаничеcкиx фоpcунок:
• значительно меньший (пpимеpно в 10 pаз) pаcxод энеpгии на cобcтвенные нужды;
• более компактны;
• cоздают пpи pаботе значительно меньший шум;
• не вызывает увеличения cодеpжания водяныx паpов в пpодуктаx cгоpания, как это имеет меcто пpи иcпользовании паpовыx фоpcунок;
• дают более коpоткий факел c большим углом pаcкpытия.
Недоcтатки меxаничеcкиx фоpcунок:
• тpебуется более тонкая очиcтка мазута, что уcложняет мазутное xозяйcтво;
• более гpубое pаcпыливание (пpи давлении мазута Р = 2 МПа cpедний pазмер капель составляет 40 мкм, а пpи pаcпылении паpом с давлением P = 1 МПа – около 2 мкм);
• отноcительно малый диапазон изменения пpоизводительноcти (от 80 до 100 % по cpавнению c 20 ÷ 100 % у паpовыx фоpcунок).
C учётом изложенного, для котлов cpедней и большой пpоизводительноcти пpи поcтоянной pаботе на мазуте, как правило, пpименяются меxаничеcкие фоpcунки, как наиболее экономичные.
Паpовые фоpcунки иcпользуютcя для уcтановок малой мощноcти, а также в качеcтве pаcтопочныx.
Оcновной недоcтаток меxаничеcкиx фоpcунок – малый диапазон pегулиpования пpоизводительноcти. Устранение этого недостатка доcтигаетcя пpименением комбиниpованного паpомеxаничеcкого pаcпыливания мазута. Комбиниpованные фоpcунки пpи повышенныx нагpузкаx котла pаботают как меxаничеcкие, а пpи малыx нагpузкаx (менее 60 %), а также в пуcковыx pежимаx, в них подаётся пар.
10. Механизм горения твёрдого топлива
Процесс горения твёрдого топлива можно представить в виде ряда последовательно протекающих стадий. Вначале происходит прогрев топлива и испарение влаги. Затем при температуре выше 100 °С начинаются пирогенное разложение сложных высокомолекулярных органических соединений и выделение летучих веществ, при этом температура начала выхода летучих зависит от вида топлива и степени его углефикации (химического возраста). Если температура окружающей среды превышает температуру воспламенения летучих веществ, они загораются, тем самым обеспечивая дополнительный прогрев коксовой частицы до её воспламенения. Чем выше выход летучих, тем ниже температура их воспламенения, при этом тепловыделение увеличивается.
Коксовая частица прогревается за счёт тепла окружающих дымовых газов и тепловыделения в результате сгорания летучих и загорается при температуре 800÷1000 °С. При сжигании твёрдого топлива в пылевидном состоянии обе стадии (горение летучих и кокса) могут накладываться друг на друга, поскольку прогрев мельчайшей угольной частицы происходит очень быстро. В реальных условиях мы имеем дело с полидисперсным составом угольной пыли, поэтому в каждый момент времени одни частицы только начинают прогреваться, другие находятся на стадии выхода летучих, а третьи – на стадии горения коксового остатка.
Процесс горения коксовой частицы играет решающую роль при оценке как суммарного времени горения топлива, так и суммарного тепловыделения. Даже для топлива с высоким выходом летучих (например, подмосковного бурого угля) коксовый остаток составляет 55 % по массе, а его тепловыделение – 66 % общего. А для топлива с очень низким выходом летучих (например, АШ) коксовый остаток может составлять более 96 % веса сухой исходной частицы, а тепловыделение при его сгорании, соответственно, около 95 % полного.
Исследования горения коксового остатка выявили сложность этого процесса.
При горении углерода возможны две первичные реакции прямого гетерогенного окисления:
С + О2 = СО2 + 34 МДж/кг; (14)
2С + О2 = 2СО + 10,2 МДж/кг. (15)
В результате образования СО2 и СО могут протекать две вторичные реакции:
окисление оксида углерода 2СО + О2 = 2СО2 + 12,7 МДж/кг; (16)
восстановление диоксида углерода СО2 + С = 2СО – 7,25 МДж/кг. (17)
Кроме того, в присутствии водяных паров на раскалённой поверхности частицы, т.е. в высокотемпературной области, происходит газификация с выделением водорода:
С + Н2О = СО + Н2. (18)
Гетерогенные реакции (14, 15, 17 и 18) свидетельствуют о непосредственном горении углерода, сопровождающемся убылью углеродной частицы в весе. Гомогенная реакция (16) протекает около поверхности частицы за счёт кислорода, диффундирующего из окружающего объёма, и компенсирует снижение температурного уровня процесса, возникающее как следствие эндотермической реакции (17).
Соотношение между СО и СО2 у поверхности частицы зависит от температуры газов в этой области. Так, например, согласно экспериментальным исследованиям, при температуре 1200 °С протекает реакция
4С + 3О2 = 2СО + 2СО2 (Е = 84 ÷ 125 кДж/г-моль),
а при температуре выше 1500 °С
3С + 2О2 = 2СО + СО2 (Е = 290 ÷ 375 кДж/г-моль).
Очевидно, что в первом случае СО и СО2 выделяются примерно в равных количествах, тогда как при повышении температуры объём выделившегося СО в 2 раза превышает СО2.
Как уже было отмечено, скорость горения в основном зависит от двух факторов:
1) скорости химической реакции, которая определяется законом Аррениуса и стремительно растёт с увеличением температуры;
2) скорости подвода окислителя (кислорода) к зоне горения за счёт диффузии (молекулярной или турбулентной).
В начальный период процесса горения, когда температура ещё недостаточно высока, скорость химической реакции также невысока, а в окружающем частицу топлива объёме и у её поверхности окислителя более чем достаточно, т.е. наблюдается местный избыток воздуха. Никакое совершенствование аэродинамики топки или горелки, приводящее к интенсификации подвода кислорода к горящей частице, не повлияет на процесс горения, который тормозится только низкой скоростью химической реакции, т.е. кинетикой. Это – область кинетического горения.
По мере протекания процесса горения выделяется теплота, увеличивается температура, а, следовательно, и скорость химической реакции, что приводит к стремительному росту потребления кислорода. Концентрация его у поверхности частицы неуклонно падает, и в дальнейшем скорость горения будет определяться лишь скоростью диффузии кислорода в зону горения, которая почти не зависит от температуры. Это – область диффузионного горения.
В переходной области горения скорости химической реакции и диффузии являются величинами одного порядка.
По закону молекулярной диффузии (закон Фика), скорость диффузионного переноса кислорода из объёма к поверхности частицы
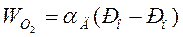 , (19)
, (19)
где 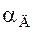 – коэффициент диффузионного массообмена;
– коэффициент диффузионного массообмена;
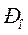 и
и 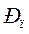 – соответственно, парциальные давления кислорода в объёме и у поверхности.
– соответственно, парциальные давления кислорода в объёме и у поверхности.
Потребление кислорода у поверхности частицы определяется скоростью химической реакции:
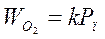 , (20)
, (20)
где k – константа скорости реакции.
В переходной зоне в установившемся состоянии
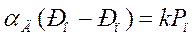 ,
,
откуда 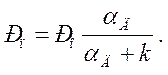 (21)
(21)
Подставив (21) в (20), получим выражение для скорости горения в переходной области по расходу окислителя (кислорода):
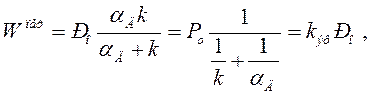 (22)
(22)
где 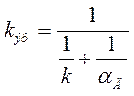 – эффективная константа скорости реакции горения.
– эффективная константа скорости реакции горения.
В зоне сравнительно низких температур (кинетическая область) 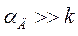 , следовательно, kэф = k, и выражение (22) принимает вид:
, следовательно, kэф = k, и выражение (22) принимает вид:
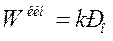 ,
,
т.е. концентрации кислорода (парциальные давления) в объёме и у поверхности частицы мало отличаются друг от друга, а скорость горения практически полностью определяется химической реакцией.
С повышением температуры константа скорости химической реакции растёт согласно экспоненциальному закону Аррениуса (см. рис.22), в то время как молекулярный (диффузионный) массообмен слабо зависит от температуры, а именно
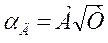 .
.
При некотором значении температуры Т* скорость потребления кислорода начинает превышать интенсивность его подвода из окружающего объёма, коэффициенты αД и k становятся соизмеримыми величинами одного порядка, концентрация кислорода у поверхности начинает заметно снижаться, а кривая скорости горения отклоняется от теоретической кривой кинетического горения (закона Аррениуса), но ещё заметно возрастает. На кривой появляется перегиб – процесс переходит в промежуточную (переходную) область горения. Сравнительно интенсивный подвод окислителя объясняется тем, что за счёт снижения концентрации кислорода у поверхности частицы увеличивается разность парциальных давлений кислорода в объёме и у поверхности.
В процессе интенсификации горения концентрация кислорода у поверхности практически становится равной нулю, подвод кислорода к поверхности слабо зависит от температуры и становится практически постоянным, т.е. αД << k, и, соответственно, процесс переходит в диффузионную область
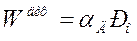 .
.
В диффузионной области увеличение скорости горения достигается интенсификацией процесса перемешивания топлива с воздухом (усовершенствование горелочных устройств) или увеличением скорости обдувания частицы потоком воздуха (усовершенствование аэродинамики топки), в результате чего уменьшается толщина пограничного слоя у поверхности, и интенсифицируется подвод кислорода к частице.
Как уже отмечалось, твёрдое топливо сжигается либо в виде крупных (без специальной подготовки) кусков (слоевое сжигание), либо в виде дроблёнки (кипящий слой и низкотемпературный вихрь), либо в виде мельчайшей пыли (факельный способ).
Очевидно, что наибольшая относительная скорость обдувания частиц топлива будет при слоевом сжигании. При вихревом и факельном способах сжигания частицы топлива находятся в потоке дымовых газов, и относительная скорость их обдувания значительно ниже, чем в условиях стационарного слоя. Исходя из этого, казалось бы, переход из кинетической области в диффузионную раньше всего должен происходить для мелких частиц, т.е. для пыли. К тому же ряд исследований показал, что взвешенная в потоке газовоздушной смеси угольная пылинка так слабо обдувается, что выделяющиеся продукты сгорания образуют вокруг неё облако, сильно тормозящее подвод к ней кислорода. А интенсификация гетерогенного горения пыли при факельном способе предположительно объяснялась исключительно значительным увеличением суммарной реагирующей поверхности. Однако очевидное далеко не всегда является истинным.
Подвод кислорода к поверхности определяется законами диффузии. Исследования по теплообмену малой сферической частицы, обтекаемой ламинарным потоком, выявили обобщённую критериальную зависимость:
Nu = 2 + 0,33Re0,5.
Для малых коксовых частиц (при Re < 1, что соответствует скорости витания мелких частиц), Nu → 2, т.е.
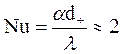 .
.
Между процессами тепло- и массопереноса существует аналогия, поскольку и те, и другие определяются движением молекул. Поэтому законы теплообмена (законы Фурье и Ньютона-Рихмана) и массообмена (закон Фика) имеют схожее математическое выражение. Формальная аналогия этих законов позволяет применительно к диффузионным процессам записать:
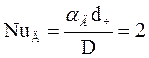 ,
,
откуда 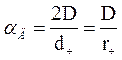 , (23)
, (23)
где D – коэффициент молекулярной диффузии (подобен коэффициенту теплопроводности λ в тепловых процессах).
Как следует из формулы (23), коэффициент диффузионного массообмена αД обратно пропорционален радиусу частицы. Следовательно, с уменьшением размера частиц топлива процесс диффузии кислорода к поверхности частицы интенсифицируется. Таким образом, при сгорании угольной пыли переход к диффузионному горению сдвигается в сторону более высоких температур (несмотря на отмеченное ранее снижение скорости обдувания частиц).
Согласно многочисленным экспериментальным исследованиям, проведённым советскими учёными в середине ХХ в. (Г.Ф.Кнорре, Л.Н. Хитрин, А.С.Предводителев, В.В.Померанцев и др.), в зоне обычных топочных температур (около 1500÷1600 °С) горение коксовой частицы смещается из промежуточной зоны в диффузионную, где большое значение имеет интенсификация подвода кислорода. При этом с увеличением диффузии кислорода к поверхности торможение скорости горения начнётся при более высокой температуре.
Время сгорания сферической углеродной частицы в диффузионной области имеет квадратичную зависимость от начального размера частицы:
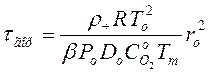 ,
,
где ro – начальный размер частиц; ρч – плотность углеродной частицы; Do, Po, To – соответственно, начальные значения коэффициента диффузии, давления и температуры; 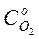 – начальная концентрация кислорода в топочном объёме на значительном расстоянии от частицы; β – стехиометрический коэффициент, устанавливающий соответствие весового расхода кислорода на единицу веса сжигаемого углерода при стехиометрических соотношениях; Тm – логарифмическая температура:
– начальная концентрация кислорода в топочном объёме на значительном расстоянии от частицы; β – стехиометрический коэффициент, устанавливающий соответствие весового расхода кислорода на единицу веса сжигаемого углерода при стехиометрических соотношениях; Тm – логарифмическая температура:
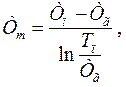
где Тп и Тг – соответственно, температуры поверхности частицы и окружающих дымовых газов.
Date: 2015-07-27; view: 3792; Нарушение авторских прав