
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Электронные конфигурации
|
|
Наша задача - разобраться в том, как заполняются электронные уровни, и как меняются при этом свойства атома по мере его усложнения.
Состояние отдельного электрона в атоме характеризуется четырьмя квантовыми числами: 
1. главным квантовым числом n = 1, 2, 3,...;
2. орбитальным квантовым числом l = 0, 1,...n-1;
3. магнитным квантовым числом ml = -1, -1+1,...l-1 (всего 2l+1 значений);
4. проекцией спина ms = +1/2, -1/2;
Порядок заполнения электронных состояний определяется двумя принципами:
· принцип Паули: в атоме может быть только один электрон с данным набором квантовых чисел;
· принцип минимума энергии: в основном состоянии атома электрон занимает квантовое состояние с наинизшей возможной энергией. Следует учесть, что вследствие взаимодействия электронов друг с другом значения энергии зависят не только от главного квантового числа n, но и от орбитального l.
Совокупность электронов атома с заданным значением главного квантового числа n образует электронную оболочку атома (эти электроны объединяют близкие значения энергии и средняя удаленность от ядра; из последнего родилось и название). В водородоподобных атомах наиболее вероятное удаление от ядра зависит от n следующим образом
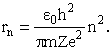
Различные оболочки атома обозначаются буквами: K (n=1), L (n=2), M (n=3),... Значение орбитального квантового числа принято обозначать буквами:
| Значение орбитального квантового числа | ... | ||||
| Название состояния | s | p | d | f | ... |
Запись, указывающая оболочку, значение орбитального числа и количество электронов в оболочке, называется электронной конфигурацией атома. Сначала указывают главное квантовое число, затем название состояния по орбитальному числу (s, p, d и т.д.) и в виде степени у символа число электронов в этом состоянии. Например, 1s22s22p3 означает: 2 электрона имеют n = 1, l = 0, для следующих двух n = 2, l = 0, и последние три электрона находятся в состоянии с n = 2, l = 1. Это электронная конфигурация атома азота.
Порядок заполнения электронных состояний определяется двумя принципами:
- принцип Паули, который гласит: в атоме не может быть двух электронов, все квантовые числа которых равны друг другу;
- принцип минимума энергии - при данном количестве электронов в атоме реализуется состояние с наименьшей энергией;
Максимальное число электронов в оболочке с заданным значением n находим суммированием
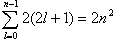
В водородоподобных атомах с одним электроном без учета спина энергия электрона зависит только от главного квантового числа n
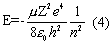 .
.
В многоэлектронных атомах существено и взаимодействие электронов друг с другом. Расчеты показывают, что при данном n энергия электронов увеличивается с увеличением орбитального квантового числа l (образно говоря, центробежная сила, возникающая при орбитальном движении, стремится удалить электрон от ядра). По этой причине энергия электронов в 4s -состоянии оказывается меньше, чем в 3d -состоянии, и с 19 K начинается заполнение состояний с n = 4, хотя не все состояния с n = 3 заняты. В итоге получаем следующую картину:
| 1s2 | 2 электрона |
| 2s22p6 | 8 электронов |
| 3s23p6 | 8 электронов |
| 4s23d104p6 | 18 электронов |
| 5s24d105p6 | 18 электронов |
| ... | ... |
Вы можете потренироваться в заполнении электронных оболочек с помощью действующей компьютерной модели.
Можно также посмотреть, как выглядят пространственные распределения электронной плотности в различных состояниях (ссылка на источник здесь). Сколь причудливы и сложны эти распределения.
Date: 2015-07-22; view: 503; Нарушение авторских прав