
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Декабоксилирование
|
|
А ОРНИТИН в состав белков не входит, но обязательно содержится в организме
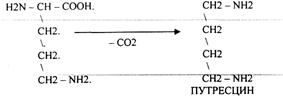
В. ЛИЗИН
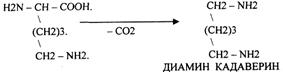
Путресцин и Кадаверин являются токсическими веществами. Они входят в состав
трупных ядов.
4.Распад боковой цепи циклических аминокислот.
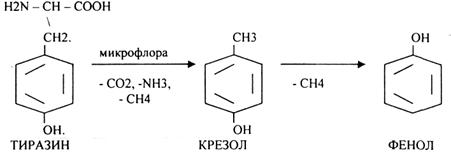
триптофан 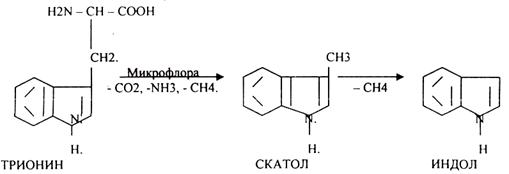
Роль белков в питании. Превращение белков в органах пищеварительной системы. Роль соляной кислоты в переваривании белков. Характеристика протеолитических ферментов пищеварительного тракта.
Белки поступают в организм человека с продуктами животного и растительного происхождения. Взрослый человек должен употреблять в сутки около 100 г белка, ребенок до 10 лет 50-70 г белка. Синтез обновленного белка происходит из аминокислот, которые образуются при распаде.
Все АК можно разделить на 4 группы:
1.Заменимые - синтезируются в организме: АЛА, АСП, АСН, ГЛУ, ГЛН, ГЛИ, ПРО, СЕР.
2.Незаменимые - не синтезируются в организме и поступают с пищей: ВАЛ, ЛЕЙ, ИЛЕ. ЛИЗ. ТРЕ, МЕТ, ФЕН, ТРИ.
3.Частично заменимые - синтезируются в организме, но очень медленно и не покрывают всех потребностей организма: ГИС, АРГ.
4.Условно заменимые - синтезируются из незаменимых аминокислот: ЦИС (МЕТ), ТИР (ФЕН). Питательная ценность белка определяется:
1. Наличием всех незаменимых аминокислот. Отсутствие даже одной незаменимой аминокислоты нарушает биосинтез белка, т.е. каждая незаменимая АК может быть лимитирующей в процессе синтеза белка.
2. Способность усваиваться организмом, доступность действию протеаз.
). В ротовой полости белки не подвергаются каким-либо химическим превращениям, т.к. здесь отсутствуют ферменты, действующие на белки. В желудке начинается химическое превращение белков. Здесь действуют два основных фермента:
Пепсин вырабатывается главными клетками слизистой желудка в неактивной форме - пепсиноген, который под действием соляной кислоты активируется и превращается в пепсин. Процесс активации является аутокаталитическим. От пептидной цепи неактивного пепсиногена со стороны N-конца отрывается один пептид, содержащий 42 аминокислоты - активация путём частичного протеолиза. Затем из остатка цепи формируется новая трёхмерная структура фермента - пепсина и новый активный центр.
Внутренние пептидные связи становятся доступными для действия пепсина, способствует продвижению желудочного содержимого далее в кишечник. Гастриксин по действию аналогичен пепсину. Это тоже эндопептидаза. Его оптимум рН = 3 - 3,5. Действует на пептидные связи, в образовании которых участвуют дикарбоновые аминокислоты (ГЛУ, АСП) своими карбоксильными группами. В желудке под действием пепсина и гастриксина сложные белковые молекулы распадаются на высокомолекулярные полипептиды, которые поступают в тонкую кишку. В ней полипептиды подвергаются действию целого ряда протеолитических ферментов, которые вырабатываются в неактивной форме: трипсиноген, химотрипсиноген, проэластаза, прокарбоксипептидаза.
Соляная кислота вырабатывается обкладочными клетками слизистой желудка и играет очень важную роль в переваривании белков:
Ø активирует пепсиноген, превращая его в пепсин,
Ø создаёт оптимум рН для действия пепсина (1,5 - 2),
Ø обладает бактерицидным действием,
Ø способствует продвижени. Желудочного содержимого в кишечник,
Ø денатурирует белки, которые потом гидролизуются.
Кислотность желудочного сока измеряется в титрационных единицах ТЕ – то количество мл NaOH, которое затрачено на титрование 100 мл желудочного сока в присутствии индикатора.
20.Цитратный цикл, его биологическое значение, последовательность реакций. Сопряжение реакций цикла трикарбоновых кислот с дыхательной цепью ферментов.
В цикле КРЕБСА АЦЕТИЛ-КОА распадается до СО2 с образованием восстановленных КОФЕРМЕНТОВ - НАДН
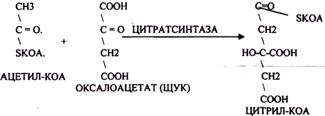
АТФ в реакции не участвует, а используется энергия макроэргической связи АЦЕТИЛ-КОА ЦИТРИЛ-КОА не устойчив и очень быстро распадается под влиянием воды.
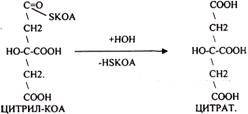
Лимонная кислота далее превращается в свой изомер (ИЗОЦИТРАТ) под влиянием фермента АКОНИТАЗЫ.
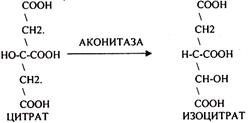
ИЗОЦИТРАТ подвергается далее ДЕГИДРИРОВАНИЮ под влиянием фермента -ИЗОЦИТРАТДЕГИДРОГЕНАЗЫ.
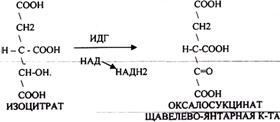
ЩЯВЕЛЕВО-ЯНТАРНАЯ К-ТА (а-кетоглутарат) подвергается ДЕКАРБОКСИЛИРОВАНИЮ достаточно легко и не требует участия дополнительных ферментов - ПРЯМОЕ ДЕКАРБОКСИЛИРОВАНИЕ.
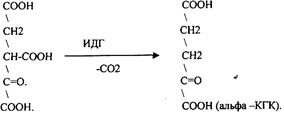

СУКЦИНИЛ-КОА подвергается реакции субстратного ФОСФОРИЛИРОВАНИЯ.
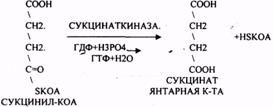
ГТФ + АДФ = ГДФ + АТФ
ФУНКЦИИ ЦТК.
1.Катаболическая - распад АЦЕТИЛ КоА до Н2О и СО2
2.Анаболическая. Компоненты ЦТК могут использоваться для синтеза др. соединений
ЩУК - синтез АСП, МАЛAT - синтез глюкозы и т.д.
3.Интегративная. Взаимосвязь обмена БЖУ.
4.Энергетическая. Образование 1 молекулы АТФ. Если ЦТК работает вместе с дыхательной цепью, то образуется ещё 1 молекул АТФ.
5.ВОДОРОДГЕНЕРИРУЮЩАЯ - в результате ЦТК образуется 3 молекулы НАДН2 и 1 молекула ФАДН2, т.е. 4 пары молекул водорода. Они транспортируются в ЦТЭ.
ИЗОЦИТРАТ подвергается далее ДЕГИДРИРОВАНИЮ под влиянием фермента -ИЗОЦИТРАТДЕГИДРОГЕНАЗЫ.
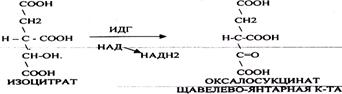
a-КГК подвергается реакции ОКИСЛИТЕЛЬНОГО ДЕКАРБОКСИЛИРОВАНИЯ, катализируемой комплексом ферментов (КЕТОГЛУТАРАТДЕГИДРОГЕНАЗНЫЙ комплекс), включающий 3 фермента и 5 КОФЕРМЕНТОВ.

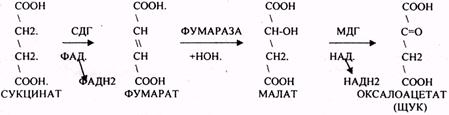
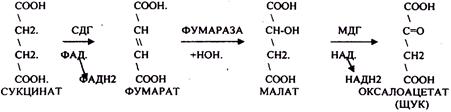
СУКЦИНАТ превращается в фумарат, малат в ЩУК
19. Пути синтеза АТФ в клетках, клеточная локализация процессов синтеза АТФ, примеры реакций. Молекулярные механизмы окислительного фосфорилирования (теория Митчелла).АТФ синтезируется в митохондриях в несколько этапов. Первый из них - подготовительный - протекает ступенчато, с вовлечением на каждой ступени специфических ферментов. При этом сложные органические соединения расщепляются до мономеров: белки - до аминокислот, углеводы - до глюкозы, нуклеиновые кислоты - до нуклеотидов и т. д. Разрыв связей в этих веществах сопровождается выделением небольшого количества энергии. Образовавшиеся мономеры под действием других ферментов могут претерпеть дальнейший распад с образованием более простых веществ вплоть до диоксида углерода и воды.
Теория окислительного фосфорилирования Митчела 1961г – хемиосмотическая теория окислительного фосфорилирования. Основные положения:
ü Мембрана митохондрий непроницаема для протонов.
ü В процессе транспорта электронов и протонов образуется протонный потенциал.
ü Обратный транспорт протонов в матрикс сопряжен с образованием АТФ.
Перенос электронов по дыхательной цепи сопровождается выделением энергии, часть которой используется для транспорта протонов из матрикса в межмембранное пространство. В результате транспорта протонов на другую сторону мембраны формируется протонный электрохимический потенциал.
Date: 2015-07-22; view: 1484; Нарушение авторских прав