
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Методика проведения реакции разложения ГП ИПБ
|
|
В предварительно взвешенную трехгорлую круглодонную колбу (1) на 250 мл налить 50 мл растворителя ИПБ и медленно, постоянно перемешивая, в отверстие для термометра прикапать пипеткой на 0,2 мл мл (3 капли) концентрированной Н2SO4. Ртутный шарик термометра (3) должен касаться реакционной массы. Включить воду в обратном холодильнике (2) и мешалку (5). Далее следует нагреть содержимое колбы до необходимой температуры реакции. Приготовить стакан (на 200 мл) с холодной водопроводной водой. В делительную воронку (4) налить 50 мл оксидата (реакционной массы ГП ИПБ) и прикапать ее за 5 минут, при этом при повышении температуры реакционной массы выше заданного значения следует охладить реактор, добавляя в водяную баню из стакана холодную воду и вычерпывая стаканом горячую воду из нее, также можно временно отключать электроплитку от сети. После прикапывания ГП ИПБ делительную воронку следует перекрыть. В течение реакции следует через определенное время (таблица 3) отбирать пипеткой по 1 мл пробы через отверстие в колбе, закрытое термометром, для определения текущей концентрации ГП ИПБ до ее полного израсходования (С ГП ИПБ, % = 0)или до тех пор, пока С ГП ИПБ, % не будет оставаться постоянной в течение трех измерений.
При проведении эксперимента следует тщательно следить за тем, чтобы температура реакционной массы не изменялась!
8. Определить текущую процентную концентрацию ГП ИПБ в реакционной массе методом иодометрического титрования, описанном в пункте 6 для всех взятых проб.
9. Результаты титрования оформить в таблицу 4:
Таблица 4.
Результаты титрования
при определении процентного содержания ГП ИПБ.
| № пробы | Время реакции t, мин | Объем 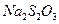 , мл , мл
| Концентрация ГП ИПБ, | ||
| a | b | С, % | с, моль/л | ||
| С '0 ГП ИПБ | |||||
| … | … |
Поскольку для кинетических расчетов следует перевести процентную концентрацию в молярную (моль/л) и учесть то, что при добавлении ГП ИПБ в растворитель ИПБ фактическая начальная концентрация ГП ИПБ уменьшается, необходимо вывести формулу для пересчета концентрации ГП ИПБ.
Вывод формулы пересчета процентной концентрации ГП ИПБ в молярную с учетом разбавления ИПБ
1. Пусть в бутылке содержится С0 ГП ИПБ, %. Это означает, что С0 г ГП ИПБ содержится в 100 г раствора ГП ИПБ;
Для реакции взято 50 г раствора ГП ИПБ, поэтому в нем содержится (С0 ГП ИПБ /2) г ГП ИПБ.
2. Масса раствора после смешения с растворителем ИПБ:
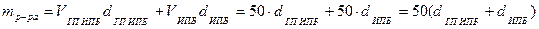 , г
, г
3. Процентная концентрация исходной ГП ИПБ С '0 ГП ИПБ после разбавления ИПБ находится из пропорции:
(С0 ГП ИПБ /2), г → 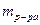 , г;
, г;
С '0 ГП ИПБ , г → 100 г р-ра.
С '0 ГП ИПБ , % = 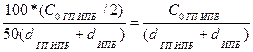 =
= 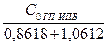 =
= 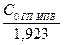
4. Расчет исходной мольной концентрации ГП ИПБ с, моль/л находится из пропорций:
(С0 ГП ИПБ /2), г ГП ИПБ → 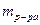 , г →
, г →  , мл =
, мл = 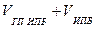 =100 мл
=100 мл
10 ∙ (С0 ГП ИПБ /2), г ГП ИПБ → 1000 мл = 1 л раствора.
1 моль ГП ИПБ → М (ГП ИПБ), г;
с моль ГП ИПБ → 10 ∙ (С0 ГП ИПБ /2), г ГП ИПБ
с = 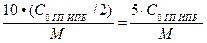 , моль/л
, моль/л
Текущая мольная концентрация с, моль/л находится из текущей процентной концентрации С, % по формуле:
с = 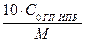 , моль/л
, моль/л
5. Провести обработку экспериментальных данных интегральным методом (заполнить таблицу 5).
Таблица 5.
Обработка экспериментальных данных разложения ГП ИПБ по интегральному методу
| № | t, мин | С, % | с, моль/л | 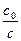
| 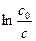
| k, 1/мин | n |
| … |
6. Построить график зависимости 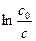 от t, мин. Определить константу скорости k, 1/мин и порядок реакции n. Результаты занести в таблицу.
от t, мин. Определить константу скорости k, 1/мин и порядок реакции n. Результаты занести в таблицу.
7. Провести обработку экспериментальных данных дифференциальным методом с помощью второго варианта. Заполнить таблицу 6.
Таблица 6.
Обработка экспериментальных данных разложения ГП ИПБ по дифференциальному методу (второй вариант)
С 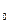 в бутылке, %
в бутылке, %
| t, мин | с, моль/л | lgс | φ | tgφ = r | lgr | lg k | k, 1/мин | γ | nt |
| … |
8. Построить графики зависимости с, моль/л от t, мин. и, затем, lgr от lgc. Определить значения k, 1/мин и nt.
9. После того, как были проведены все опыты, соответствующие номерам работ с 1 по 5 (таблица 1) следует приступить к полной обработке всех полученных результатов. Для этого следует на одном графике построить все пять зависимостей с, моль/л от t, мин. для различных параметров процесса, указав на графике для каждой зависимости значения С0, в бутылке,% и T, °C.
10. Провести обработку экспериментальных данных дифференциальным методом с помощью первого варианта. Следует учесть, что для заполнения таблицы берутся результаты работ с номерами с 1 по 3, соответствующие опытам с различной начальной концентрацией, но постоянной температурой. Заполнить таблицу 7.
Таблица 7.
Обработка экспериментальных данных разложения ГП ИПБ по дифференциальному методу (первый вариант)
С 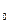 в бутылке, %
в бутылке, %
| с0, моль/л | lgс0 | φ | tgφ = r | lgr | lg k | k, 1/мин | γ | nс |
11. Построить графики зависимости с, моль/л от t, мин. для различных трех значений с0 и, затем, lgr от lgc0. Определить значения k, 1/мин и nс.
12. Сравнить значения nс и nt при одной и той же концентрации. Сделать вывод, опираясь на теоретические знания.
13. Заполнить таблицу 8, используя полученные результаты.
Таблица 8.
Зависимость k, 1/мин., nс и nt от с0, моль/л
С 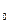 в бутылке, %
в бутылке, %
| с0, моль/л | k, 1/мин | nt | nс | T,°C |
Проанализировать как изменяется значения k, nс и nt c изменением концентрации исходной ГП ИПБ. Сформулировать выводы, опираясь на теоретические знания.
14. Заполнить таблицу 9, используя полученные результаты работ с 3 по 5 (таблица 1).
Таблица 9.
Обработка Зависимость k, 1/мин., nс и nt от с0, моль/л
| T,°C | k, 1/мин | nt | С 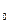 в бутылке, %
в бутылке, %
| с0, моль/л |
Проанализировать как изменяется значения k и nt c изменением температуры реакции. Сформулировать выводы, опираясь на теоретические знания.
15. Используя полученные результаты работ с 3 по 5 (таблица 1) рассчитать значения энергии активации по первому варианту. Расчеты привести в отчете. На основании расчетов заполнить таблицу 10.
Таблица 10.
Определение значения энергии активации Еа расчетным методом
| Т1,°С | Т2,°С | Т1,°С | Т2,°С | Т1,°С | Т2,°С | |
| Т,°С | ||||||
| Еа расч. |
Проанализировать изменяется ли расчетное значение Еа c изменением температуры реакции. Сформулировать выводы, опираясь на теоретические знания.
16. Используя полученные результаты работ с 3 по 5 (таблица 1) определить значения k0 энергии активации Еа по второму варианту, построив график зависимости lnk от 1/T.При построении графика использовать значения k, полученные интегральным методом. На основании расчетов заполнить таблицу 11.
Таблица 11.
Определение значения энергии активации Еа графическим методом
С 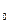 в бутылке, %
в бутылке, %
| с0, моль/л | Т,°С | Т, К | 1/Т∙104, 1/К | k, 1/мин | ln k | ln k0 | k0 | α | Еa |
Проанализировать изменяется ли графическое значение Еа c изменением температуры реакции. Сформулировать выводы, опираясь на теоретические знания. Cравнить значения энергии активации, полученные расчетным и графическим методами.
17. Рассчитать значение энтропии активации ∆S#, Дж/моль∙К. Расчет привести в отчете и результаты расчета занести в таблицу 12.
Таблица 12.
Определение значения энтропии активации ∆S#, Дж/моль∙К
С 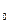 в бутылке, %
в бутылке, %
| с0, моль/л | Т,°С | Т, К | k0, 1/мин | k0, 1/c | χ | e∆S#/R | ∆S#, Дж/моль∙К |
Проанализировать изменяется ли значение ∆S# c изменением температуры реакции. Сформулировать выводы, опираясь на теоретические знания.
18. Заполнить итоговую таблицу 13.
Таблица 13.
Кинетические параметры реакции разложения ГП ИПБ
С 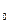 в
бутылке,
%
в
бутылке,
%
| Т, °С | lgс0 | k, 1/мин (интегр) | k, 1/мин (диф) (2 вар.) | k, 1/мин (диф) (1 вар.) | nс | nt | k0 | Еа, расч кДж/ моль | Еа, граф кДж/ моль | ∆S#, Дж/ моль∙К |
| ― | ― | ― | ― | ||||||||
| ― | ― | ― | ― | ||||||||
| * | |||||||||||
| ― | ― | ** | |||||||||
| ― | ― | *** |
* ― привести значение Еа при T1= 40°C и Т2 = 50°С.
** ― привести значение Еа при T1= 50°C и Т2 = 60°С.
***― привести значение Еа при T1= 40°C и Т2 = 60°С.
19. Оформить отчет, и сформулировать выводы по всем проделанным экспериментам
Date: 2015-07-24; view: 1286; Нарушение авторских прав