
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Кинетика химических реакций. Последовательные реакции
|
|
Кафедра химии
Лабораторная работа
по дисциплине «Физическая и коллоидная химия»
специальность
специализация
______________________________________________________________________
| Проверил | Выполнили |
| ______________________________ | студенты группы____________ |
| ______________________________ | |
| ______________________________ | |
| «____» ____________2014 г | «____»____________ 2014 г. |
Могилев 2014
1. Цель работы – познакомиться с основными закономерностями кинетики последовательных реакций.
2.Работа выполняется на ЭВМ по имеющейся программе.
3. Теоретическое введение.
В последовательных химических реакциях образующееся на первой стадии промежуточное вещество превращается затем в конечные продукты. В лабораторной работе рассматривается простейшая схема таких реакций, когда обе эти реакции необратимы и имеют первый порядок:
k1 k2
A → B → D. (1)
С0–x x–y y
Концентрация вещества A рассчитывается на ЭВМ по уравнению:
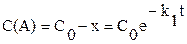 . (2)
. (2)
Концентрация вещества B рассчитывается на ЭВМ по уравнению:
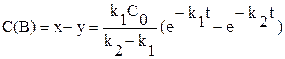 . (3)
. (3)
Концентрация вещества D рассчитывается по разности
C(D) = С0 – С(A) – C(B). (4)
Время достижения максимальной концентрации промежуточного вещества B рассчитывается на ЭВМ по уравнению:
 . (5)
. (5)
В основе рассмотрения кинетики сложных химических реакций лежит принцип независимости отдельных реакций. Принимается, что каждый элементарный процесс идет в соответствии со своим кинетическим уравнением, и его скорость зависит только от концентрации соответствующих реагирующих веществ. Присутствие других веществ и других реакций прямо не сказывается на скорости данной реакции, константа скорости также не изменяется.
Например, скорость первой реакции пропорциональна концентрации вещества А и не зависит от концентрации вещества В:
v1 = k1 CA. (6)
Концентрация вещества А с течением времени уменьшается, поэтому и скорость первой реакции dC(A)/dt также постепенно уменьшается.
Скорость второй реакции пропорциональна концентрации вещества В и не зависит от концентрации вещества D:
v2 = k2 CВ. (7)
Концентрация вещества В в начальный момент времени равна нулю, она также равна нулю после окончания этих реакций. Таким образом, концентрация промежуточного продукта B должна проходить через максимум.
В соответствии с уравнением (6) скорость образования вещества В должна постепенно уменьшаться; в то же время скорость его исчезновения по второй реакции должна, в соответствии с уравнением (7), постепенно возрастать. При равенстве этих скоростей получим dC(В)/dt = 0, т.е. скорость изменения концентрации вещества В делается равной нулю (в точке максимума концентрации В). Далее начинает преобладать вторая реакция, и скорость исчезновения В постепенно возрастает; затем, по мере расходования вещества В, скорость изменения концентрации вещества В уменьшается в соответствии с уравнением реакции (7).
Концентрация вещества D монотонно возрастает, при этом в начальном периоде, когда концентрация вещества B очень мала, наблюдается некоторый индукционный период; в соответствии с уравнением (7) скорость образования вещества D сначала возрастает, до достижения максимальной концентрации вещества В, а затем постепенно уменьшается.
4. Методика выполнения (ход работы).
В «Методических указаниях» [2] по двум последним цифрам номера зачетной книжки определяют исходные данные для расчетов на ЭВМ – начальную концентрацию исходного вещества С0, константы скорости последовательных реакций k1 и k2. Запускают на ЭВМ программу «kinetic2.exe» и выполняют работу в соответствии с указаниями, которые появляются на экране монитора.
5. Результаты работы.
Date: 2015-07-24; view: 707; Нарушение авторских прав