
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

А5. При повышении температуры на 30 °С (температурный коэффициент равен 3) скорость увеличится
|
|
Х–11 Контрольная работа №2 «Химические реакции» Вариант №1
| При выполнении заданий А1-А10 из предложенных вариантов ответов выберите тот, который вы считаете правильным. 2 балла за каждое верно выполненное задание. |
А1. Характеристика реакции, уравнение которой 4Fe + 6H2O + 3O2 →4Fe(OH)3:
1) Соединения, ОВР 2) Замещения ОВР 3) Обмена не ОВР 4) Разложения ОВР
А2. Какая масса угля вступает в реакцию, термохимическое уравнение которой С+О2 = СО2 + 402 кДж, если при этом выделилось 1608 кДж теплоты?
1) 4,8 г 2) 48 г 3) 120 г 4) 240 г
А3. Химическая реакция, уравнение которой: 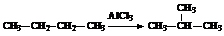
1) Дегидрирования 2) Изомеризации 3) Полимеризации 3) Присоединения
А4. Окислитель в реакции синтеза аммиака, уравнение которой N2 + 3H2 = 2NH3 + Q
1) N0 2) H0 3) H+1 4) N–3
А5. При повышении температуры на 30 °С (температурный коэффициент равен 3) скорость увеличится
1) в 3 раза 2) в 9 раз 3) в 27 раз 4) в 81 раз
А6. Факторы, позволяющие сместить химическое равновесие, для реакции CaO(т)+CO2(г)↔CaCO3(т)+Q, в сторону продуктов реакции:
1) Повышение температуры и понижение давления 2) Понижение температуры и давления
3) Понижение температуры и повышение давления 4) Повышение температуры и давления
А7. Щелочную среду имеет водный раствор соли, формула которой:
1) AlCl3 2) KNO3 3) K2CO3 4) FeCl3
А8. Наиболее сильной кислотой из перечисленных является:
1) H2CO3 2) H3PO4 3) H2SO4 4) H2SO3
А9. Осадок образуется при взаимодействии хлорида калия с:
1) AgNO3 2) NaOH 3) H2SO4 4) NaCl
А10. Гидролизу не подвергается:
1) ZnSO4 2) Ba(NO3)2 3) Na2S 4) NH4Cl
| В заданиях В1-В3 установите соответствие. Ответ запишите в виде последовательности цифр. 4 балла за верно выполненное задание. |
В1. Установите соответствие между схемой ОВР и коэффициентом перед формулой восстановителя:
| Схема реакции | Коэффициент |
| А) NH3 + CuO = Cu + N2 + H2O | 1) 2 |
| Б) NH3 + O2 = NO + H2O | 2) 6 |
| В) HNO3 + Cu = Cu(NO3)2 + NO2 + H2O | 3) 4 |
| Г) Li + N2 = L3N | 4) 1 |
| 5) 5 |
| А | Б | В | Г |
Date: 2015-07-22; view: 1437; Нарушение авторских прав