
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Н н н н н н
|
|
Н.хОх. Н
хх
Атоми зв′язані між собою двома ковалентними (рівносильними, двохелектро-нними, двохцентровими) полярними зв′язками:
хх
Нà O ß H
хх
Кисень більш електронегативний (сильніший) атом і відтягує електронну гус-тину зв′язків на себе, набуваючи при цьому частково негативного заряду (за-ряд електрона –). Атоми водню, збіднені електронами, набувають часткового позитивного заряду.
 +
+  –
–  +
+
H à O ß H 
Електростатичне відштовхування між однойменно зарядженими атомами, та наявність двох вільних пар електронів у атома кисню, обумовлює тетраедрич-ну будову молекул води в просторі, протилежні кінці якої заряджені різнойме-нно:
 Н
Н  +
+
 О
О  –
–

 .. Н
.. Н  +
+
(–)
..
(–)
Молекула – кінці якої мають протилежні заряди називається диполем.
Дипольний момент –кількісна характеристика полярності молекули, являє со-бою добуток величини зарядів на відстань між ними:
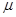 =
=  q L (D)
q L (D) 
Дипольна будова приводить до того, що молекули води об′єднуються між со-бою з утворенням асоціатів (рідини) за рахунок водневих зв′язків:
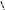




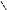
 Н—О ---Н: О—Н:О—Н:О—Н:О—Н:О—Н:О---Н
Н—О ---Н: О—Н:О—Н:О—Н:О—Н:О—Н:О---Н
Н Н Н Н Н Н
При цьому, хімічні властивості води залишаються незмінними (водневі зв′язки слабкі), а фізичні властивості змінюються дуже. Зокрема значно зростає розчи-нююча здатність води. Взаємодіючи з молекулами інших полярних речовин во-да гідратує їх, розриваючи внутрішньомолекулярні зв′язки:
t = 14000 C
 NaCI Na+ + CI --
NaCI Na+ + CI --
 NaCI t=20 C H2O Na+ + CI --
NaCI t=20 C H2O Na+ + CI --
Процес розпаду речовин на іони під впливом розчинника називається дисоціа-цією.
Date: 2015-07-01; view: 449; Нарушение авторских прав