
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Етапи вивільнення енергії в катаболічних шляхах обміну біомолекул
|
|
Пластичний обмін в організмі відбувається в декілька стадій. Синтез біологічно активних сполук починається з піровиноградної кислоти, ацетил–КоА, проміжних продуктів циклу лимонної кислоти. Із цих попередників утворюються різноманітні макромолекули. Перетворення білків, ліпідів і вуглеводів складають центральні метаболічні шляхи з великим потоком метаболітів. Окрім них, проходять інші метаболічні перетворення, при цьому утворюється менший об’єм метаболітів. Ці шляхи становлять вторинний метаболізм. Відбувається синтез коферментів, гормонів, медіаторів, пігментів.
Обмін речовин в організмі безперервно пов’язаний з обміном і перетворенням енергії. Обмін енергії включає процеси: звільнення, трансформації та використання енергії, яка утворюється при розпаді певних речовин в організмі. Кожна органічна речовина, яка входить до складу живої матерії, має запас потенціальної енергії, за рахунок якої може бути здійснена робота.
Речовини піддаються в організмі поступовому перетворенню і окисненню із вивільненням енергії, яка запасається в макроергічних зв`язках АТФ. Енергія заключена основним чином в електронах водню і її вивільнення можна розбити на три етапи (фази) (рис.2.1).
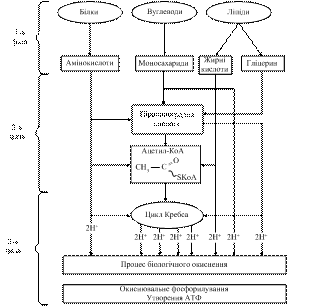
Рис.2.1. Схема загальних шляхів катаболізму біомолекул
Перший етап, підготовчий. В цій фазі високомолекулярні сполуки, які поступають із їжею, в травному тракті, а також у клітинах організму перетворюються на прості сполуки. На цьому етапі в основному діють ферменти гідролази і вивільняється приблизно до 1% енергії субстратів, яка розсіюється у вигляді тепла.
На другому етапі мономери розпадаються в клітинах тканин і органів на більш прості сполуки, такі як, наприклад, піровиноградна, лимонна, ізолимонна, α-кетоглутарова, янтарна, яблучна, оксалоацетатна, ацетатна кислоти, амінокислоти перетворюються на ацетил-КоА.
На цьому етапі в анаеробних умовах звільняється приблизно 25-30 % енергії вихідної речовини. Частина цієї енергії акумулюється у вигляді макроергічних зв`язків (субстратне фосфорилування), а частина розсіюється у вигляді тепла. Перетворення мономерів проходить в гіалоплазмі, а кінцеві реакції - в мітохондріях.
Третій етап - кінцевий розпад речовин до СО2 і Н2О з участю кисню із повним вивільненням енергії. Звільнений водень в складі своїх перенощиків під дією ферментів тканинного дихання розділяється на Н+ і електрон (ē). Електрон, переходить на більш низьку орбіталь кисню, активує його, з`єднується з протонами, утворює воду, а енергія, яка звільняється, акумулюється в молекулах АТФ. В утворенні цієї енергії приймає участь АДФ, фосфат та фермент АТФ -синтетаза.
Приблизно 70-80 % усієї енергії хімічних сполук виділяється в цій фазі. Всі реакції цієї фази локалізовані в мітохондріях.
2.4. Основні високоенергетичні сполуки. Центральна роль АТФ в біоенергетиці
У людини і тварин основними макроергічними сполуками є фосфор- і сірковмісні речовини. Одним із представників є АТФ:
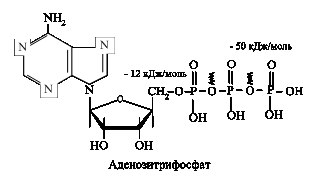 Енергія виділена при гідролізі одного макроергічного зв`язку АТФ, в залежності від локалізації може змінюватися від 40 до 60 кДж/моль, в середньому прийнято рахувати, що вона дорівнює 50 кДж/моль. АТФ є термодинамічно нестійкою молекулою і при гідролізі утворюється АДФ або АМФ і залишки фосфатів.
Енергія виділена при гідролізі одного макроергічного зв`язку АТФ, в залежності від локалізації може змінюватися від 40 до 60 кДж/моль, в середньому прийнято рахувати, що вона дорівнює 50 кДж/моль. АТФ є термодинамічно нестійкою молекулою і при гідролізі утворюється АДФ або АМФ і залишки фосфатів.
АТФ забезпечує енергією практично всі процеси життєдіяльності організму. До макроергічних сполук відносяться ГТФ, ЦТФ, УТФ ТТФ.
Основний шлях синтезу АТФ - це біологічне окиснення, спряжене з процесом фосфорилування, що проходить в мітохондріях.
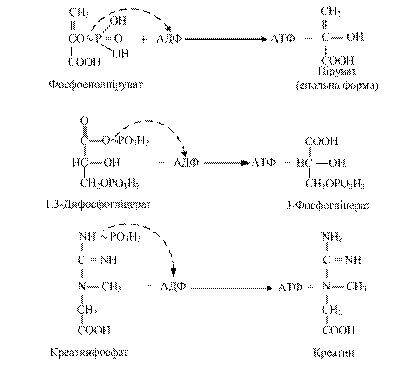
Другий шлях синтезу АТФ із АДФ - субстратне фосфорилування, яке локалізоване в цитоплазмі. Енергія цього процесу разом із залишком фосфорної кислоти переноситься на АДФ з утворенням АТФ. В процесі субстратного фосфорилування використовуються високоергічні сполуки – 2-фосфоенолпіровиноградна кислота, 1,3-дифосфогліцеринова кислота і креатинфосфат.
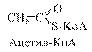
|
Крім фосфатних похідних, є тіоефірні сполуки, які мають макроенергічні зв`язки, що утворюються в процесі активації молекул різних кислот, в тому числі оцтової кислоти при участі коферменту ацетилювання, який позначається КоА-SН (КоА-кофермент ацетилювання, а SH - функціональна група).
Ацетил-КоА включається в цикл Кребса. При розриві тіоефірного зв`язку виділяється в середньому 33,6 кДж/моль енергії.
2.5. Лимоннокислий цикл (цикл дикарбонових і трикарбонових кислот)
Двовуглецеві фрагменти у вигляді СН3СО~SКоА, що утворюються в процесі обміну вуглеводів, жирів і азотистих сполук, перетворюються за так званим лимоннокислим циклом або циклом дикарбонових і трикарбонових кислот.
Вважають, що цикл дикарбонових і трикарбонових кислот є найвірогіднішим шляхом окиснювального перетворення проміжних продуктів розщеплення органічних сполук. Внаслідок цього складного процесу в клітинах весь час утворюються і перетворюються одна в одну ряд три- та дикарбонових кислот, звідки походить і назва циклу- цикл ди- і трикарбонових кислот. Можливість окиснення органічних сполук за допомогою такого механізму вперше довів Кребс, у зв'язку з чим цикл має ще назву циклу Кребса.
Коли говорять про цикл трикарбонових кислот як про загальний окиснювальний шлях органічних сполук, то це не означає, що до цього не відбувалось окиснення органічних сполук. Так, вуглеводи до включення в цикл трикарбонових кислот проходять дві стадії окиснення, а саме:
1) В анаеробних умовах у реакціях гліколізу з 3-фосфогліцеринальдегіду утворюється 3-фосфогліцеринова кислота.
2) В аеробних умовах внаслідок окиснювального декарбоксилювання з піровиноградної кислоти утворюється ацетил~КоА.
Жири при перетворенні жирних кислот на ацетил-КоА також проходять дві стадії окиснення:
1) Жирна кислота® a,b-ненасичені жирні кислоти;
2) (b-окси) жирна кислота ® (b-кето) жирна кислота.
Утворений з нейтральних жирів гліцерин зазнає ще одного окиснювального перетворення:
a-гліцерофосфат ® тріозофосфат.
Утворений тріозофосфат вступає в загальний процес використання вуглеводів.
Амінокислоти також перш ніж вступити в цикл трикарбонових кислот, повинні включитися в реакції переамінування або ж окиснювального декарбоксилювання, а потім внаслідок відповідних реакцій також утворити СН3СО~SКоА.
Внаслідок таких перетворень вуглеводів, ліпідів і азотистих сполук утворюється активний ацетил у вигляді СН3СО~SКоА, який є загальним продуктом метаболізму цих органічних сполук. Досить сказати, що 2/3 атомів вуглецю вуглеводів і всі атоми вуглецю жирних кислот, а також приблизно половина атомів вуглецю амінокислот проходять через стадію утворення ацетил-КоА. Підраховано, що при добовій нормі харчування людини, яка складається з 400 г вуглеводів, 70 г жирів і 100 г білків, в її організмі щодоби утворюється 350—400 г ацетил-КоА.
На шляху перетворення органічних сполук до утворення ацетил~КоА використовується лише невелика частина вільної енергії харчових речовин. У процесі гліколізу, наприклад, на шляху від глюкози до молочної кислоти витрачається всього близько 5-7 % вільної енергії вуглеводів.
Так, якщо зміна вільної енергії при повному окисненні глюкози становить-686 ккал/моль, то на шляху перетворення глюкози до двох молекул молочної кислоти витрачається лише -50 ккал/моль або близько 7 %, а на шляху перетворення від однієї молекули піровиноградної кислоти до однієї молекули ацетил-КоА ця енергія становить -60 ккал/моль, тобто близько 9 %.
Значно вищою є зміна енергії на шляху перетворення від однієї молекули пальмітинової кислоти до восьми молекул ацетил-КоА, яка становить-679 ккал/моль, тобто близько 30 % від зміни вільної енергії при повному окисненні пальмітинової кислоти.
Процес повного окиснення ацетил-КоА до СО2 і Н2О відбувається за допомогою циклу дикарбонових і трикарбонових кислот, який має основне значення в утворенні енергії в живих організмах. Як і процеси окиснення жирних кислот, цикл Кребса локалізований у мітохондріях, які, таким чином, є енергетичним центром живих клітин.
Сумарна реакція окиснення ацетил-КоА, пов'язана з виділенням великої кількості енергії (-207 ккал/моль), проходить в організмі через ряд проміжних реакцій за участю великої кількості ферментів і є багатоступінчастим процесом. Цикл Кребса є головним шляхом кінцевих перетворень ацетил-КоА; тільки незначна частина його витрачається на ацетилювання холіну, ароматичних амінів та інших побічних продуктів обміну. Більша частина СН3СО~SКоА вступає в реакцію з оксалоацетатом, починаючи цим самим цикл трикарбонових кислот.
Оксалоацетат у циклі трикарбонових кислот відіграє істотну роль. Він може утворюватися при перетворенні різних органічних субстратів: при окисненні яблучної кислоти, при окиснювальному дезамінуванні аспарагінової кислоти, при карбоксилюванні піровиноградної кислоти. Проте основним джерелом його утворення є процес конденсації піровиноградної кислоти з СО2.
Утворений цим або іншим способом оксалоацетат вступає в реакцію з ацетил-КоА за участю ензиму цитратсинтази, утворюючи лимонну кислоту, яка є, таким чином, початковою речовиною циклу дикарбонових і трикарбонових кислот, звідки цей цикл дістав назву лимоннокислого циклу, або циклу лимонної кислоти (рис.2.2).
Лимонна кислота перетворюється через цис-аконітову кислоту в ізолимонну.
Реакція каталізується ферментом аконітатгідратазою. Утворена ізолимонна кислота під дією ферменту ізоцитратдегідрогенази окиснюється, внаслідок цього утворюються НАДН2 і оксалосукцинат:
Утворений оксалосукцинат у результаті декарбоксилювання в присутності цього ж ферменту перетворюється в a-кетоглутарову.
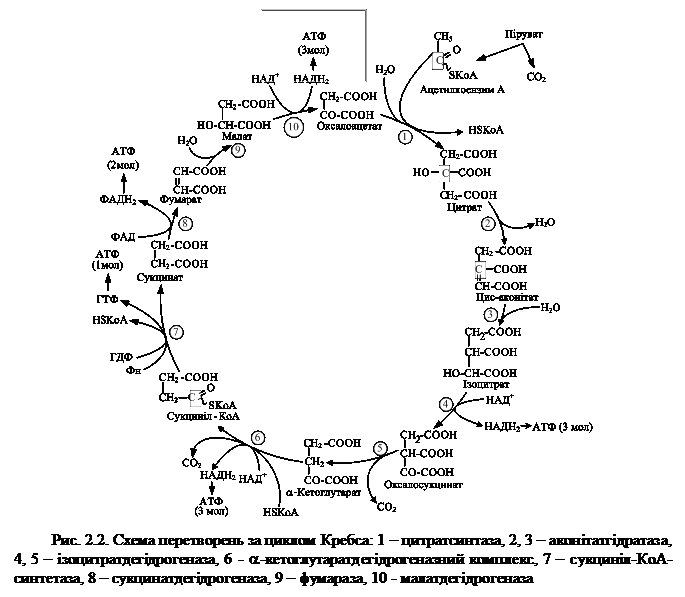
Наступне перетворення a-кетоглутарової кислоти подібне до декарбоксилювання пірувату і відбувається за участю цих самих коферментів (НАД, ліпоєвої кислоти, КоА-SН і тіаміндифосфату - ТДФ).
Каталізується реакція ферментом a-кетоглутаратоксидазою:
В утвореному сукциніл-КоА ацильний радикал сукцинату має макроергічний зв'язок. У цьому зв'язку акумулюється енергія, яка вивільняється при окиснювальному декарбоксилюванні a-кетоглутарової кислоти. Ця енергія під дією специфічного ферменту сукциніл-КоА-синтетази переходить у макроергічний зв'язок гуанозинтрифосфату, внаслідок цього утворюється янтарна кислота (сукцинат).
Сукцинат у присутності сукцинатдегідрогенази окиснюється до фумарової кислоти:
Фумарова кислота, сполучаючись з водою, перетворюється в яблучну кислоту - малат. Реакція каталізується ферментом фумаратгідратазою.
Нарешті, останнім етапом циклу є окиснення яблучної кислоти в присутності малатдегідрогенази, внаслідок чого виникає оксалоацетат.
На стадії утворення оксалоацетату цикл замикається і знову можливе використання нової молекули ацетил-КоА для синтезу лимонної кислоти (цитрату).
Таким чином, у присутності невеликої кількості оксалоацетату та певних ферментних систем відбувається перетворення великої кількості ацетил-КоА. Уся ця складна система ферментів, яка пов'язана з перенесенням електронів і протонів, локалізована в мітохондріях.
Енергія, яка вивільняється при окисненні лимонної кислоти або ацетил-КоА, зберігається в зв'язках НАДН2, ФАДН2 і в ГТФ. Окиснення НАДН2 і ФАДН2 призводить до синтезу макроергічних фосфатних зв'язків АТФ. У цьому випадку окиснення субстрату відокремлене від синтезу макроергічних зв'язків.
Утворення АТФ у циклі Кребса спряжене з окисненням киснем повітря через систему дихальних ферментів відновленого НАДН2 (3 молекули) і однієї молекули ФАДН2.
Експериментально доведено, що при відновленні однієї молекули НАДН2 або НАДФН2 утворюється три молекули АТФ. Отже, усього з 3 молекул НАДН2 утвориться 3 ´ 3 = 9 молекул АТФ.
При відновленні однієї молекули ФАД утвориться 2 молекули АТФ і одна молекула ГТФ (АТФ) синтезується на рівні субстрату при перетворенні сукциніл-КоА в янтарну кислоту. Таким чином, внаслідок перетворення за циклом Кребса 1 молекули ацетил-КоА до СО2 і Н2О може синтезуватися до 12 молекул АТФ. У зв'язку з цим, що при окисненні однієї молекули глюкози утворюється 2 молекули піровиноградної кислоти, а отже, і 2 молекули ацетил-КоА, то при перетворенні в циклі Кребса однієї молекули глюкози синтезуватиметься до 24 молекул АТФ. Крім цього, 2 молекули АТФ утворюватимуться на анаеробному етапі (баланс гліколізу) на стадії утворення піровиноградної кислоти при окисненні 3-фосфогліцеринальдегіду до 3-фосфогліцеринової кислоти, і 6 молекул АТФ синтезуватимуться при окисненні двох молекул НАДН2, що утворюються при окисненні піровиноградної кислоти до ацетил-КоА. Отже, загальний баланс аеробного перетворення 1 моль глюкози становитиме 38 молекул АТФ.
Таким чином, аеробне окиснення органічних субстратів є джерелом максимальної кількості молекул АТФ, в яких акумулюється енергія, що може бути використана організмом для його життєдіяльності.
2.5.2. Біохімічні функції циклу Кребса та його регуляція. Цикл Кребса виконує в організмі людини низку важливих біохімічних функцій, а саме:
а) інтегративну – цикл Кребса є своєрідним метаболічним "колектором", який об'єднує шляхи розпаду вуглеводів, ліпідів і білків:
б) амфіболічну – цикл Кребса виконує подвійну функцію: катаболічну, оскільки в ньому проходить розпад ацетил – КоА, і анаболічну – субстрати цього циклу використовуються для синтезу інших речовин. Так, оксалоацетат йде на синтез аспарагінової кислоти і глюкози, α- кетоглутарат - глутамінової кислоти, сукцинат – гему;
в) енергетичну – в процесі цього обміну утворюється 12 молекул АТФ;
г) водневодонорна - цикл Кребса є основним генератором водню для дихального ланцюга мітохондрій.
Реакції циклу Кребса регулюються на рівні:
1) цитратсинтази (ацетил-КоА та оксалоацетат є активаторами ферменту, інгібіторами ферменту є АТФ, НАДН, сукциніл-КоА);
2) ізоцитратдегідрогенази (АДФ, АМФ) – алостеричні активатори ферменту, іони Са2+- активатори ферментного комплексу; АТФ, ГТФ, НАДН, сукциніл–КоА - алостеричні інгібітори);
3) α-кетоглутаратдегідрогеназа (АДФ-активатор ферменту, АТФ, НАДН, сукциніл-КоА – інгібітори ферменту).
2.5.3. Анаплеротичні та амфіболічні реакції циклу Кребса. Анаплеротичні реакції — реакції, що підвищують концентрацію субстратів циклу Кребса, за рахунок утворення їх в інших метаболічних шляхах (зокрема, при обміні амінокислот, пірувату). Внаслідок цих реакцій посилюються катаболічні процеси в організмі.
Субстрати циклу Кребса утворюються в наступних анаплеротичних реакціях:
1. Перетворення амінокислот на дикарбонові кислоти — субстрати ЦТК:
- утворення α-кетоглутарату в реакціях трансамінування;
- утворення оксалоацетату в реакціях трансамінування;
- утворення α-кетоглутарату внаслідок окиснювального дезамінування у глутаматдегідрогеназній реакції;
- утворення сукциніл-КоА внаслідок трансамінування та окиснювального декарбоксилювання ізолейцину, валіну.
2. Утворення оксалоацетату з пірувату в піруваткарбоксилазній реакції:
Піруват + СО2 + АТФ → Оксалоацетат + АДФ + Фн
У піруваткарбоксилазі коферментом виступає біотин (вітамін Н). За рахунок розщеплення АТФ утворюється проміжний комплекс–фермент-біотин-СОО-, з якого карбоксильна група переноситься на піруват. Активатором піруваткарбоксилази є ацетил-КоА.
За умов низької внутрішньоклітинної концентрації ацетил-КоА швидкість піруваткарбоксилазної реакції є низькою.
Накопичення ацетил-КоА, що спостерігається при активації катаболічних процесів, стимулює через утворення оксалоацетату цикл трикарбонових кислот та інтенсивність окиснення ацетил-КоА. Утворення оксалоацетату з пірувату під дією піруваткарбоксилази є важливою анаплеротичною реакцією в клітинах печінки та нирок.
Таким чином, при наявності ацетил-КоА і нестачі оксалоацетату стимулюється піруваткарбоксилазна реакція, у результаті більше утворюється оксалоацетату, що забезпечує синтез лимонної кислоти та функціонування циклу.
3. Утворення оксалоацетату з фосфоенолпірувату.
Реакція каталізується фосфоенолпіруваткарбоксикіназою. При цьому відбувається утворення ГТФ за рахунок розщеплення макроергічного зв'язку в молекулі фосфоенолпірувату—метаболіту гліколізу.
Фосфоенолпіруваткарбоксикіназна реакція є анаплеротичною реакцією ЦТК, що має місце в міокарді та інших м'язових тканинах. Ця ж реакція, за умов її перебігу в зворотному напрямку, використовується в процесі синтезу глюкози.
Амфіболічні реакції —реакції, що звикористовують субстрати ЦТК для утворення інтермедіатів, необхідних для біосинтетичних процесів:
Фосфоенолпіруват + СО2 + ГДФ → Оксалоацетат + ГТФ
Оксалоацетат є проміжним продуктом глюконеогенезу, використовується для синтезу амінокислот.
1) у ролі амфіболічних можуть виступати реакції, обернені до перетворень амінокислот—у цьому разі дикарбонові кислоти, що утворюються в ЦТК, стимулюють процеси білкового синтезу;
2) важливою реакцією глюконеогенезу є утворення фосфоенолпірувату з оксалоацетату та ГТФ за участю фосфоенолпіруваткарбоксикінази за умов її перебігу в напрямку, зворотному до анаплеротичного процесу.
3) використання проміжного продукту циклу лимонної кислоти–сукциніл-КоА - для синтезу гему;
4) α-кетоглутарат, а також тісно пов'язаний з циклом трикарбонових кислот піруват використовуються для синтезу амінокислот.
Використання проміжних продуктів циклу лимонної кислоти з біосинтетичною метою повинно супроводжуватися катаболічною активністю циклу для утворення АТФ, який необхідний для здійснення реакцій анаболізму.
Отже, ЦТК разом з тканинним диханням і окиснювальним фосфорилуванням забезпечує утворення АТФ, об'єднує процеси метаболізму білків, вуглеводів, ліпідів, пов'язує процеси анаболізму та катаболізму.
Розділ 3. БІОЕНЕРГЕТИЧНІ ПРОЦЕСИ: ТРАНСПОРТ ЕЛЕКТРОНІВ.
ОКИСНЕ ФОСФОРИЛУВАННЯ В МІТОХОНДРІЯХ
Внутрішньомолекулярне окиснення біологічних субстратів (або біологічне окиснення) є основним молекулярним механізмом, за рахунок якого забезпечується енергетичні потреби функціонування живих організмів.
Важливу роль у розвитку теорії біологічного окиснення відіграли роботи В. Палладіна (1907). Вивчаючи окиснення субстратів в рослинах, В. Палладін встановив, що воно може проходити і при відсутності кисню, якщо в середовиші є речовини, які здатні приєднувати водень. Такими речовинами можуть бути пігменти хромогени й інші речовини, які виконують функцію проміжних перенощиків водню. Приєднуючи водень від субстратів, які при цьому окиснюються, хромогени відновлюються і стають неполярними:

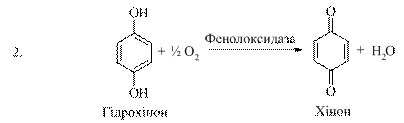
Біологічне окиснення має важливе значення для живих організмів. Велика кількість енергії, яка необхідна для життєдіяльності, утворюється в результаті окиснювально-відновних реакцій.
Окиснення – це процес втрати атомом, молекулою, що окиснюється (субстратом окиснення), електронів або атомів водню. Окиснення речовин може здійснюватись наступним чином: а) відщепленням водню від субстрату (процес дегідрування); б) віддачею субстратом електрона; в) приєднанням кисню до субстрату. Окиснення шляхом приєднання кисню до різних речовин відбувається переважно шляхом включенням його з води. Перетворення жирних кислот, амінокислот в окси- та кетокислоти відбувається саме поєднанням процесів дегідрування і гідратації.
Такий процес окиснення без участі атмосферного кисню, як уже зазначалося, називається анаеробним окисненням. У вищих організмів, в тому числі і в людини, теж відбувається анаеробне окиснення багатьох субстратів. Таке окиснення, зокрема, спостерігається при перетворенні фосфогліцеринового альдегіду в 1,3-дифосфогліцеринову кислоту, при окиснювапьному дезамінуванні глутамінової кислоти до α-кетоглутарової кислоти і в ряді інших процесів. Однак вирішальне значення для життя цих організмів мають аеробні процеси, врешті-решт, водень через ряд проміжних систем передається на атмосферний кисень з утворенням молекули води.
Відновлення – реакція зворотна окисненню, супроводжується приєднанням органічним субстратом електронів або атомів водню (гідруванням) субстрату.
Відповідно, в окисно-відновному процесі бере участь два типи речовин: окисник (сполука, що приймає електрони) та відновник (сполука, що віддає електрони). Окисник та відновник складають окисно-відновну систему (редокс систему).
Здатність окисно-відновної системи віддавати або приймати електрони характеризується її окисно-відновним потенціалом, величина якого кількісно визначає здатність системи бути донором або акцептором електронів відносно іншої редокс-системи.
Згідно рекомендованих положень Міжнародного союзу з теоретичної та прикладної хімії прийнято вважати, що більш негативні редокс-потенціали мають системи з підвищеною здатністю віддавати електрони, а більш позитивні - системи, що схильні акцептувати електрони.
Стандартні окисно-відновні потенціали вимірюють (у вольтах) відносно потенціалу водневого електрода Н+/Н2, приймаючи останній за нуль, при рН=0. Для біологічних систем більш зручно визначати редокс-потенціали за умов рН=7,0 – такий стандартний потенціал позначають Е0’. За цих умов Е0’ водневого електрода дорівнює -0,42 в.
Date: 2015-07-17; view: 1353; Нарушение авторских прав