
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глютаминовая кислота
|
|
1. Кислоту глутаминовую получают гидролизом белковых веществ. В миозине, казеине, α-лактоглобулине содержится до 20% глутаминовой кислоты и до 3% метионина. Еще больше (до 45%) глутаминовой кислоты в пшеничном глиадине, который обычно служит источником ее получения. Выделяют аминокислоты из гидролизатов белков хроматографическим методом. Эти аминокислоты можно так же синтезировать. В настоящее время в промышленности кислоту глутаминовую получают микробиологическим синтезом из α-кетоглутаровой кислоты.
2. Химическая реакция получения глутаминовой кислоты:
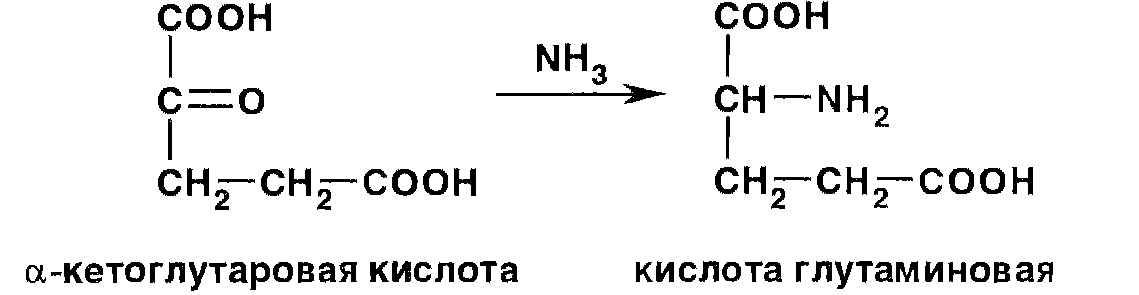
3. Технологическая схема получения глутаминовой кислоты:

4. Acidum glutaminicum. Удельное вращение составляет от + 30 до + 340 (5% раствор препарата в разведенной кислоте хлороводородной).
5. Кислота глютаминовая – вещество органической природы, представляет собой белый кристаллический порошок, кислого вкуса, с едва ощутимым запахом.
ЭТАП
1.
2. Приготовил пробирки, разновесы, аптечные весы, воду свежепрокипяченную, пипетки на 1 мл, 5 мл, глазные пипетки, УФ – лампу.
3. Предложил, что для испытания подлинности кислоты глютаминовой, государственная фармакопея Х издания рекомендует цветную реакцию с резорцином в присутствии концентрированной кислоты серной. Реакция основана на гидратации кислоты глютаминовой до пирролидонкарбоновой кислоты и конденсации последней резорцином.
2 мг препарата смешал с 2 мг резорцина и 5 каплями концентрированной кислоты серной и нагрел до появления зелено-коричневого окрашивания. Охладил, прибавил 5 мл воды и 5 мл раствора аммиака, появляется красно-фиолетовое окрашивание с зеленой флюоресценцией.
4. Указал, что кислота глютаминовая при нагревании с резорцином в присутствии концентрированной кислоты серной образует плав красного цвета.
5. Показал зеленую флюоресценцию.
ЭТАП
1. Определил, что примесь специфическая – посторонние аминокислоты.
СООН Метод йодометрии
СН NH2
Метод меркуриметрии
CH2 CH2 COOH
Метод определения азота Метод нитритометрии
2. Выделил общие принципы испытаний на специфические примеси:
1) В государственной фармакопее Х издания приведены не константы индивидуальных (свободных от примесей) веществ, а допустимые пределы этих констант.
2) Способ, основанный на приготовлении эталонного раствора из вещества, являющегося примесью к данному препарату.
3) Выделение примеси из препарата бумажной хромотографией.
Путем сравнения расположения величины пятен, интенсивности их окраски у свидетеля и испытуемого препарата делают заключение о допустимых пределах примесей.
3. Охарактеризовал испытание на предельное содержание посторонних аминокислот. К 5 мл того же фильтрата прибавляют 5 мл реактива Фелинга и кипятят на сетке 2 минуты, не должно появляться зеленое или бурое окрашивание.
Предложил, что кислоту глютаминовую государственной фармакопее Х издания количественно определяют методом нейтрализации 0,1 н. раствором натрия гидроксида с индикатором бромтимоловым синим.
4. Дал методику определения допустимых пределов примесей (хлоридов). 0,1 г препарата взбалтывают с 25 мл воды в течение 5 минут и фильтруют. 10 мл фильтрата должны выдерживать испытание на хлориды (не более 0,05 % в препарате).
А 0,3116
5. Vтеор = = = 21,18 мл
Т 0,01471
М (1/Z) = М.м. / 2
ЭТАП
1. Выбрал смешанный индикатор: смесь метилового красного и метиленового синего в отношении 2:1.
2. В методе нейтрализации молярная масса эквивалента кислоты глютаминовой равна его молярной массе.
3. Масса точной навески а = 0,3013 г, Т = 0,01471 г/мл, М.м. кислоты глютаминовой
а
Vтеор = = 20,3 мл
Т
Vпр = 20,4 мл
Т ∙ Vпр ∙ 100 % 0,01471 ∙ 20,4 ∙ 100 %
Х = = = 99,1 %
а 0,3013
4. Сделал заключение, что удовлетворяет требованиям государственной фармакопеи Х издания по разделу «количественное определение» (должно быть не менее 98,5 %).
ЭТАП
1. Обосновал, что условия хранения лекарственных средств регламентируются приказом Министерства Здравоохранения от 10.05.1989г. № 238. В соответствии с этим приказом все лекарственные средства в зависимости от физических и физико-химических свойств, а также от воздействия на них различных факторов внешней среды подразделяют на требующие защиты от света, воздействия влаги, улетучивания, повышенной и пониженной температуры, от газов, содержащихся в окружающей среде. Препарат кислоты глютаминовой хранят в хорошо укупоренной таре, предохраняющей от воздействия света, в сухом, прохладном, защищенном от света месте, чтобы не допустить разложения.
2. Отразил 6 пункт приказа № 238: Особенности хранения лекарственных средств, требующих защиты от воздействия света. К числу лекарственных средств, требующих защиты от воздействия света относятся аминосоединения.
3. Описал по государственной фармакопее Х издания показатель «Хранение» на кислоту глютаминовую. В хорошо укупоренной таре, предохраняющей от действия света.
4. Описал, что кислоту глютаминовую вводят внутрь или внутривенно до 1 г в сутки. Применяется в виде таблеток по 0,25 г, покрытые оболочкой.
Указал состав на одну таблетку:
Кислоты глютаминовой 0,25 г
Вспомогательных веществ - до получения
таблетки массой 0,3 г (без оболочки)
КАЛЬЦИЯ ГЛЮКОНАТ
1. Кальция глюконат получают электрохимическим окислением глюкозы в присутствии бромида кальция и карбоната кальция. При электролизе бромида кальция на аноде выделяется свободный бром, который окисляет глюкозу до глюконовой кислоты. Глюконовая и бромоводородная кислоты нейтрализуется карбонатом кальция. Образующейся бромид кальция вновь подвергают электролизу.
2. Химическая реакция получения кальция глюконата:

3. Технологическая схема получения кальция глюконата в промышленности:
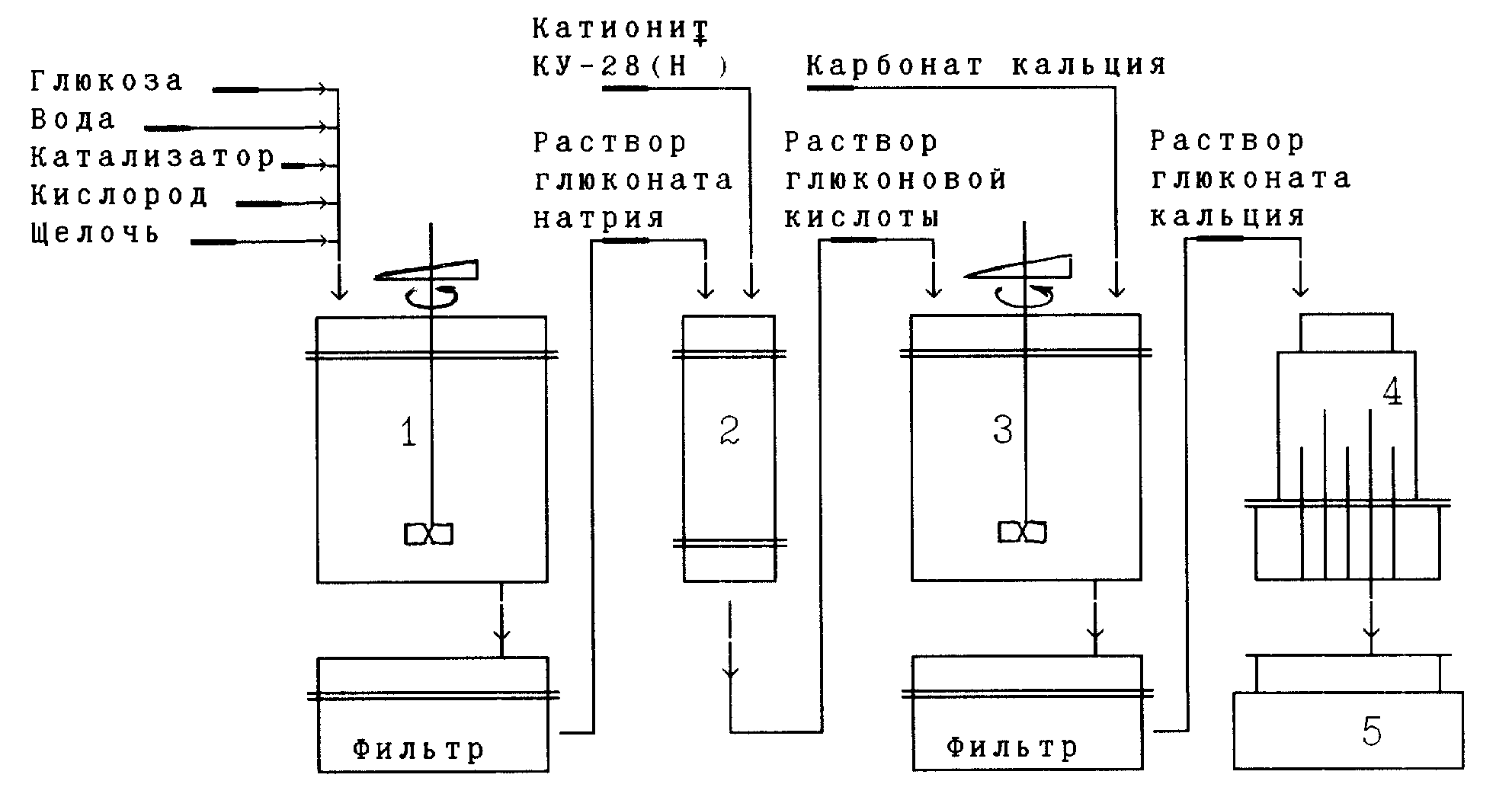
4. Кальция глюконат - вещество органической природы. Относится к солям карбоновых кислот.
5. Порошок, раствор для инъекций 10%, таблетки по 0,5 г. Для применения в детской практике выпускаются таблетки по 0,25 г и 5% раствор с фруктовым сиропом. Применение: противоаллергическое, гемостатическое, снижающее проницаемость капилляров, источник ионов кальция.
ЭТАП
1. Провел реакцию подлинности на ионы кальция: к 1 мл раствора кальция глюконата (0,002-0,02г иона кальция) прибавил 1 мл раствора оксалата аммония. Определил, что белый осадок, полученный при взаимодействии глюконата кальция с раствором оксалата аммония, нерастворим в кислоте уксусной и растворе аммиака, растворим в разведенных минеральных кислотах.
2. Правильно указал метод идентификации по ГФ РК: определение проводят методом тонкослойной хроматографии, используя в качестве тонкого слоя силикагель G P.
3. Определил, что соль кальция, смоченная кислотой хлороводородной и внесенная в пламя горелки, окрашивает его в кирпично-красный цвет.
4. Выбрал пипетки на 1, 2 мл, пробирки, весы ручные, разновесы, бюкс. Выбрал растворы оксалата аммония, хлорида окисного железа, аммиака, хлороводородной кислоты, кислоты серной.
5. Указал реакцию подлинности на глюконат-ион: 5 мл (1:50) раствора с 2 каплями раствора хлорида окисного железа дает светло-зеленое окрашивание. Соль в воде нерастворима.
6. Указал, что ион кальция и глюконат-ион определяются в нейтральной среде.
ЭТАП
1. Растворил 2 г препарата в 20 мл воды очищенной. После 5 минутного кипячения раствора сравнивают с водой очищенной на компоратаре. Прозрачным считают раствор, если при рассмотрении невооруженным глазом не наблюдается присутствие нерастворимых частиц.
Дал определение кислотности или щелочности: 0,5 г препарата растворяют при подогревании в 25 мл свежепрокипяченной воды; раствор должен быть нейтральным (раствор лакмуса)
2. Указал недопустимые примеси – декстрин, сахароза: 0,5 г субстанции растворяют в смеси 2 мл кислоты хлороводородной и 10 мл воды. Кипятят в течении 5 минут. Затем охлаждают, прибавляют 10 мл раствора натрия карбоната и выдерживают. Затем доводят объем раствора водой до 25 мл и фильтруют. К 5 мл фильтрата прибавляют 2 мл раствора медно-тартратного и кипятят в течении 1 минуты, не должен образовываться красный осадок.
3. Назвал метод количественного определения кальция глюконата – комплексонометрия. Выбрал титрант 0.05 М раствор натрия эдетата. Выбрал индикатор кислотный хром темно-синий. Указал, что взятую навеску 0,4 г вещества растворяют при подогревании. Указал, что необходимо соблюдать последовательность добавления реагентов по методике: точную навеску растворяют в 25 мл воды очищенной и прибавляют 5 мл аммиачного буферного раствора, 7 капель раствора кислотного хром темно-синего и титруют 0,05 М раствором натрия эдедата до сине-фиолетового окрашивания.
Указал, что раствор титруют до появления синей окраски. Содержание препарата должно быть не менее 98.5 % и не более 102.0 %.
4. Добавил аммиачный-буферный раствор. Указал рН 9.5-10 титруемого раствора.
5. Указал образование комплексов металлов с эриохром черным специальным в щелочном растворе при рН 7.0-11.0.
6. Указал на малую устойчивость раствора индикатора во времени.
ЭТАП
1. Э=М.М.
2. Т= 0.02242 г/мл
3. Расчет содержания лекарственного вещества в препарате, в процентах
(Х):
Х(%)= V*Т*100* Kn / а=100,89%
где V - количество титрованного раствора, израсходованного на титрование лекарственного вещества, мл;
Т- титр, количество растворенного вещества, соответствующего 1 мл титрованного раствора, г/мл;
а – навеска порошка, взятая для анализа, г;
Kn - коэффициент поправки.
4. Расчет содержания лекарственного вещества в растворе для инъекций, (Х) в пересчете на один мл.
Х (г)= V*Т*Kn*1 / а;
где а - объем раствора исследуемого раствора, мл;
V - количество титрованного раствора, израсходованного на титрование лекарственного вещества, мл;
Т- титр, количество растворенного вещества, соответствующего 1 мл титрованного раствора, г/мл;
Kn - коэффициент поправки.
5. Содержание кальция глюконата в 10 % растворе для инъекций должно быть в пределах 0,0106-0,0112 г в 1 мл.
ЭТАП
1. Указал, что 10 ампул помещают в коробки из картона коробочного марки А по ГОСТ 7933-75. Указал, что в коробки вкладывают скарификатор ампульный по ТУ 64-1-994-80 или нож ампульный по ТУ 400-6-169-85.
2. Объяснил, что на каждой ампуле методом глубокой печати быстро закрепляющейся краской по ТУ 788-86 указывают название препарата на государственном и русском языках, концентрацию раствора в %, объем в мл, номер серии и срок годности.
3. Транспортирование проводят в соответствии с ОСТ 64-034-87 и ГОСТ 17768-80.
4. В защищенном от света месте, срок годности растворов по 5 и 10 мл, 2 года.
Date: 2016-07-18; view: 2706; Нарушение авторских прав