
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Глава 1. Обзор литературы
|
|
ВВЕДЕНИЕ
В современной науке и технике непрерывно возрастает практическое использование расплавленных солевых смесей, которые представляют собой в большинстве случаев многокомпонентные системы. Определение характеристик (состав, температура плавления) важных в прикладном отношении композиций, процессов, протекающих при плавлении и кристаллизации сплавов, а также фаз находящихся в равновесии при данных термодинамических условиях возможно при изучении фазовых диаграмм.
Целью работы: поиск фазового состава в нонвариантных равновесиях в тетраэдрах LiF-KCl-LiCl-Li2CrO4 и LiF-KCl-K2CrO4-KF и в секущем треугольнике LiF-KCl-K2CrO4. Для достижения данной цели необходимо решить следующие задачи:
· Разбиение диаграмм составов четырехкомпонентной взаимной системы Li,K||F,Cl,CrO4 на симплексы формирование древа фаз;
· Анализ элементов огранения изученных систем; прогноз числа и состава кристаллических фаз в точках нонвариантного равновесия.
· Экспериментальное исследование систем, входящих в элементы огранения четырехкомпонентной взаимной системы Li,K||F,Cl,CrO4;
· Расчет термодинамических свойств систем: удельных энтальпий плавления, плотности, объемных удельных энтальпий, энтропий плавления;
· Поиск функциональных составов для использования в качестве теплоаккумулирующих материалов и электролитов химических источников тока (ХИТ).
В работе впервые проведено разбиение на симплексы четырехкомпонентной взаимной системы Li,K||F,Cl,CrO4, построено древо фаз, экспериментально определены составы, температуры и энтальпии плавления точек нонвариантных равновесий систем, входящих в элементы огранения четырехкомпонентной взаимной системы Li,K||F,Cl,CrO4 подтвержденные методом ДТА, и рассчитаны термодинамические свойства систем:LiF-KCl-LiCl-Li2CrO4, LiF-KCl-K2CrO4-KF, LiF-KCl-K2CrO4.
ГЛАВА 1. ОБЗОР ЛИТЕРАТУРЫ
Ценные свойства солевых расплавов на основе галогенидов, хроматов и щелочных металлов обеспечивают постоянное расширение областей их применения. Ряд свойств: высокая электрическая проводимость, сравнительно низкая плотность, возможность работать в широком температурном диапазоне, возможность электролитического выделения из них наиболее активных металлов. При этом исследование многокомпонентных систем из солей лития и калия представляет особый интерес, что обусловлено в первую очередь их доступностью и низкими температурами плавления. В настоящее время в центре внимания батареи на основе лития, в связи с обилием и технологическим преимуществом [ ]. Расплавы натрия и калия используются в качестве теплоносителей в атомных реакторах и в авиационных двигателях.
Литий - ионные аккумуляторы (ЛИА) появились на мировом рынке химических источников тока (ХИТ) сравнительно не давно. В качестве анода литиевых аккумуляторов используют матрицу из углеродных материалов. Электрический ток во внешней цепи появляется за счет переноса литиевых ионов от анода к катоду. Широкое использование литий - ионные аккумуляторы в электронных устройствах. Массовое производство ЛИА в России отсутствует, так как основная масса электронной техники поступает к нам из-за рубежа. Зарубежная продукция поступает на российский рынок практически только в виде батарей в продаваемой портативной аппаратуре и запасных [ ].
Химический источник тока (ХИТ) – это электрохимические устройства, где происходит прямое преобразование химической энергии в электрическую энергию постоянного тока. Относятся: аккумуляторы, гальванические элементы, топливные элементы. Во всех ХИТ используются электролиты: водные, неводные, твердые. К достоинствам ХИТ относятся высокий КПД (до 0.8) и высокая удельная мощность. Недостатком является ограниченный срок службы [ ].
Солевые смеси используются во многих промышленных процессах, в частности, для создания перспективных флюсов для сварки и пайки металлов, в машиностроении для нанесения гальванических покрытий из ионных расплавов, в ядерной энергетике солевые ионные расплавы перспективны как теплоносители, высокотемпературных химических источников тока (ХИТ), металлотермия, в качестве рабочих тел тепловых аккумуляторов. Развитие связано с применением технологических приемов физического и химического воздействия на жидкий металл в процессе плавки, разливки, сварки [ ].
1.3. Обзор изученных систем, входящих в четырехкомпонентную взаимную систему Li,K||F,Cl,CrO4
Исследуемая система Li,K||F,Cl,CrO4 (рис.) относится к типу 2||3 по В.П. Радищеву и представляет собой четырехкомпонентную взаимную систему из 6 солей, включающую 9 двухкомпонентных, 2 трехкомпонентных и 3 трехкомпонентных взаимных системы. На основании проведенного анализа литературных источников составлена табл. 1.1, в которой приведены данные по системам, ограняющим четырехкомпонентную взаимную систему Li,K||F,Cl,CrO4.
Двухкомпонентные систем:
LiF-LiCl [8]. Эвтектика (e1) при температуре 498°С и 30.5% LiF.
LiF-Li2CrO4 [9]. Эвтектика (e2) при температуре 453°С и 14% LiF.
LiCl-Li2CrO4 [9]. Эвтектика (e3) при температуре 400°С и 32% LiCl.
KF-KCl [8]. Эвтектика (e4) при температуре 606°С и 45% KF.
KF-K2CrO4 [8]. Эвтектика (e5) при температуре 727°С и 57% KF, эвтектика (e6) при температуре 764°С и 31% KF, образуется соединение конгруэнтного плавления K3FCrO4 (D1) при температуре 766°С и 67% хромата калия.
KCl-K2CrO4 [10]. Эвтектика (e7) при температуре 650°С и 52% KCl.
LiF-KF [11]. Эвтектика (e8) при температуре 492°С и 50% KF.
LiCl-KCl [11]. Эвтектика (e9) при температуре 354°С и 58% LiCl.
Li2CrO4-K2CrO4 [10]. Соединения конгруэнтного плавления LiKCrO4 (D2) при температуре 550°С и 50% хромата лития, эвтектика (e10) при температуре 415°С и 74% Li2CrO4, эвтектика (e11) при температуре 546°С и 46% Li2CrO4.
Трехкомпонентные системы:
LiF-LiCl-Li2CrO4 [9]. Эвтектика (Е1) при температуре 379°С и составе6% фторида лития, 31% хромата лития и 63% хромата лития.
KF-KCl-K2CrO4 [12]. Соединение конгруэнтного плавления K3FCrO4, присутствующее в двухкомпонентной системе KF-K2CrO4, разбивает трехкомпонентную систему на два симплекса. В стабильном треугольнике KF-KCl-K3FCrO4 образуется эвтектика (E2) при температуре 576°С и составе 34.5% фторида калия, 41.5% хлорида калия и 24% хромата калия. В стабильном треугольнике KCl-K3FCrO4-K2CrO4 образуется эвтектика (E3) при температуре 576°С и составе 18.5% фторида калия, 42% хлорида калия и 39.5% хромата калия. В квазибинарной системе KCl-K3FCrO4 образуется эвтектика (e12) при температуре 580°С и 57% KF.
Трехкомпонентные взаимные системы:
Li,K||F,Cl [13]. Эвтектика (Е4) при 468°С и составе 46% фторида лития, 47.5% фторидакалия, 6.5% хлорида калия. Эвтектика (Е5) при температуре 346°С и составе 3.5% фторида лития, 56% хлорида лития, 40.5% хлорида калия. На стабильной диагоналиLiF-KCl - эвтектика (е13) при температуре 710°С и составе 19% фторида лития.
Li,K||F,CrO4 [13]. Внутри тройной взаимной системы соединение K3FCrO4 (D1) выклинивается и не принимает участие в разбиении системы. Следовательно, в трехкомпонентной взаимной системе образуются три эвтектики и точка выклинивания. Эвтектика (Е6) при температуре 378°С и составе 77% хромата лития, 5% фторида лития, 18% хромата калия. Эвтектика (Е7) при температуре 486°С и составе 51% фторида лития, 47.5% фторида калия, 1.5% хромата калия. Эвтектика (Е8) при температуре 496°С и составе 8% фторида лития, 53% хромата лития, 39% хромата калия. Точка выклинивания (R) образуется при температуре 524°С и составе47% фторида калия, 1.5% фторида калия, 51.5% хромата калия. Стабильная диагональ LiF-K2CrO4 также характеризуется эвтектическим типом плавления (e14 735°Си 45% LiF).
Li,K||Cl,CrO4 [14]. Образуются эвтектики: (Е9) при температуре 320°С и составе 29.5% хлорида калия, 25.8% хлорида лития, 44,7% хромата лития; (Е10) при температуре 346°С и составе 17.6% хлорида калия, 68.6% хромата лития, 13.8% хромата калия; (Е11) при температуре 432°С и составе 43.5% хромата лития, 15.5% хлорида калия, 41% хромата калия. На стабильной диагонали KCl-Li2CrO4 и триангулирующей секущей KCl-LiKCrO4 образуются эвтектики с температурами плавления 352°С и 434°С, соответственно.
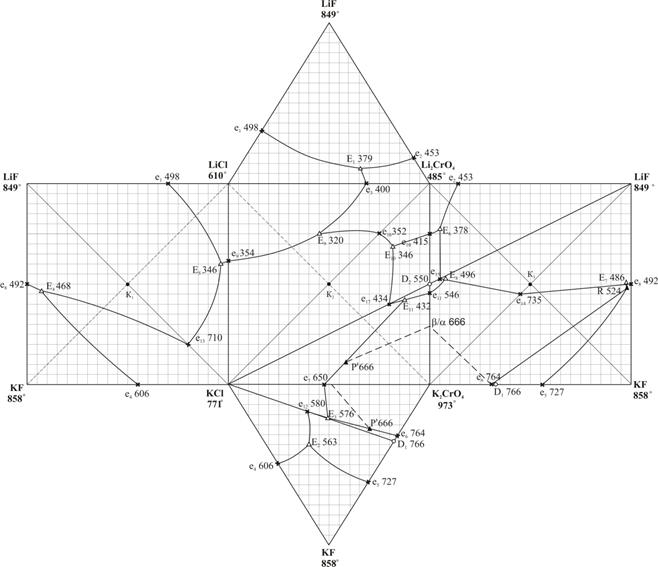
Рис. 1. 1. Развертка граневых элементов четырехкомпонентной взаимной системы Li,K||F,Cl,CrO4
Таблица 1.1
Данные литературы о характеристиках точек нонвариантных равновесий двух-, трех- и трехкомпонентных взаимных систем
| Наименование системы | Точки (линии) нонвариантных равновесий | Метод исследова-ния | Лите-рату-ра | ||||||||
| Состав, экв. доля, выраженная в % | Характер точек нонвариантного равновесия | Температура фазового перехода, ºС | Твердые фазы, характер превращений | ||||||||
| Двухкомпонентные системы | |||||||||||
| LiF-LiCl | 30.5 | 69.5 | - | - | e1 | LiF, LiCl | ДТА, РФА | [8] | |||
| LiF-Li2CrO4 | - | - | e2 | LiF, Li2CrO4 | ДТА | [9] | |||||
| LiCl-Li2CrO4 | - | - | e3 | LiCl, Li2CrO4 | ДТА | [9] | |||||
| KF-KCl | - | - | е4 | KF, KCl | ВПА | [8] | |||||
| KF-K2CrO4 | - | - | е5 | KF, KF·K2CrO4 | ДТА | [8] | |||||
| D1 | KF·K2CrO4 | ||||||||||
| е6 | KF·K2CrO4, β-K2CrO4 | ||||||||||
| KCl-K2CrO4 | - | - | e7 | KCl, α-K2CrO4 | ВПА | [10] | |||||
| LiF-KF | - | - | e8 | LiF, KF | ВПА | [11] | |||||
| LiCl-KCl | - | - | e9 | LiCl, KCl | ВПА | [11] | |||||
| Li2CrO4 -K2CrO4 | - | - | e10 | Li2CrO4, Li2CrO4·K2CrO4 | ДТА | [10] | |||||
| - | - | e11 | Li2CrO4·K2CrO4, α-K2CrO4 | ||||||||
| - | - | D2 | Li2CrO4·K2CrO4 | ||||||||
| Трехкомпонентные системы | |||||||||||
| Li||F,Cl,CrO4 | - | Е1 | LiF, LiCl, Li2CrO4 | ДТА | [9] | ||||||
| K||F,Cl,CrO4 | 34.5 | 41.5 | - | E2 | KF, KCl, KF·K2CrO4 | ВПА, ДТА | [12] | ||||
| 18.5 | 39.5 | - | E3 | KCl, KF·K2CrO4, α-K2CrO4 | |||||||
| 21.5 | 21.5 | - | e12 | KCl, KF·K2CrO4 | |||||||
| Трехкомпонентные взаимные системы | |||||||||||
| Li,K||F,Cl | - | 47.5 | 6.5 | E4 | LiF, KF, KCl | ВПА | [13] | ||||
| 3.5 | - | 40.5 | E5 | LiF, LiCl, KCl | |||||||
| - | - | е13 | LiF, KCl | ||||||||
| Li,K||F,CrO4 | - | E6 | LiF, Li2CrO4·K2CrO4 , Li2CrO4 | ВПА | [13] | ||||||
| - | 47.5 | 1.5 | E7 | LiF, KF, K2CrO4 | |||||||
| - | E8 | LiF, Li2CrO4·K2CrO4, K2CrO4 | |||||||||
| - | - | е14 | LiF, K2CrO4 | ||||||||
| Продолжение табл. 1.1 | |||||||||||
| Li,K||F,CrO4 | е15 | LiF, Li2CrO4·K2CrO4 | |||||||||
| - | 51.5 | 1.5 | R | KF,K2CrO4, KF·K2CrO4 | |||||||
| Li,K||Cl,CrO4 | 29.5 | 44.7 | 25.8 | - | E9 | KCl, LiCl, Li2CrO4 | ДТА | [14] | |||
| - | 68.6 | 17.6 | 13.8 | E10 | KCl, Li2CrO4 , Li2CrO4·K2CrO4 | ||||||
| - | 41.0 | 15.5 | 43.5 | E11 | KCl, β-K2CrO4, Li2CrO4·K2CrO4 | ||||||
| - | - | е16 | KCl, Li2CrO4 | ||||||||
| - | е17 | KCl, Li2CrO4·K2CrO4 | |||||||||
Date: 2016-06-06; view: 685; Нарушение авторских прав