
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Газ молекуласының еркіндік дәрежесі
|
|
Газ молекуласының еркіндік дәрежесі деп молекуланың кеңістіктегі орнын анықтайтын тәуелсіз параметрлердің жиынтығын айтамыз. Егер кез-келген дене кеңістікте қозғалатын болса, онда осы қозғалысты тәуелсіз алты қозғалыстың жиынтығы түрінде қарастыруға болады: үш ілгерілемелі қозғалыстың (тікбұрышты координаталар жүйесінің осьтері бойымен), үш айналмалы қозғалыстың (дененің массалар центрі арқылы өтетін өзара перпендикуляр үш осьтің айналасында) жиынтығы.
Қалыпты жағдайда газ молекулаларының еркіндік дәрежесі:

Жоғары температураларда бұл еркіндік дәрежесіне тербелмелі қозғалыстың бұл еркіндік дәрежесі қосылады.
Бір атомды газ үш бағытта ілгерілемелі қозғала алады. Сондықтан бір атомды газдың еркіндік дәрежесі  -ке тең.
-ке тең.
Екі атомды газ үш бағытта ілгерілемелі және екі бағытта айналмалы қозғала алады (сурет). Сондықтан екі атомды газдың еркіндік дәрежесі  -ке тең болады.
-ке тең болады.

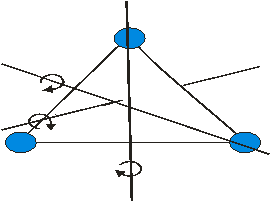
2-атомды газ үшін 3-атомды газ үшін
Үш атомды газ үш бағытта ілгерлемелі және үш бағытта айналмалы қозғала алады Сондықтан үш атомды газдың еркіндік дәрежесі  -ға тең болады.
-ға тең болады.
Максвелл таралуы
Ағылшын ғалымы Максвелл газ молекулаларының жылдамдық бойынша таралып орналасуын анықтайтын заңды ашты. Бұл заңдылық Максвелл таралуы деп аталды.
Максвелл ықтималдық теориясы мен математикалық статистика заңдылықтарын пайдалана отырып таралу функциясын алды.
Таралу функциясы  - дегеніміз жылдамдықтары модулі
- дегеніміз жылдамдықтары модулі  интервалы арасында жататын газ молекулаларының үлесі болып табылады.
интервалы арасында жататын газ молекулаларының үлесі болып табылады.
 -функциясы газ молекулаларының жылдамдықтар бойынша таралып орналасу функциясы деп аталады. Өз кезегінде
-функциясы газ молекулаларының жылдамдықтар бойынша таралып орналасу функциясы деп аталады. Өз кезегінде  молекулалардың жылдамдықтарының модульдері
молекулалардың жылдамдықтарының модульдері  және
және  аралығында жату ықтималдылығын анықтайды.
аралығында жату ықтималдылығын анықтайды.

мұндағы: 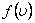 -таралу тығыздығы,
-таралу тығыздығы, 
 .
.
Жылдамдықтары  -ден
-ден  -ге дейінгі аралықта жататын молекулалар саны:
-ге дейінгі аралықта жататын молекулалар саны:

Газ молекулаларының жылдамдықтар бойынша таралу графигі келесі суретте көрсетілген.


мұндағы: Т1<Т2.
Газ температурасы артқан сайын графиктің максимумы үлкен жылдамдықтар жағына ығысады. Сондықтан газдарды қыздырғанда аз жылдамдықпен қозғалатын молекулалардың үлесі азаяды, ал үлкен жылдамдықпен қозғалатын молекулалардың үлесі артады.
Газдағы көпшілік молекулалар ықтимал жылдамдықтай жылдамдықпен қозғалады. 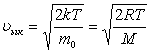 .
.
Молекулалардың орташа жылдамдығы -  .
.
Молекулалардың орташа квадраттық жылдамдығы - 
Яғни осы формулалардан  болатыны көрінеді.
болатыны көрінеді.
Больцман таралуы
Сыртқы күштер болмаған жағдайда термодинамикалық тепе-теңдік күйіндегі газ молекулаларының орташа концентрациясы бар жерде бірдей болады.

| Ал газ сыртқы өрісте орналасқан кезде молекулалардың таралып орналасуы өзгеше болады. Сыртқы потенциалды өрістегі газды қарастырамыз. Мысалы: ауырлық өрісіндегі ауаны. Газдың барлық қабаттарындағы температурасы бірдей деп есептейік. Сыртқы күш төмен, ал z осі жоғары бағытталсын. |
Газда ойша  қабатын бөліп аламыз (сурет). Осы
қабатын бөліп аламыз (сурет). Осы  қабатқа төменнен жоғары бағытталған
қабатқа төменнен жоғары бағытталған  қысым айырмасының нәтижесінде пайда болған күш әсер етеді, ал жоғарыдан төмен қарай сыртқы өрістің F күші әсер етеді. Бөлініп алынған газ қабатының төменгі және жоғарғы қабатына әсер ететін
қысым айырмасының нәтижесінде пайда болған күш әсер етеді, ал жоғарыдан төмен қарай сыртқы өрістің F күші әсер етеді. Бөлініп алынған газ қабатының төменгі және жоғарғы қабатына әсер ететін  және
және  қысымдарының айырмасы
қысымдарының айырмасы  гидростатикалық қысымға тең болады:
гидростатикалық қысымға тең болады:
 .
.
 екенін ескере отырып, келесі өрнекті аламыз:
екенін ескере отырып, келесі өрнекті аламыз:
 немесе
немесе  .
.
Осы өрнекті 0-ден h биіктікте және  -ден
-ден  қысымға дейін интегралдап, алатынымыз:
қысымға дейін интегралдап, алатынымыз:

Барометрдің көмегімен  және
және  қысымдарын өлшеу арқылы биіктікті анықтауға болады:
қысымдарын өлшеу арқылы биіктікті анықтауға болады:
 .
.
Бұл өрнек барометрлік формула деп аталады.
 екенін ескерсек
екенін ескерсек
 .
.
 өрнектерін пайдаланып, жоғарыдағы өрнек келесі түрде жазылады:
өрнектерін пайдаланып, жоғарыдағы өрнек келесі түрде жазылады:
 ,
,
мұндағы: 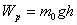 газ молекулаларының сыртқы өрістегі потенциалдық энергиясы болып табылады.
газ молекулаларының сыртқы өрістегі потенциалдық энергиясы болып табылады.
Сонда алынатын 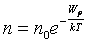 формуласы Больцман таралуының математикалық өрнегі болып табылады.
формуласы Больцман таралуының математикалық өрнегі болып табылады.
Date: 2016-05-18; view: 1617; Нарушение авторских прав