
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изотермический, изохорический (изохорный) и изобарический (изобарный) процессы в идеальном газе. Их аналитическое и графическое представление
|
|
Изопроцесс – процесс, протекающий при неизменном значении одного из макропараметров системы.
 Изотермический процесс – процесс в системе, протекающий при неизменном значении температуры (Т = const).
Изотермический процесс – процесс в системе, протекающий при неизменном значении температуры (Т = const).
Закон Бойля – Мариотта: для газа данной массы произведение давления газа на его объем есть величина постоянная, если температура не меняется.
Формулы, выражающие закон Бойля – Мариотта:
 ;
;  ;
;
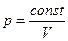 .
.
Графики изотермического процесса представлены на рис. 6, 7, 8.
Изобарический (изобарный) процесс – процесс в системе, протекающий при неизменном значении давления (р = const).
Закон Гей-Люссака: для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется.
Формулы, выражающие закон Гей-Люссака:  ;
;  ;
;  ;
;  ;V = VoαT,где Vo – объем газа при
;V = VoαT,где Vo – объем газа при  , to – температура газа по шкале Цельсия,V – объем газа при температуре toC, T – абсолютная температура газа, α = 1/273 К – температурный коэффициент объемного расширения газа.
, to – температура газа по шкале Цельсия,V – объем газа при температуре toC, T – абсолютная температура газа, α = 1/273 К – температурный коэффициент объемного расширения газа.
Графики изобарического процесса представлены на рис. 9, 10, 11, 12.
Изохорический (изохорный) процесс – процесс в системе, протекающий при неизменном значении объема (V = const).
Закон Шарля: для газа данной массы отношение давления к температуре постоянно, если объем газа не меняется.
Формулы, выражающие закон Шарля:
 ;
;  ;
;  ;
;  ;
;  ,где po – давление газа при
,где po – давление газа при  , toC – температура газа по шкале Цельсия, p – давление газа при температуре toC, Т – абсолютная температура газа, γ = 1/273K – термический коэффициент давления.
, toC – температура газа по шкале Цельсия, p – давление газа при температуре toC, Т – абсолютная температура газа, γ = 1/273K – термический коэффициент давления.
Графики изохорического процесса представлены на рис. 13, 14, 15, 16.
Парциальное давление – давление одной компоненты смеси газов при отсутствии других компонент.
Закон Дальтона: давление смеси газов равно сумме парциальных давлений всех её компонент (р = р1 + р2 + … + рn).
Date: 2016-06-09; view: 826; Нарушение авторских прав