
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

на 2014/2015 учебный год
|
|
Вопросы по Биохимии для лечебного факультета
1. Аминокислоты, классификация и строение протеиногенных кислот. Зависимость заряда аминокислот от рН среды. Изоэлектрическая точка. Характеристика пептидной связи. Первичная структура белков, методы определения. Зависимость биологических свойств белков от первичной структуры. Видовая специфичность первичной структуры белков.
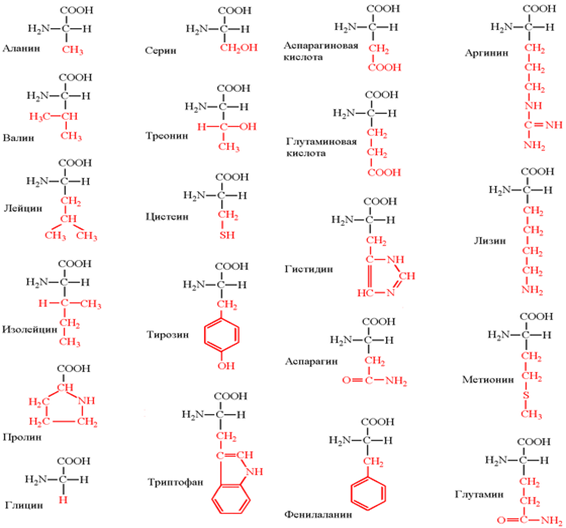
Белки - полимерные молекулы, в которых мономерами служат аминокислоты. В составе белков в организме человека встречают только 20?-аминокислот. Одни и те же аминокислоты присутствуют в различных по структуре и функциям белках. Общая структурная особенность аминокислот - наличие амино- и карбоксильной групп, соединённых с одним и тем же?-углеродным атомом. 19 из 20 аминокислот содержат в?-положении асимметричный атом углерода, с которым связаны 4 разные замещающие группы. В результате эти аминокислоты в природе могут находиться в двух разных изомерных формах - L и D. В составе белков присутствуют только L-изомеры аминокислот.
2. Классификация аминокислот
По химическому строению аминокислоты можно разделить на алифатические, ароматические и гетероциклические.
3. Классификация аминокислот по растворимости их радикалов в воде
Все 20 аминокислот в белках организма человека можно сгруппировать по способности их радикалов растворяться в воде. Радикалы можно выстроить в непрерывный ряд, начинающийся полностью гидрофобными и заканчивающийся сильно гидрофильными. Растворимость радикалов аминокислот определяется полярностью функциональных групп, входящих в состав молекулы.
Аминокислоты с неполярными радикалами
К неполярным (гидрофобным) относят радикалы, имеющие алифатические углеводородные цепи (радикалы аланина, валина, лейцина, изолейцина, пролина и метионина) и ароматические кольца (радикалы фенилаланина и триптофана). Радикалы таких аминокислот в воде стремятся друг к другу или к другим гидрофобным молекулам, в результате чего поверхность соприкосновения их с водой уменьшается.
Аминокислоты с полярными незаряженными радикалами
Радикалы этих аминокислот лучше, чем гидрофобные радикалы, растворяются в воде, так как в их состав входят полярные функциональные группы, образующие водородные связи с водой. К ним относят серии, треонин и тирозин, имеющие гидроксильные группы, аспарагин и глутамин, содержащие амидные группы, и цистеин с его тиольной группой.
Аминокислоты с полярными отрицательно заряженными радикалами
К этой группе относят аспарагиновую и глутаминовую аминокислоты, имеющие в радикале дополнительную карбоксильную группу. Следовательно, радикалы данных аминокислот - анионы.
Аминокислоты с полярными положительно заряженными радикалами
Дополнительную положительно заряженную группу в радикале имеют лизин и аргинин.
Наибольшей растворимостью в воде обладают полярные заряженные радикалы аминокислот.
4. Изменение суммарного заряда аминокислот в зависимости от рН среды
При нейтральных значениях рН все кислотные (способные отдавать Н+) и все основные (способные присоединять Н+) функциональные группы находятся в диссоциированном состоянии. Поэтому в нейтральной среде аминокислоты, содержащие недиссоциирующий радикал, имеют суммарный нулевой заряд. Аминокислоты, содержащие кислотные функциональные группы, имеют суммарный отрицательный заряд, а аминокислоты, содержащие основные функциональные группы, - положительный заряд. Изменение рН в кислую сторону (т.е. повышение в среде концентрации Н+) приводит к подавлению диссоциации кислотных групп. В сильно кислой среде все аминокислоты приобретают положительный заряд. Напротив, увеличение концентрации ОН- групп вызывает отщепление Н+ от основных функциональных групп, что приводит к уменьшению положительного заряда. В сильно щелочной среде все аминокислоты имеют суммарный отрицательный заряд.
?-Аминокислоты могут ковалентно связываться друг с другом с помощью пептидных связей. Пептидная связь образуется между а-карбоксильной группой одной аминокислоты и?-аминогруппой другой, т.е. является амидной связью. При этом происходит отщепление молекулы воды.
Пептидная связь имеет характеристику частично двойной связи, поэтому она короче, чем остальные связи пептидного остова, и вследствие этого мало подвижна. Электронное строение пептидной связи определяет плоскую жёсткую структуру пептидной группы. Плоскости пептидных групп расположены под углом друг к другу. Связь между?-углеродным атомом и?-аминогруппой или?-карбоксильной группой способна к свободным вращениям (хотя ограничена размером и характером радикалов), что позволяет полипептидной цепи принимать различные конфигурации. Пептидные связи обычно расположены в транс-конфигурации, т.е.?-углеродные атомы располагаются по разные стороны от пептидной связи. В результате боковые радикалы аминокислот находятся на наиболее удалённом расстоянии друг от друга в пространстве. Пептидные связи очень прочны и самопроизвольно не разрываются при нормальных условиях, существующих в клетках. В некоторых белках имеются нестандартные модифицированные аминокислоты - производные одной из этих 20 аминокислот. Например, в молекуле коллагена присутствуют гидроксипроизводные лизина и пролина - 5-гидроксилизин и 4-гидроксипролин.
Установление первичной структуры белков включает 2 основных этапа:
определение аминокислотного состава изучаемого белка(Кислотный гидролиз белка, Разделение аминокислот с помощью ионообменной хроматографии, Количественный анализ полученных фракций)
определение аминокислотной последовательности в белке(Определение N-концевой аминокислоты в белке и последовательности аминокислот в олигопептидах, Ферментативное расщепление полипептида по специфическим участкам, Химическое расщепление полипептида по специфическим участкам, Получение аминокислотной последовательности полипептида с помощью перекрывающихся фрагментов)
2. Конформация пептидных цепей (вторичная и третичная структуры). Дисульфидные, водородные, гидрофобные и ионные связи в стабилизации конформации белковой молекулы. Супервторичная структура белков. Четвертичная структура белков. Кооперативные изменения конформации протомеров при функционировании белков. Возможность адаптивной регуляции биологической функции олигомерных белков с помощью аллостерических лигандов. Доменная структура белков. Функционирование белков. Комплементарность центра связывания белков структуре лиганда.
Линейные полипептидные цепи индивидуальных белков за счёт взаимодействия функциональных групп аминокислот приобретают определённую пространственную трёхмерную структуру, называемую "конформация". В белках различают 2 основных типа конформации полипептидных цепей: вторичную и третичную структуры.
Вторичная структура белков - пространственная структура, образующаяся в результате взаимодействий между функциональными группами, входящими в состав пептидного остова. При этом пептидные цепи могут приобретать регулярные структуры двух типов:?-спираль и?-структура.
?-Спираль. В данном типе структуры пептидный остов закручивается в виде спирали за счёт образования водородных связей между атомами кислорода карбонильных групп и атомами азота аминогрупп, входящих в состав пептидных групп через 4 аминокислотных остатка. На один виток?-спирали приходится 3,6 аминокислотных остатка. В образовании водородных связей участвуют практически все атомы кислорода и водорода пептидных групп. Радикалы аминокислот находятся на наружной стороне?-спирали и направлены от пептидного остова в стороны.
?-Структура формируется за счёт образования множества водородных связей между атомами пептидных групп линейных областей одной полипептидной цепи, делающей изгибы, или между разными полипептидными цепями,?-Структура образует фигуру, подобную листу, сложенному "гармошкой", -?-складчатый слой. В?-структурах водородные связи расположены перпендикулярно полипептидной цепи.
Как?-спираль, так и?-структуры обнаружены в глобулярных и фибриллярных белках.
Третичная структура белков - трёхмерная пространственная структура, образующаяся за счёт взаимодействий между радикалами аминокислот, которые могут располагаться на значительном расстоянии друг от друга в полипептидной цепи.
Гидрофобные взаимодействия. При укладке полипептидная цепь белка стремится принять энергетически выгодную форму, характеризующуюся минимумом свободной энергии. Поэтому гидрофобные радикалы аминокислот стремятся к объединению внутри глобулярной структуры растворимых в воде белков. Между ними возникают так называемые гидрофобные взаимодействия, а также силы ван дер Ваальса между близко прилегающими друг к другу атомами. В результате внутри белковой глобулы формируется гидрофобное ядро. Гидрофильные группы пептидного остова при формировании вторичной структуры образуют множество водородных связей, благодаря чему исключается связывание с ними воды и разрушение внутренней, плотной структуры белка.
Ионные и водородные связи
Ионные связи могут возникать между отрицательно заряженными (анионными) карбоксильными группами радикалов аспарагиновой и глутаминовой кислот и положительно заряженными (катионными)
группами радикалов лизина, аргинина или гистидина.
Водородные связи возникают между гидрофильными незаряженными группами (такими как -ОН, -CONH2, SH-группы) и любыми другими гидрофильными группами.
Ковалентные связи.Третичную структуру некоторых белков стабилизируют дисульфидные связи, образующиеся за счёт взаимодействия SH-групп двух остатков цистеина. Эти два остатка цистеина могут находиться далеко друг от друга в линейной первичной структуре белка, но при формировании третичной структуры они сближаются и образуют прочное ковалентное связывание радикалов.
Пространственная структура каждого белка индивидуальна и определяется его первичной структурой. Однако сравнение конформаций разных по структуре и функциям белков выявило наличие у них похожих сочетаний элементов вторичной структуры. Такой специфический порядок формирования вторичных структур называют супервторичной структурой белков. Супервторичная структура формируется за счёт межрадикальных взаимодействий.
Определённые характерные сочетания?-спиралей и?-структур часто обозначают как "структурные мотивы". Они имеют специфические названия: "?-спираль-поворот-?-спираль", "структура?-бочонка", "лейциновая застёжка-молния", "цинковый палец" и др. Специфическое пространственное расположение?-спиралей и?-структур формируется за счёт межрадикальных взаимодействий.
Многие белки содержат в своём составе только одну полипептидную цепь. Такие белки называют мономерами. К мономерным относят и белки, состоящие из нескольких цепей, но соединённых ковалентно, например дисульфидными связями. В то же время существуют белки, состоящие из двух и более полипептидных цепей.гидрофобных, ионных, водородных. Количество и взаиморасположение полипептидных цепей в пространстве называют "четвертичная структура белков". Отдельные полипептидные цепи в таком белке носят название протомеров, или субъединиц. Белок, содержащий в своём составе несколько протомеров, называют олигомерным.
О2 связывается с протомерами гемоглобина через Fe2+, который соединён с четырьмя атомами азота пиррольных колец тема и атомом азота. Связывание О2 с оставшейся свободной координационной связью Fe2+ происходит по другую сторону от плоскости гема в области Гис Е7 (аналогично тому, как это происходит у миоглобина). Гис Е7 не взаимодействует с О2, но обеспечивает оптимальные условия для его связывания. В дезоксигемоглобине благодаря ковалентной связи с белковой частью атом Fe2+ выступает из плоскости гема в направлении Гис F8. Присоединение О2 к атому Fe2+ одного протомера вызывает его перемещение в плоскость гема, за ним перемещаются остаток Гис F8 и полипептидная цепь, в состав которой он входит. Так как протомер связан с остальными протомерами, а белки обладают конформационной лабильностью, происходит изменение конформации всего белка. Конформационные изменения, произошедшие в других протомерах, облегчают присоединение следующей молекулы О2, что вызывает новые конформационные изменения в белке и ускорение связывания следующей молекулы О2. Четвёртая молекула О2 присоединяется к гемоглобину в 300 раз легче, чем первая молекула Изменение конформации (а следовательно и функциональных свойств) всех протомеров олигомерного белка при присоединении лиганда только к одному из них носит название кооперативных изменений конформации протомеров.
Связывание одного протомера с лигандом изменяет конформацию этого протомера, а также всего олигомера и, кроме того, сродство к другим лигандам. Таким образом, функциональная активность олигомерных белков может регулироваться аллостерическими лигандами.
Если полипептидная цепь белка содержит более 200 аминокислот, как правило, её пространственная структура сформирована в виде двух или более доменов. Домен - участок полипептидной цепи, который в процессе формирования пространственной структуры приобрёл независимо от других участков той же цепи кон-формацию глобулярного белка. Так, лёгкая цепь иммуноглобулина G состоит из двух доменов. В некоторых случаях доменами называют отдельные структурные участки полипептидной цепи. Каждый индивидуальный белок, имеющий уникальную первичную структуру и конформацию, обладает и уникальной функцией, отличающей его от bqcx остальных белков. Набор индивидуальных белков выполняет в клетке множество разнообразных и сложных функций.
Необходимое условие для функционирования белков - присоединение к нему другого вещества, которое называют "лиганд". Лигандами могут быть как низкомолекулярные вещества, так и макромолекулы. Взаимодействие белка с лигандом высокоспецифично, что определяется строением участка белка, называемого центром связывания белка с лигандом или активным центром. Активный центр белков - определённый участок белковой молекулы, как правило, находящийся в её углублении ("кармане"), сформированный радикалами аминокислот, собранных на определённом пространственном участке при формировании третичной структуры и способный комплементарно связываться с лигандом. Под комплементарностью понимают пространственное и химическое соответствие взаимодействующих молекул. Лиганд должен обладать способностью входить и пространственно совпадать с конформацией активного центра. Это совпадение может быть неполным, но благодаря конформационной лабильности белка активный центр способен к небольшим изменениям и "подгоняется" под лиганд. Кроме того, между функциональными группами лиганда и радикалами аминокислот, образующих активный центр, должны возникать связи, удерживающие лиганд в активном центре. Связи между лигандом и активным центром белка могут быть как нековалентными (ионными, водородными, гидрофобными), так и ковалентными.
3. Лабильность пространственной структуры белков и их денатурация. Факторы, вызывающие денатурацию.Механизм денатурации.Применение денатурирующих агентов в биологических исследованиях и медицине. Роль шаперонов в предотвращении денатурации белков. Ренативация белков.
Гидрофобные взаимодействия, а также ионные и водородные связи относят к числу слабых. Однако белки состоят из огромного числа атомов, находящихся в постоянном (броуновском) движении, что приводит к небольшим перемещениям отдельных участков полипептидной цепи, которые обычно не нарушают общую структуру белка и его функции. Следовательно, белки обладают конформационной лабильностью - склонностью к небольшим изменениям конформации за счёт разрыва одних и образования других слабых связей. Разрыв большого количества слабых связей в молекуле белка приводит к разрушению её на-тивной конформации. Так как разрыв связей под действием различных факторов носит случайный характер, то молекулы одного индивидуального белка приобретают в растворе форму случайно сформировавшихся беспорядочных клубков, отличающихся друг от друга трёхмерной структурой. Потеря нативной конформации сопровождается утратой специфической функции белков. Этот процесс носит название денатурации белков. При денатурации белков не происходит разрыва пептидных связей, т.е. первичная структура белка не нарушается.
В денатурированном белке гидрофобные радикалы, которые в нативной структуре молекулы спрятаны внутри гидрофобного ядра, оказываются на поверхности. При достаточно высокой концентрации белка и отсутствии сильного отталкивающего заряда молекулы могут объединяться друг с другом гидрофобными взаимодействиями, при этом растворимость белка снижается и происходит образование осадка.
высокая температура (более 50 °С), увеличивающая тепловое движение атомов в молекуле и приводящая к разрыву слабых связей;
интенсивное встряхивание раствора, приводящее к соприкосновению белковых молекул с воздушной средой на поверхности раздела фаз и изменению конформации этих молекул;
органические вещества (например, этиловый спирт, фенол и его производные) способны взаимодействовать с функциональными группами белков, что приводит к их конформа-ционным изменениям. Для денатурации белков в биохимических исследованиях часто используют мочевину или гуанидинхлорид, которые образуют водородные связи с амино- и карбонильными группами пептидного остова и некоторыми функциональными группами радикалов аминокислот. Происходит разрыв связей, участвующих в формировании вторичной и третичной структуры нативных белков, и образование новых связей с химическими реагентами;
кислоты и щелочи, изменяя рН среды, вызывают перераспределение связей в молекуле белка;
соли тяжёлых металлов (такие как медь, ртуть, серебро, свинец и др.) образуют прочные связи с важными функциональными группами белков (чаще всего с -SH), изменяя их конформацию и активность;
детергенты - вещества, содержащие гидрофобный углеводородный радикал и гидрофильную функциональную группу (такие вещества называют амфифильными). К наиболее известным детергентам относят различные мыла.
В биохимических исследованиях перед определением в биологическом материале низкомолекулярных соединений из раствора обычно удаляют белки. Для этой цели чаще всего используют трихлоруксусную кислоту, её можно также использовать для денатурации ферментов в целях прекращения ферментативной реакции.В медицине - для стерилизации медицинских инструментов и материала, а также в качестве антисептиков. Фенол и его производные (крезол, резорцин) относят к известным антисептикам ароматического ряда. Обладающие высокой гидрофобностью, они эффективно действуют на вегетативные формы бактерий и грибы, вызывая денатурацию их белков. Раствор крезола в калийном мыле известен как препарат лизол, применяемый в качестве дезинфицирующего средства. Берёзовый дёготь - одна из основных составных частей мази Вишневского, содержит в своем составе фенол. Препарат, используемый для лечения ран, обладает высоким антимикробным действием. Значительное количество антисептиков представлено солями тяжёлых металлов. Их антимикробное действие связано с тем, что уже в довольно низких концентрациях они взаимодействуют с белками микроорганизмов, блокируют их SH-группы и изменяют их конформа-цию.(HgCl2). Её используют для обработки рук и дезинфекции помещений. Антимикробными свойствами обладают и препараты серебра, такие как ляпис (AgNO3), колларгол (серебро коллоидальное), применяемые для обработки слизистых оболочек при инфекционных заболеваниях. Однако если путём диализа очистить рибонуклеазу от денатурирующих агентов и?-меркаптоэтанола, ферментативная активность белка постепенно восстанавливается. Этот процесс называется ренатурацией, или ренативацией белка.
В процессе синтеза полипептидных цепей, транспорта их через мембраны, при сборке олигомерных белков возникают промежуточные нестабильные конформации, склонные к агрегации. На вновь синтезированном полипептиде имеется множество гидрофобных радикалов, которые в трёхмерной структуре спрятаны внутри молекулы. Поэтому на время формирования нативной конформации реакционно-способные аминокислотные остатки одних белков должны быть отделены от таких же групп других белков. Шапероны, участвующие в защите клеточных белков от денатурирующих воздействий, как уже говорилось выше, относят к белкам теплового шока (БТШ). При действии различных стрессовых факторов (высокая температура, гипоксия, инфекция, УФО, изменение рН среды, изменение моляр-ности среды, действие токсичных химических веществ, тяжёлых металлов и т.д.) в клетках усиливается синтез БТШ. Имея высокое сродство к гидрофобным участкам частично денатурированных белков, они могут препятствовать их полной денатурации и восстанавливать натив-ную конформацию белков. Установлено, что кратковременные стрессовые воздействия увеличивают выработку БТШ и повышают устойчивость организма к длительным стрессовым воздействиям. Так, кратковременная ишемия сердечной мышцы в период бега при умеренных тренировках значительно повышает устойчивость миокарда к длительной ишемии, вызванной стенокардией или закупоркой сосудов сердца тромбом.
4. Физико-химические свойства белков: молекулярная масса, размеры и форма белковой молекулы, растворимость. Факторы стабилизации белковых растворов. Механизм возникновения электрического заряда белков, зависимость от рН. Изоэлектрическая точка белка.
5. Индивидуальные белки различаются по своим физико-химическим свойствам: форме молекул, молекулярной массе, суммарному зарядумолекулы, соотношению полярных и неполярных групп на поверхности нативной молекулы белка, растворимости белков, а также степени устойчивости к воздействию денатурирующих агентов. 1. Различия белков по форме молекул. Как уже говорилось выше, по форме молекул белки делят на глобулярные и фибриллярные. Глобулярные белки имеют более компактную структуру, их гидрофобные радикалы в большинстве своём спрятаны в гидрофобное ядро, и они значительно лучше растворимы в жидкостях организма, чем фибриллярные белки (исключение составляют мембранные белки). 2. Различия белков по молекулярной массе. Белки - высокомолекулярные соединения, но могут сильно отличаться по молекулярной массе, которая колеблется от 6000 до 1 000 000 Д и выше. Молекулярная масса белка зависит от количества аминокислотных остатков в полипептидной цепи, а для олигомерных белков - и от количества входящих в него протомеров (или субъединиц). 3. Суммарный заряд белков. Белки имеют в своём составе радикалы лизина, аргинина, гистидина, глутаминовой и аспарагиновой кислот, содержащие функциональные группы, способные к ионизации (ионогенные группы). Кроме того, на N- и С-концах полипептидных цепей имеются α-амино- и α-карбоксильная группы, также способные к ионизации. Суммарный заряд белковой молекулы зависит от соотношения ионизированных анионных радикалов Глу и Асп и катионных радикалов Лиз, Apr и Гис. Степень ионизации функциональных групп этих радикалов зависит от рН среды. При рН раствора около 7 все ионогенные группы белка находятся в ионизированном состоянии. В кислой среде увеличение концентрации протонов (Н+) приводит к подавлению диссоциации карбоксильных групп и уменьшению отрицательного заряда белков: -СОО- + Н+ → -СООН. В щелочной среде связывание избытка ОН" с протонами, образующимися при диссоциации NH3+с образованием воды, приводит к уменьшению положительного заряда белков.Значение рН, при котором белок приобретает суммарный нулевой заряд, называют "изоэлектрическая точка" и обозначают как pI. В изоэлектрической точке количество положительно и отрицательно заряженных групп белка одинаково, т.е. белок находится в изоэлектрическом состоянии.Так как большинство белков в клетке имеет в своём составе больше анионогенных групп (-СОО-), то изоэлектрическая точка этих белков лежит в слабокислой среде. Изоэлектрическая точка белков, в составе которых преобладают катионогенные группы, находится в щелочной среде. Наиболее яркий пример таких внутриклеточных белков, содержащих много аргинина и лизина, - гистоны, входящие в состав хроматина. 4. Растворимость белков. Растворимость белков в воде зависит от всех перечисленных выше свойств белков: формы, молекулярной массы, величины заряда, соотношения полярных и неполярных функциональных групп на поверхности белка. Кроме этого, растворимость белка определяется составом растворителя, т.е. наличием в растворе других растворённых веществ. Например, некоторые белки легче растворяются в слабом солевом растворе, чем в дистиллированной воде. С другой стороны, увеличение концентрации нейтральных солей может способствовать вьшадению определённых белков в осадок. Денатурирующие агенты, присутствующие в растворе, также снижают растворимость белков.
Большинство белков гидрофильны. Однако белковые молекулы имеют очень большие размеры, поэтому белки не могут образовывать истинных растворов, а только коллоидные. Факторы стабилизации белка в растворе.1) Гидратная Оболочка - это слой молекул воды, определенным образом ориентированных на поверхности белковой молекулы. Поверхность большинства белковых молекул заряжена отрицательно, и диполи молекул воды притягиваются к ней своими положительно заряженными полюсами. 2) Заряд Белковой Молекулы. Поверхность большинства белковых молекул заряжена потому, что в каждой молекуле белка есть свободные заряженные СОО- и NH3+ группы.
6. Методы выделения индивидуальных белков: избирательное осаждение солями и органическими растворителями, гель-фильтрация, ионообменная хроматография, аффинная хроматография. 
7. Многообразие белков. Глобулярные и фибриллярные белки. Простые белки: общая характеристика. Сложные белки: классификация, общая характеристика. Классификация белков по биологическим функциям. Семейства родственных белков (сериновые протеазы, иммуноглобулины).

8. Иммуноглобулины, особенности строения, избирательность взаимодействия с антигеном. Многообразие антигенсвязывающих участков Н и L цепей. Классы иммуноглобулинов, особенности строения и функционирования.
Суперсемейство иммуноглобулинов
В работе иммунной системы огромную роль играют белки, относящиеся к суперсемейству иммуноглобулинов. Это суперсемейство включает по крайней мере три больших семейства белков, участвующих в иммунной защите организма: семейство иммуноглобулинов, семейство Т-клеточных антигенраспознающих рецепторов и белки главного комплекса гистосовместимости I и II классов. Основной критерий включения белков в суперсемейство иммуноглобулинов - их доменная организация, достоверная гомология аминокислотных последовательностей и пространственных структур отдельных доменов. Кроме того, белки этого суперсемейства имеют схожие функции: иммуноглобулины взаимодействуют с чужеродными структурами, находящимися в крови, лимфе, межклеточной жидкости или секретах желёз, а рецепторы Т-лимфоцитов и белки главного комплекса гистосовместимости - с антигенами, находящимися на поверхности клеток данного организма.
3.Семейство иммуноглобулинов. Иммуноглобулины, или антитела, - специфические белки, вырабатываемые В-лимфоцитами в ответ на попадание в организм чужеродных структур, называемых антигенами. Все иммуноглобулины характеризуются общим планом строения, который мы рассмотрим на примере строения IgG. Молекула IgG состоит из четырёх полипептидных цепей: двух идентичных лёгких (L), содержащих около 220 аминокислотных остатков, и двух тяжёлых (Н), состоящих из 440 аминокислот каждая. Все 4 цепи соединены друг с другом множеством нековалентных и четырьмя дисульфидными связями. Поэтому молекулу IgG относят к мономерам. Лёгкие цепи IgG состоят из 2 доменов: вариабельного (VL), находящегося в N-концевой области полипептидной цепи, и константного (CL), расположенного на С-конце. Каждый из доменов состоит из 2 слоев с β-складчатой структурой, где участки полипептидной цепи лежат антипараллельно. β-Слои связаны ковалентно дисульфидной связью примерно в середине домена. Тяжёлые цепи IgG имеют 4 домена: один вариабельный (VH), находящийся на N-конце, и три константных (СН1, СН2, СH3). Домены тяжёлых цепей IgG имеют гомологичное строение с доменами лёгких цепей. Между двумя константными доменами тяжёлых цепей СH1, и СН2 есть участок, содержащий большое количество остатков пролина, которые препятствуют формированию вторичной структуры и взаимодействию соседних Н-цепей на этом отрезке. Этот участок называют "шарнирной областью"; он придаёт молекуле гибкость. Между вариабельными доменами тяжёлых и лёгких цепей находятся два идентичных участка, связывающих два одинаковых специфических антигена; поэтому такие антитела часто называют "биваленты". В связывании антигена с антителом участвует не вся аминокислотная последовательность вариабельных доменов обеих цепей, а всего лишь 20-30 аминокислот, расположенных в гипервариабельных областях каждой цепи. Именно эти области определяют уникальные способности каждого клона антител взаимодействовать с соответствующим (комплементарным) антигеном. Основные функции антител - обнаружение и связывание чужеродных антигенов, находящихся в организме вне его клеток (в крови, лимфе, межклеточной жидкости, в слизистых секретах). Это происходит с помощью специфических антигенсвязывающих участков разных клонов иммуноглобулинов. Кроме, того, благодаря связыванию антигена с антителом облегчается процесс дальнейшего разрушения чужеродных веществ. Специфичность пути разрушения комплекса антиген-антитело зависит от класса антител.
Классы иммуноглобулинов. Существует 5 классов тяжёлых цепей иммуноглобулинов, отличающихся по строению константных доменов: α, δ, ξ, γ и μ. В соответствии с ними различают 5 классов иммуноглобулинов: A, D, Е, G и М. Особенности строения тяжёлых цепей придают их "шарнирным участкам" и С-концевым областям характерную для каждого класса конформацию. Связывание антигена с антителом изменяет конформацию константных доменов тяжёлых цепей, что определяет путь разрушения комплекса в организме (связывание с белками системы комплемента или поглощение комплекса фагоцитирующими клетками).
Иммуноглобулины М - первый класс антител, синтезирующийся в развивающихся В-лимфоцитах. Различают 2 формы иммуноглобулинов М: мономерная, мембранно-связанная форма и пентамерная, секретируемая В-лимфоцитами в кровь. Мембранно-с вязанная форма иммуноглобулинов М. Созревающие В-лимфоциты синтезируют мономерные бивалентные молекулы IgM, по структуре похожие на рассматриваемые выше IgG, которые встраиваются в плазматическую мембрану клеток и играют роль первых антиген-распознающих рецепторов. Прикрепление IgM к мембране осуществляется с помощью гидрофобного участка, находящегося в С-концевой ("хвостовой") области тяжёлых цепей, содержащей 25 гидрофобных аминокислотных остатков. Взаимодействие антигена с рецептором на поверхности В-лимфоцита вызывает его размножение и образование целого клона лимфоцитов, происходящих из одной, стимулированной антигеном клетки. Этот клон В-лимфоцитов будет вырабатывать иммуноглобулины с одинаковыми антигенсвязывающими участками. Однако В-лимфоциты способны переключаться на выработку других классов антител. Секреторная форма иммуноглобулинов М. Когда В-лимфоциты впервые встречаются в жидкостях организма с неизвестным ранее антигеном, они синтезируют и секретируют в кровь IgM, которые содержат пять мономерных субъединиц, связанных друг с другом дисульфидными связями и дополнительной полипептидной J-цепью. В тяжёлых цепях их мономеров отсутствует гидрофобная "хвостовая" часть. Пентамерная молекула содержит 10 участков связывания с антигеном, что облегчает вероятность прикрепления Неизвестного ранее антигена к иммуноглобулину. Взаимодействие антигена с IgM изменяет его конформацию и индуцирует связывание его "хвостовой" области с первым компонентом системы комплемента. Если антиген расположен на поверхности микроорганизма, активирование системы комплемента вызывает нарушение целостности клеточной мембраны и гибель бактериальной клетки. Иммуноглобулины G. В количественном отношении IgG доминируют в крови и составляют около 75% от общего количества этих белков. У человека обнаружено 4 подкласса IgG: IgGg1, IgGg2, IgGg3, IgGg4. IgG не только эффективно связывают и инактивируют чужеродные молекулы и клетки, попавшие в организм, но также облегчают их дальнейшее уничтожение. Конформационные изменения в "хвостовой" области IgG после его взаимодействия с антигеном приводят к связыванию и активации белков системы комплемента. Кроме того, С-концевая область IgG способна взаимодействовать со специфическими рецепторами макрофагов и нейтрофилов, что приводит к фагоцитозу комплексов антиген-антитело и разрушению их в фагосомах. IgG - единственный класс антител, способный проникать через плацентарный барьер и обеспечивать внутриутробную защиту плода от инфекций. Иммуноглобулины А. Основной класс антител, присутствующий в секретах желёз организма (слюны, молока, пищеварительного сока, секретов дыхательных путей). На базальной поверхности эпителиальных клеток димер IgA специфически взаимодействует с белками клеточной поверхности, называемыми секреторным компонентом. Образующийся комплекс посредством эндоцитоза поглощается внутрь клетки и перемещается к апикальной части. Здесь комплекс подвергается действию протеолитических ферментов, и свободный димер высвобождается во внеклеточное пространство. Образующийся при взаимодействии IgA с антигеном комплекс не взаимодействует с белками системы комплемента и фагоцитирующими клетками, но препятствует прикреплению антигенов к поверхности эпителиальных клеток и проникновению их в организм. Иммуноглобулины Е. После синтеза и секреции в кровь В-лимфоцитами IgE связываются своими С-концевыми участками с соответствующими рецепторами на поверхности тучных клеток и базофилов. В результате они становятся рецепторами антигенов на поверхности данных клеток. После присоединения антигена хотя бы к двум антигенсвязывающим участкам двух соседних IgE клетка получает сигнал к секреции биологически активных веществ (серотонина, гистамина), хранящихся в секреторных пузырьках. Выброс этих веществ в значительной мере ответственен за развитие воспалительной реакции, а также таких аллергических реакций, как бронхиальная астма, крапивница, сенная лихорадка. Увеличение количества IgE может предшествовать развитию аллергических реакций. Иммуноглобулины D. IgD обнаружены в крови в очень малых количествах. Мономерные белки играют роль рецепторов В-лимфоцитов; других функций у IgD пока не выявлено.
9. Биуретовый метод количественного определения содержания белка в сыворотке крови, диагностическое значение. Возрастные особенности нормальных величин белков сыворотки крови. Гипер- и гипопротеинемические состояния. Электрофорез белков сыворотки крови. Белковый спектр в норме и патологии.
Белки реагируют в щелочной среде с сульфатом меди с образованием комплексных соединений, окрашенных в фиолетовый цвет. По интенсивности окрашивания, которое пропорционально количеству белка, определяют содержание его в сыворотке крови.
В широкой клинической практике определяют, как правило, общее содержание белка в плазме крови и содержание в крови белковых фракций. Общее количество белка в плазме крови в норме составляет 55—85 г/л.
Гипопротеинемия возникает вследствие:
недостаточного поступления белка;
повышенной потери белка;
нарушения образования белка в организме;
сочетания различных из перечисленных причин.
Повышенная потеря белка происходит при различных заболеваниях почек (особенно с нефротическим синдромом), кровопотерях, новообразованиях. Нарушение образования белка возможно при недостаточности функции печени (гепатиты, циррозы, подострая дистрофия печени). Небольшая степень гипопротеинемии возможна при беременности вследствие того, что объем циркулирующей крови увеличивается значительнее, чем общее количество белка плазмы.
Гиперпротеинемия нередко развивается как следствие дегидратации в результате потери части внутрисосудистой жидкости. Это происходит при тяжелых травмах, обширных ожогах, холере. При острых инфекциях содержание белка часто повышается от дегидратации и одновременного выброса белков острой фазы. При хронических инфекциях содержание белка в крови может нарастать в результате иммунного процесса с увеличением концентрации иммуноглобулинов. Гиперпротеинемия наблюдается также при появлении в крови парапротеинов — патологических белков, вырабатываемых в большом количестве при миеломной болезни, при болезни Вальденстрема.
Методом электрофореза на ацетилцеллюлозе или геле агарозы белки плазмы крови можно разделить на альбумины (55-65%), α1-глобулины (2- 4%), α2 -глобулины (6-12%), β-глобулины (8-12%) и γ-глобулины (12-22%)
При ряде заболеваний происходит изменение соотношения распределения белковых фракций при электрофорезе по сравнению с нормой. Такие изменения называют диспротеинемиями, однако их интерпретация часто имеет относительную диагностическую ценность. Например, характерное для нефротического синдрома снижение альбуминов, α1- и γ-глобулинов и увеличение α2- и β-глобулинов отмечают и при некоторых других заболеваниях, сопровождающихся потерей белков. При снижении гуморального иммунитета уменьшение фракции γ-глобулинов свидетельствует об уменьшении содержания основного компонента иммуноглобулинов - IgG, но не отражает динамику изменений IgA и IgM. Содержание некоторых белков в плазме крови может резко увеличиваться при острых воспалительных процессах и некоторых других патологических состояниях (травмы, ожоги, инфаркт миокарда). Такие белки называют белками острой фазы, так как они принимают участие в развитии воспалительной реакции организма. Основной индуктор синтеза большинства белков острой фазы в гепатоцитах - полипептид интерлейкин-1, освобождающийся из мононуклеарных фагоцитов. К белкам острой фазы относят С-реактивный белок, называемый так, потому что он взаимодействует с С-полисахари-дом пневмококков, α1-антитрипсин, гаптоглобин, кислый гликопротеин, фибриноген. Известно, что С-реактивный белок может стимулировать систему комплемента, и его концентрация в крови, например, при обострении ревматоидного артрита может возрастать в 30 раз по сравнению с нормой. Белок плазмы крови а,-антитрипсин может инактивировать некоторые протеазы, освобождающиеся в острой фазе воспаления.
10. Ферменты, специфичность действия. Классификация и номенклатура ферментов. Структурно-функциональная организация ферментных белков. Активный и аллостерический центры ферментов. Механизм действия ферментов.
Ферме́нты — обычно белковые молекулы или молекулы РНК или их комплексы, катализирующие химические реакции в живых системах. Биологическая функция фермента, как и любого белка, обусловлена наличием в его структуре активного центра. Лиганд, взаимодействующий с активным центром фермента, называют субстратом. В активном центре фермента есть аминокислотные остатки, функциональные группы которых обеспечивают связывание субстрата, и аминокислотные остатки, функциональные группы которых осуществляют химическое превращение субстрата. Условно эти группы обозначают как участок связывания субстрата и каталитический участок. Специфичность - наиболее важное свойство ферментов, определяющее биологическую значимость этих молекул. Различают субстратную и каталитическую специфичности фермента, определяемые строением активного центра.
Субстратная специфичность: абсолютную субстратную специфичность(уреаза); групповую субстратную специфичность(панкреатическая липаза); стереоспецифичность(к D-сахарам, L-аминокислотам)
Классы ферментов
1. Оксидоредуктазы (Дегидрогеназы. Оксидазы. Оксигеназы). Катализируют различные окислительно-восстановительные реакции с участием 2 субстратов (перенос е- или атомов водорода с одного субстрата на другой). Систематическое наименование ферментов составляют по формуле "донор: акцептороксидоредуктаза»
2. Трансферты. Катализируют перенос функциональных групп от одного соединения к другому. Подразделяют в зависимости от переносимой группы. Название этих ферментов составляют по формуле "донор: ацетрофэкспортируемая группатрансфераза".
3. Гидролазы. Катализируют реакции гидролиза (расщепления ковалентной связи с присоединением молекулы воды по месту разрыва). Подразделяют в зависимости от расщепляемой связи. Наименование ферментов составляют по формуле "субстрат-гидролаза" или прямым присоединением к названию субстрата суффикса "аза".
4. Лиазы. К лиазам относят ферменты, отщепляющие от субстратов негидролитическим путём определённую группу (при этом могут отщепляться СО2, Н2О, NH2,SН2и др.) или присоединяющие чаще всего молекулу воды по двойной связи. Наименование ферментов составляют по формуле "субстрат-отщепляемая или присоединяемая группировка".
Ферменты по химической структуре являются простыми и сложными белками. Ферменты, которые являются простыми белками, состоящие только из остатков аминокислот, поэтому они еще называются однокомпонентными. Ферменты, которые являются сложными белками, называются двухкомпонентными: они состоят из белка и небелковой части. Белковая часть двухкомпонентных ферментов называется апоферментом, а молекула в целом - холоферментом. Небелковый компонент принято называть кофактором. Сочетание белковой части фермента с небелковой происходит за счет ионных, водородных и изредка ковалентных связей, а также гидрофобных взаимодействий. В ферменте присутствует активный центр, в некоторых случаях аллостерический центр.
Аллостерический центр- центр регуляции активности фермента, который пространственно отделён от активного центра.
Механизм действия ферментов может быть рассмотрен с двух позиций: с точки зрения изменения энергетики химических реакций и с точки зрения событий в активном центре. Ферменты обеспечивают высокую скорость реакций при оптимальных условиях, существующих в клетке, путём понижения уровня Еа. Таким образом, ферменты снижают высоту энергетического барьера, в результате возрастает количество реакционно-способных молекул, следовательно, увеличивается скорость реакции. В механизме ферментативного катализа решающее значение имеет образование нестойких промежуточных соединений - фермент-субстратный комплекс ES, подвергающийся превращению в нестабильный переходный комплекс ЕР, который почти мгновенно распадается на свободный фермент и продукт реакции. Таким образом, биологические катализаторы (ферменты) не изменяют свободную энергию субстратов и продуктов и поэтому не меняют равновесие реакции. Этапы ферментативного катализа: E+S -> ES->EP-> E+P. Первый этап: теория Фишера (ключ-замок), Кошланда(индуцированного взаимодействия). Третий этап самый медленный.
11. Характеристика кофакторов ферментов: строение и классификация. Коферменты НАД, НАДФ, ФАД, ФМН, КоАSH, ГДФ, пиридоксальфосфат, ТГФК: химическая природа, витамины-предшественники, катализируемые реакции.
NAD представляет собой динуклеотид и состоит из двух нуклеотидов, соединённых своими фосфатными группами. Один из нуклеотидов в качестве азотистого основания содержит аденин, другой — никотинамид. Никотинамидадениндинуклеотид существует в двух формах: окисленной (NAD+) и восстановленной (NADH). В метаболизме NAD задействован в окислительно-восстановительных реакциях, перенося электроны из одной реакции в другую. В живых организмах NAD синтезируется de novo из аминокислот аспартата или триптофана. Другие предшественники кофермента поступают в организм экзогенно, как, например, витамин ниацин (витамин В3) с пищей.
NADP — кофермент, отличающийся от NAD содержанием ещё одного остатка фосфорной кислоты, присоединённого к гидроксилу одного из остатков D-рибозы, кофермент некоторых дегидрогеназ — ферментов, катализирующих окислительно-восстановительные реакции в живых клетках. НАДФ принимает на себя водород и электроны окисляемого соединения и передает их на другие вещества. Витамин РР принимает участие в синтезе НАД и НАДФ.
ФАД-кофермент многих оксидоредуктаз, представляющий собой производное рибофлавина (витамина В2), содержащее два остатка фосфорной кислоты. Сукцинатдегидрогеназная реакция.
Флавинмононуклеотид образуется из рибофлавина (витамина В2) ферментом рибофлавин киназой и является простетической группой различных оксидоредуктаз.
Кофермент А (коэнзим А) — кофермент ацетилирования; один из важнейших коферментов, принимающий участие в реакциях переноса ацильных групп при синтезе и окислении жирных кислот и окислении пирувата в цикле лимонной кислоты. Кофермент А синтезируется из пантотеновой кислоты (витамина B5) и цистеина.
Гуанозиндифосфат (ГДФ, GDP,) — нуклеотид, эфир пирофосфорной кислоты с гуаниловым нуклеозидом. ГДФ состоит из пирофосфата, сахара пентозы рибозы и азотистого основания гуанина. Разрьш тиоэфирной связи здесь сопряжен с реакцией, в ходе которой происходит запасание энергии с фосфорилированием гуанозиндифосфата (GDP) до гуанозинтрифосфата (GTP).
пиридоксальфосфат — кофактор ферментов, которые катализируют декарбоксилирование и трансаминирование аминокислот. Образуется из витамина B6. особенно важна его роль в метаболизме триптофана, глицина, серина, глутаминовой кислоты и серосодержащих аминокислот. Пиридоксальфосфат необходим также для синтеза предшественника гема - дельта-АЛК.
ТГФК(тетрагидрофолиевая кислота). Производное витамина В9, коферментные функции ТГФК непосредственно связаны с переносом одноуглеродных групп. Имеются данные, что производные ТГФК участвуют в переносе одно-углеродных фрагментов при биосинтезе метионина и тимина.
12. Ферментативный катализ. Зависимость скорости ферментативных реакций от температуры, рН, концентраций фермента и субстрата. Константа Михаэлиса, физический смысл. Единицы выражения активности ферментов. Принципы количественного определения активности ферментов.
ФЕРМЕНТАТИВНЫЙ КАТАЛИЗ - ускорение биохим. р-ций при участии белковых макромолекул, называемых ферментами (энзимами). Выделяют 2 основных механизма ферментативного катализа: кислотно-основной катализ и ковалентный катализ. Концепция кислотно-основного катализа объясняет ферментативную активность участием в химической реакции кислотных групп (доноры протонов) и/или основных групп (акцепторы протонов). Кислотно-основной катализ - часто встречающееся явление. Аминокислотные остатки, входящие в состав активного центра, имеют функциональные группы, проявляющие свойства как кислот, так и оснований. Примером можно привести фермент алкогольдегидрогеназу печени, катализирующую реакцию окисления спирта Ковалентный катализ основан на атаке нуклеофильных (отрицательно заряженных) или электрофильных (положительно заряженных) групп активного центра фермента молекулами субстрата с формированием ковалентной связи между субстратом и коферментом или функциональной группой аминокислотного остатка (как правило, одной) активного центра фермента.Трипсин, химотрипсин и тромбин, - пример механизма ковалентного катализа, когда ковалентная связь образуется между субстратом и аминокислотным остатком серина активного центра фермента.
Повышение температуры до определённых пределов оказывает влияние на скорость ферментативной реакции, подобно влиянию температуры на любую химическую реакцию. С повышением температуры ускоряется движение молекул, что приводит к повышению вероятности взаимодействия реагирующих веществ. Кроме того, температура может повышать энергию реагирующих молекул, что также приводит к ускорению реакции. Однако скорость химической реакции, катализируемая ферментами, имеет свой температурный оптимум, превышение которого сопровождается понижением ферментативной активности, возникающим из-за термической денатурации белковой молекулы. Для большинства ферментов человека оптимальна температура 37-38 °С.
Для каждого фермента существует значение рН, при котором наблюдается его максимальная активность. Отклонение от оптимального значения рН приводит к понижению ферментативной активности. Влияние рН на активность ферментов связано с ионизацией функциональных групп аминокислотных остатков данного белка, обеспечивающих оптимальную конформацию активного центра фермента.
При проведении ферментативной реакции в условиях избытка субстрата скорость реакции будет зависеть от концентрации фермента. Графическая зависимость такой реакции имеет вид прямой линии.
Если концентрацию ферментов оставить постоянной, изменяя только количество субстрата, то график скорости ферментативной реакции описывают гиперболой. При увеличении количества субстрата начальная скорость возрастает. Когда фермент становится полностью насыщенным субстратом, т.е. происходит максимально возможное при данной концентрации фермента формирование фермент-субстратного комплекса, наблюдают наибольшую скорость образования продукта. Дальнейшее повышение концентрации субстрата не приводит к увеличению образования продукта, т.е. скорость реакции не возрастает. Данное состояние соответствует максимальной скорости реакции Vmax. Таким образом, концентрация фермента - лимитирующий фактор в образовании продукта. Это наблюдение легло в основу ферментативной кинетики, разработанной учёными Л. Михаэлисом и М. Ментен в 1913 г.
Ферментативный процесс можно выразить следующим уравнением: 
где k1 - константа скорости образования фермент-субстратного комплекса; k-1 - константа скорости обратной реакции, распада фермент-субстратного комплекса; k2 - константа скорости образования продукта реакции. Следующее соотношение констант скоростей (k-1 + k2)/k1 называют константой Михаэлиса и обозначают Кm. Таким образом, константа Михаэлиса численно равна концентрации субстрата, при которой достигается половина максимальной скорости. Зависимость скорости ферментативной реакции от концентрации субстрата выражается следующим уравнением V = Vmax[S] /Km + [S]
Однако количество фермента часто невозможно определить в абсолютных величинах, поэтому на практике пользуются условными величинами, характеризующими активность фермента: одна международная единица активности (ME) соответствует такому количеству фермента, которое катализирует превращение 1 мкмоль субстрата за 1 мин при оптимальных условиях проведения ферментативной реакции. В 1973 г. была принята новая единица активности ферментов: 1 катал (кат), соответствующий такому количеству катализатора, которое превращает 1 моль субстрата за 1 с. 1 кат = 6х107 ME, 1 ME = 16,67 нкат.
Определение количественного содержания ферментов в биологических объектах представляет известные трудности, поскольку, за редким исключением, ферменты в тканях присутствуют в ничтожно малых концентрациях. Поэтому о количестве ферментов судят по скорости катализируемой реакции в определенных, согласованных условиях измерения. При оптимальных условиях температуры, рН среды и полном насыщении фермента субстратом скорость катализируемой реакции пропорциональна концентрации фермента. О скорости ферментативной реакции судят или по скорости убыли субстрата, или по скорости образования продукта реакции.
13. Внутриклеточная локализация ферментов. Различия ферментного состава органов и тканей. Органоспецифичные ферменты. Понятие о мультиферментных комплексах. Мультисубстратные реакции.
Внутриклеточные ферменты локализованы либо в клеточных органеллах, либо в комплексе с надмолекулярными структурами. Установлено, что в ядре клетки локализованы ферменты, принимающие участие в синтезе РНК, ДНК; с митохондриями связаны ферменты окисления жирных кислот, продуктов распада углеводов, ЦТК т.е. ферменты, играющие важную роль в биоэнергетике клетки; в лизосомах в основном содержатся ферменты гидролиза; с рибосомами связаны ферменты белкового синтеза, в цитоплазме: гликолиз, глюконеогенез, синтез белка, синтез ЖК, синтез холестерина.
Органоспецифические ферменты преимущественно локализованы в определенных органах. Как правило, эти ферменты катализируют реакции, обеспечивающие специфические функции органа. В клетках других органов этих ферментов нет или только находят их следы. Выход органоспецифических ферментов в кровь сигнализирует о поражении определенного органа. АЛТ и A T — органоспецифические ферменты, в норме в крови активность их мала — 5—40 ЕД/л. Эти различия, по-видимому, связаны с метаболической специализацией. Такие органоспецифические ферменты используются для клинической диагностики например, в ряде случаев при повреждениях мышечной ткани наблюдается увеличение количества креатинкиназы в сыворотке крови.
Мультиферментные комплексы — это объединение нескольких ферментов, катализирующих последовательные превращения субстрата (цепочечные реакции). Часто составляющие комплекс энзимы в строгой последовательности фиксированы в мембранах, в частности, эндоплазматической сети и аппарата Гольджи (рибосомы, синтетаза жирных кислот и др.). Конвейерный принцип работы значительно ускоряет получение конечного продукта реакции и позволяет более эффективно регулировать процесс.
Большинство ферментов катализирует реакции, в которых участвует более чем один субстрат. В случае если кофермент не является простетической группой, его также можно рассматривать как ещё один субстрат. Следовательно, участников ферментативной реакции может быть несколько: непосредственно фермент, несколько субстратов и кофермент.
В этих случаях механизм ферментативной реакции, как правило, может идти по одному из двух путей: по механизму "пинг-понг" (механизму двойного замещения) или последовательному. Субстрат А, взаимодействуя с ферментом (Е), превращается в продукт (Р1). Фермент остаётся в результате этого преобразования не в нативной форме, а в изменённой (Е') в результате модификации кофермента. Далее к активному центру Е' присоединяется субстрат В, подвергающийся преобразованию в продукт (Р2) с высвобождением нативной формы фермента (Е). Хороший пример механизма "пинг-понг" - реакции трансаминирования с участием ферментов аминотрансфераз.
В случае последовательного механизма для протекания ферментной реакции требуется одновременно взаимодействие двух субстратов. В этом случае возможно присоединение субстратов двумя различными путями:
Механизм упорядоченного взаимодействия субстрата с активным центром фермента:
Первым в активный центр фермента присоединяется субстрат А, облегчая присоединение субстрата В. После химической модификации также наблюдают определённый порядок высвобождения продуктов реакции.
Механизм случайного взаимодействия субстрата с активным центром фермента:
Приоритетности за взаимодействие субстратов А и В в активном центре фермента нет (каждый субстрат имеет свой центр связывания в активном центре). Также нет строгой закономерности высвобождения продуктов реакции.
Примером последовательного упорядоченного механизма может быть реакция дегидрирования с участием коферментов NAD+, NADP+.
14. Понятие о метаболизме и метаболических путях. Способы регуляции скорости ферментативной реакции. Способы регуляции каталитической активности молекулы фермента. Ингибиторы ферментов. Обратимое и необратимое ингибирование. Лекарственные препараты как ингибиторы ферментов.
В клетке постоянно происходит большое количество разнообразных химических реакций, которые формируют метаболические пути - последовательное превращение одних соединений в другие. Метаболизм - совокупность всех метаболических путей, протекающих в клетках организма.
Среди всех метаболических путей, протекающих в организме, выделяют противоположно направленные процессы: катаболизм и анаболизм. Катаболизм - распад сложных веществ до простых с высвобождением энергии. Анаболизм - синтез из простых более сложных веществ. Метаболические пути согласованы между собой по месту, времени и интенсивности протекания.
Регуляция скорости ферментативных реакций осуществляется на 3 независимых уровнях:
изменением количества молекул фермента;
доступностью молекул субстрата и кофер-мента;
изменением каталитической активности молекулы фермента.
Основные способы регуляции активности ферментов:
аллостерическая регуляция;
регуляция с помощью белок-белковых взаимодействий;
активация ферментов в результате присоединения регуляторных белков;
изменение каталитической активности ферментов вследствие ассоциации или диссоциации протомеров фермента.
регуляция путём фосфорилирования/дефосфорилирования молекулы фермента;
регуляция частичным (ограниченным) протеолизом.

15. Энзимодиагностика заболеваний. Изоферменты. Диагностическое значение определения изоферментов (ЛДГ, креатинкиназа). Энзимотерапия. Виды энзимопатий.

Лактатдегидрогеназа (ЛДГ) общая – внутриклеточный гликолитический фермент, который участвует в обратимом превращении лактата в пируват и содержится в большинстве тканей организма. При заболеваниях, сопровождающихся повреждением тканей и разрушением клеток, концентрация ЛДГ в крови повышается. В связи с этим она является важным маркером тканевой деструкции. Несмотря на то что увеличение количества фермента не указывает на какую-то определённую болезнь, его определение в комплексе с другими лабораторными анализами помогает в диагностике инфаркта лёгкого, мышечной дистрофии и гемолитической анемии. Креатинкиназа – фермент, который стимулирует превращение креатинина в креатинфосфат и обеспечивает энергией мышечное сокращение. Креатинкиназа – это фермент, который катализирует реакцию переноса фосфорильного остатка с АТФ на креатинин с образованием креатинфосфата и АДФ. Таким образом, повышение креатинкиназы в крови позволяет сделать вывод об опухолевом процессе, поражении сердца или мышц, которое в свою очередь может развиться как при первичном повреждении данных органов (при ишемии, воспалении, травмах, дистрофических процессах), так и вследствие их поражения при других состояниях (из-за отравления, метаболических нарушений, интоксикаций). Энзимопатии (ферментопатии) в широком смысле слова — патологические изменения активности ферментов.
1. Наследственные энзимопатии, связанные:
а) с полным выпадением синтеза какого-либо фермента;
б) с конституциональной слабостью отдельных звеньев ферментных процессов.
2. Токсическая энзимопатия, обусловленные:
а) избирательным угнетением активности отдельных ферментов;
б) специфическим угнетением биосинтеза ферментов;
в) неспецифическим угнетением биосинтеза белка.
3. Алиментарные энзимопатии, вызванные:
а) дефицитом витаминов;
б) дефицитом белка;
в) дефицитом микроэлементов;
г) разбалансированностью рационов питания.
4. Энзимопатия, вызванная нарушением нейрогуморальной регуляции.
5. Энзимопатии, связанные с нарушением внутриклеточной организации ферментных процессов.
6. Прочие патологические процессы.
Ферменты, катализирующие одну и ту же химическую реакцию, но отличающиеся по первичной структуре белка, называют изофермен-тами, или изоэнзимами. Они катализируют один и тот же тип реакции с принципиально одинаковым механизмом, но отличаются друг от друга кинетическими параметрами, условиями активации, особенностями связи апофермента и кофермента (Изоформы креатинкиназы, лактатдегидрогеназы).
16. Обмен веществ: питание, метаболизм и выделение продуктов метаболизма. Основные пищевые вещества: углеводы, жиры, белки; суточная потребность. Незаменимые компоненты основных пищевых веществ. Незаменимые аминокислоты; пищевая ценность разных белков. Незаменимые жирные кислоты.

17. Витамины. Классификация, функции водо- и жирорастворимых витаминов. Алиментарные и вторичные авитаминозы и гиповитаминозы. Гипервитаминозы.
Витамины - низкомолекулярные органические соединения различной химической природы и различного строения, синтезируемые главным образом растениями, частично - микроорганизмами. Для человека витамины - незаменимые пищевые факторы.

18. Витамин С (аскорбиновая кислота). Структура, суточная потребность, пищевые источники, авитаминоз. Участие в окислительно-восстановительных процессах, стероидогенезе и образовании коллагена. Реакции гидроксилирования пролина и лизина.
Аскорбиновая кислота - лактон кислоты, близкой по структуре к глюкозе. Существует в двух формах: восстановленной (АК) и окисленной (дегидроаскорбиновой кислотой, ДАК).
Обе эти формы аскорбиновой кислоты быстро и обратимо переходят друг в друга и в качестве коферментов участвуют в окислительно-восстановительных реакциях. Аскорбиновая кислота может окисляться кислородом воздуха, пероксидом и другими окислителями. ДАК легко восстанавливается цистеином, глутатионом, сероводородом. В слабощелочной среде происходят разрушение лактонового кольца и потеря биологической активности. При кулинарной обработке пищи в присутствии окислителей часть витамина С разрушается.
Суточная потребность человека в витамине С составляет 50-75 мг.
Биологические функции. Главное свойство аскорбиновой кислоты - способность легко окисляться и восстанавливаться. Вместе с ДАК она образует в клетках окислительно-восстановительную пару с редокс-потенциалом +0,139 В. Благодаря этой способности аскорбиновая кислота участвует во многих реакциях гидроксилирования: остатков Про и Лиз при синтезе коллагена (основного белка соединительной ткани), при гидроксилировании дофамина, синтезе стероидных гормонов в коре надпочечников.
В кишечнике аскорбиновая кислота восстанавливает Fe3+в Fe2+, способствуя его всасыванию, ускоряет освобождение железа из ферритина, способствует превращению фолата в коферментные формы. Аскорбиновую кислоту относят к природным антиоксидантам.
Клинические проявления недостаточности витамина С. Недостаточность аскорбиновой кислоты приводит к заболеванию, называемому цингой (скорбут). Цинга, возникающая у человека при недостаточном содержании в пищевом рационе свежих фруктов и овощей, описана более 300 лет назад, со времени проведения длительных морских плаваний и северных экспедиций. Это заболевание связано с недостатком в пище витамина С. Болеют цингой только человек, приматы и морские свинки. Главные проявления авитаминоза обусловлены в основном нарушением образования коллагена в соединительной ткани. Вследствие этого наблюдают разрыхление дёсен, расшатывание зубов, нарушение целостности капилляров (сопровождающееся подкожными кровоизлияниями). Возникают отёки, боль в суставах, анемия. Анемия при цинге может быть связана с нарушением способности использовать запасы железа, а также с нарушениями метаболизма фолиевой кислоты.
Синтез и созревание коллагена включают в себя целый ряд посттрансляционных изменений:
· гидроксилирование пролина и лизина с образованием гидроксипролина и гидроксилизина;
· гликозилирование гидроксилизина;
· частичный протеолиз - отщепление "сигнального" пептида, а также N- и С-конце-вых пропептидов;
· образование тройной спирали.
Гидроксилазы пролина и лизина содержат в активном центре атом железа Fe2+. Для сохранения атома железа в ферроформе необходим восстанавливающий агент. Роль этого агента выполняет кофермент гидроксилаз - аскорбиновая кислота, которая легко окисляется в дегидроаскорбиновую кислоту. Обратное превращение происходит в ферментативном процессе за счёт восстановленного глутатиона.
| <== предыдущая | | | следующая ==> |
| Выбор подвижного состава | | |
Date: 2016-02-19; view: 908; Нарушение авторских прав