
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Задача № 3. Вычислить теплоту образования оксида кальция по его реакции взаимодействия с водой, если количество теплоты
|
|
Вычислить теплоту образования оксида кальция по его реакции взаимодействия с водой, если количество теплоты, которое выделяется вследствие реакции, составляет 32,53кДж, а ∆Н0обр..[Са(ОН)2]= ‑ 986,2кДж/моль; ∆Н0обр..(Н2О) = ‑285,84кДж/моль
 Дано:
Дано:
Q = 32,53кДж
∆Н0обр..[Са(ОН)2] = ‑ 986,2кДж/моль
∆Н0обр..(Н2О) = ‑ 285,84кДж/моль
 Вычислить: ∆Н0обр..(СаО) ‑?
Вычислить: ∆Н0обр..(СаО) ‑?
Решение:
Запишем уравнение взаимодействия оксида кальция с водой:
СаО (тв.) + Н2О (ж.) → Са(ОН)2 (тв.)
Молярная масса вещества эквивалента fэкв(Х)Х – это масса одного моль вещества эквивалента fэкв(Х)Х, равна произведению фактора эквивалентности fэкв(Х) и молярной массы вещества Х.
Форма записи молярной массы вещества эквивалента fэкв(Х)Х: М(fэкв(Х)Х) и вычисляется по формуле:
М(fэкв (Х)Х) = fэкв (Х) ∙ М(Х);
Мэкв[Ca(OH)2] = 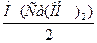 =
= 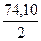 = 37,05г/моль, где fэкв(Ca(OH)2) = ½;
= 37,05г/моль, где fэкв(Ca(OH)2) = ½;
Вычислим количество вещества Ca(OH)2, соответствующее 37,05г:
n[Ca(OH)2] = m / Мэкв.[Ca(OH)2] = 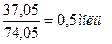
Зная, что количество выделяющейся (поглощающейся) теплоты при химических реакциях, прямо пропорционально количеству вещества, принимающего участие в реакции:
Q = n ∙ ∆Н0
Вычислим тепловой эффект реакции образования гидроксида кальция:
∆Н0 = 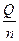
Учитывая то, что реакция экзотермическая (сопровождается выделением теплоты):
Q = ‑ ∆Н0, ∆Н0 = ‑ 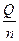 , то есть ∆Н0 = ‑
, то есть ∆Н0 = ‑  = ‑ 65,06кДж
= ‑ 65,06кДж
Запишем следствие из закона Гесса для данной реакции:
∆Н0 = ∆Н0обр..[Са(ОН)2] ‑ ∙∆Н0обр..(СаО) – ∆Н0обр.(Н2О)
Находим,
∆Н0обр..(СаО) = ∆Н0обр..[Са(ОН)2] – ∆Н0обр.(Н2О) – ∆Н0
После подстановки соответствующих численных значений величин и расчётов, получим:
∆Н0обр..(СаО)= ‑ 986,2 + 285,84 + 65,06 = ‑ 635,3кДж/моль
Ответ: ∆Н0обр..(СаО)= ‑ 635,3кДж/моль
Date: 2016-01-20; view: 980; Нарушение авторских прав