
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Металлы
|
|
Благородные - Ag, Au, Pt, Ru, Rh, Os, Ir
Лёгкие (ρ < 5 г/см3) - Li, Na, K, Rb, Cs, Be, Mg, Ca, Al, Ti
Легкоплавкие (tпл. < 1000°C) - Li, Na, K, Cs, Rb, Ca, Mg и др.
Радиоактивные - Fr, Ra, U, Тс, актиноиды
Рассеянные - Ga, In, Tl, Ge, Hf, Re
Редкоземельные — Sc, Y, La, лантаноиды
Тугоплавкие (tпл. > 1000°C) - Ti, Ir, Hf, W, Nb, Та, Cr, Mo, V, Re
Тяжёлые (p > 5 г/см3) - Mn, Fe, Co, Ni, Cu, Zn, Cd, Hg, Sn, Pb и др.
Цветные - Ag, Au, Cu, Mn, Co, Ni, Cr и др.
Чёрные - Fe и его сплавы
Продолжение
Взаимодействие серной и азотной кислот с некоторыми металлами
| Кислота (окислитель) | ||||
| Металл | H2SO4 | HNO3 | ||
| разб. | конц. | разб. | конц. | |
| К, Ва, Са, | соль | соль | соль | |
| Na, Mg | соль + H2 | + H2S | + NH3 (NH4NO3) | + N2O |
| + Н2О | + Н2O | + Н2О | ||
| пассивация (на | ||||
| Al, Cr, Fe | СОЛЬ + H2 | холоде); | соль | пассивация |
| при нагревании с | + NO | |||
| А1 (соль | + Н2О | |||
| + H2S | ||||
| + Н2О), | ||||
| с Cr, Fe (соль | ||||
| + SO2 | ||||
| + Н2O) | ||||
| соль | соль | соль | ||
| Zn, Sn | СОЛЬ + H2 | + SO2 | + NO | + NO2 |
| + Н2О | + Н2О | + Н2О | ||
| Ni, Pb, | соль | соль | соль | |
| Cu, Hg, Ag | - | + SO2 | + NO | + NO2 |
| + Н2О | + Н2О | + H2O |
10.
Растворимость кислот, солей и оснований в воде
| Ионы | н+ | NH4+ | Na+ | К+ | Ва2+ | Са2+ | Mg2+ | А13+ | Сr3+ | Fe2+ | Fe3+ | Мn2+ | Zn2+ | Сu2+ | Ag+ | Рb2+ |
| ОН | 18,0 | 35,0 | Р 40,0 | Р 56,1 | Р 171,4 | М 74,1 | Н 58,3 | Н 78,0 | Н 103,0 | Н 89,9 | Н 106,0 | Н 88,9 | Н 99,4 | Н 97,6 | 124,9 | Н 241,2 |
| Сl- | Р 36,5 | Р 53,5 | Р 58,4 | Р 74,6 | Р 208,2 | Р 111,0 | Р 95,2 | Р 133,3 | Р 158,4 | Р 126,8 | Р 162,2 | Р 125,8 | Р 136,3 | Р 134,4 | Н 143,3 | М 278,1 |
| Вr- | Р 80,9 | Р 97,9 | Р 102,9 | Р 119,0 | Р 297,2 | Р 199,9 | Р 184,1 | Р 266,7 | Р 271,7 | Р 215,7 | Р 295,6 | Р 214,8 | Р 225,2 | 223,4 | Н 187,8 | М 367,0 |
| I- | Р 127,9 | Р 144,9 | Р 149,9 | Р 166,0 | Р 391,1 | Р 293,9 | Р 276,1 | Р 407,7 | Р 432,7 | Р 310,1 | Р 436,9 | Р 308,8 | Р 319,2 | 317,4 | Н 234,8 | М 461,0 |
| NO3- | Р 63,0 | Р 80,0 | Р 85,0 | Р 101,1 | Р 261,4 | Р 164,1 | Р 148,3 | Р 213,0 | Р 239,0 | Р 179,9 | Р 241,9 | Р 179,0 | Р 189,4 | Р 187,4 | Р 169,9 | Р 331,2 |
| S2- | Р 34,1 | Р 68,1 | Р 78,0 | Р 110,3 | Р 169,4 | 72,1 | 56,1 | Н 150,2 | Н 200,2 | Н 87,9 | Н 207,9 | Н 87,0 | Н 97,4 | Н 95,6 | Н 247,8 | Н 239,2 |
| SO32- | Р 82,1 | Р 116,1 | Р 126,0 | Р 158,3 | М 217,4 | М 120,1 | М 104,4 | 294,1 | 344,2 | М 135,9 | 351,9 | 135,0 | М 145,4 | 143,6 | М 259,8 | Н 287,2 |
| SO42- | Р 98,1 | Р 132,3 | Р 142,0 | Р 174,3 | Н 233,4 | М 136,1 | Р 12,4 | Р 342,2 | Р 392,2 | Р 151,9 | Р 399,9 | Р 151,0 | Р 161,4 | Р 159,6 | М 311,8 | Н 303,2 |
| СO32- | Р 62,0 | Р 96,1 | Р 105,9 | Р 138,2 | Н 197,4 | Н 100,1 | Н 84,3 | 234,0 | 284,0 | Н 115,9 | 291,7 | М 115,0 | Н 125,3 | Н 123,6 | Н 275,8 | Н 267,2 |
| SiO32- | Н 78,1 | 112,2 | Р 122,1 | Р 154,3 | Н 213,4 | М 116,2 | 100,4 | 282,2 | 332,2 | Н 131,9 | 339,9 | 131,0 | Н 141,4 | 139,6 | Н 291,8 | Н 283,3 |
| РО43- | Р 98,0 | Р 149,1 | Р 163,9 | Р 212,3 | Н 602,0 | Н 310,2 | Н 262,8 | Н 122,0 | 147,0 | Н 357,5 | Н 150,8 | 354,8 | Н 386,1 | Н 380,6 | Н 418,6 | Н 811,5 |
Растворимость соединения (Р) - Растворимое (больше 10 г на 100 г воды); (М) - Малорастворимое (меньше 10 г до 0,01 г на 100 г воды);
Молекулярная масса соединения (Н) - Нерастворимое (меньше 0,01 г на 100 г воды); (-)- Вещество разлагается водой или не существует
СОДЕРЖАНИЕ
I. Моль. Эквивалентные массы и эквиваленты простых и сложных
веществ. Закон эквивалентов................................................................... 3
П. Стехиометрические законы химии...................................................... 5
III. Строение атома. Химическая связь. Периодический закон и
периодическая система химических элементов Д.И. Менделеева.......... 7
IV. Тепловые эффекты химических реакций. Термохимические
уравнения и расчёты............................................................................ 12
V. Химическая кинетика и химическое равновесие............................. 15
VI. Растворы. Способы выражения концентрации................................... 19
Свойства растворов............................................................................... 23
VII. Электролитическая диссоциация. Степень электролитической
диссоциации. Ионное произведение воды. Произведение
растворимости..................................................................................... 26
VIII. Ионные уравнения реакций............................................................. 29
IX. Гидролиз......................................................................................... 32
X. Окислительно-восстановительные реакции (ОВР)............................. 35
XI. Электрохимические процессы. Электролиз. Коррозия металлов.... 41
XII. Неметаллы...................................................................................... 46
Углерод. Кремний................................................................................ 46
Азот. Фосфор............................................................................................ 48
Кислород. Сера..................................................................................... 49
Галогены................................................................................................... 50
XIII. Металлы......................................................................................... 51
Металлы главных подгрупп................................................................. 51
Металлы побочных подгрупп............................................................... 53
XIV. Осуществите следующие превращения........................................ 55
XV. Органические соединения.............................................................. 56
Формулы для расчётов в химии.............................................................. 60
Варианты контрольных заданий............................................................. 62
Список рекомендуемой литературы....................................................... 68
Приложение
1. Относительные электроотрицательности элементов....................... 69
2. Основные физические постоянные....................................................... 69
3. Стандартные энтальпии образования ΔН°298, энтропии S°298 и
энергии Гиббса образования ΔG°298 некоторых веществ при 298 К
(25°С)........................................................................................................ 70
4. Групповые названия химических элементов....................................... 70
5. Названия некоторых кислот и их солей.............................................. 71
6. Названия некоторых средних, кислых и основных солей............... 72
7. Электрохимический ряд напряжений металлов.................................. 73
8. Металлы................................................................................................ 73
9. Взаимодействие серной и азотной кислот с некоторыми
металлами............................................................................................... 74
10. Растворимость кислот, солей и оснований в воде.......................... 75
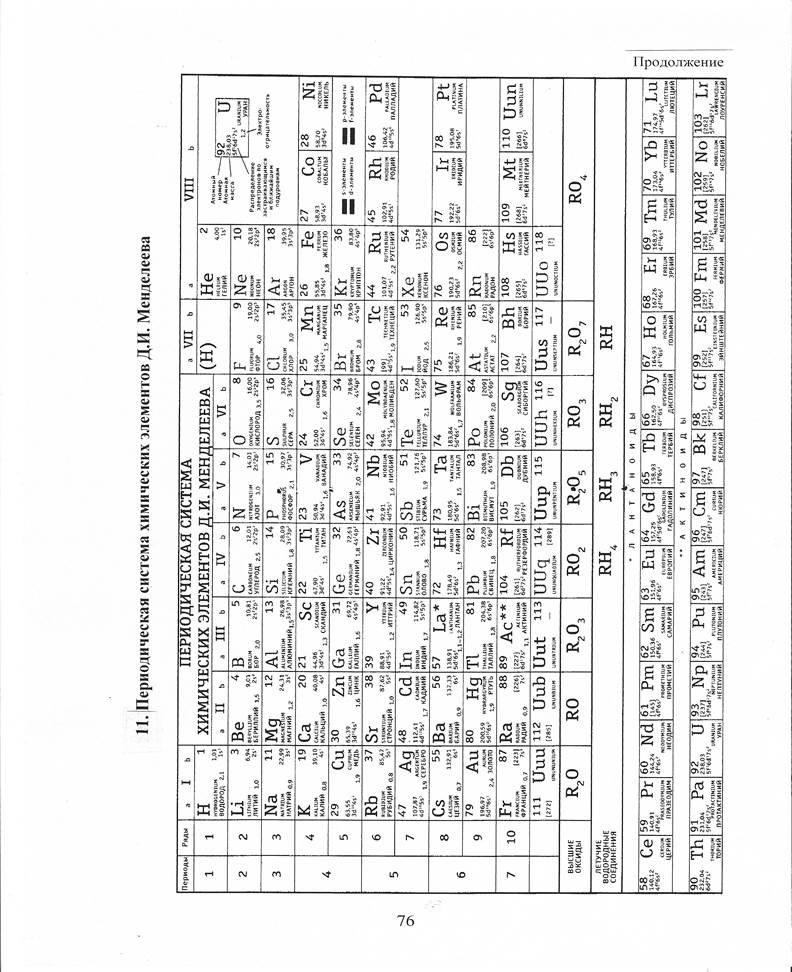
11. Периодическая система химических элементов Д.И. Менделеева.... 76
Учебное издание
Кудаярова Рушания Равильевна Мазитова Алия Карамовна Михайлюк Юрий Иванович
Date: 2016-02-19; view: 645; Нарушение авторских прав