
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

I. Iб. Ферментативное окисление
|
|
Некоторые ЖК с длинной цепью окисляются специфическими ферментами, при этом образуется целый ряд разных биологически активных и очень важных соединений.
Из арахидоновой кислоты образуются простагландины, тромбоксаны и лейкотриены (о которых было сказано выше). Суммарный процесс отражают следующие реакции:
Инициация: RH + 'OH --- H2O + R'
R' + O2 --- ROO'
Развитие: ROO' + RH --- ROOH + R'
Завершение: R' + R' ---R - R, где LH, L', LOO' and LOOH - соответственно полиненасыщенный липид, липидный алкильный радикал, липидный пероксирадикал и липоперекись.Любой радикал, способный вырвать атом водорода, может запустить реакцию ПОЛ. В этом смысле гидроксирадикал, липидный пероксирадикал LOO', алкоксильный радикал LO' - все обладают достаточной энергией для инициации ПОЛ, тогда как 'O2- и Н2О2 - нет. В то же время при взаимодействии 'O2 с H2O2 образуется 'OH, который запускает ПОЛ. В принципе, гидроксирадикал может реагировать с любым органическим субстратом. Он включается в ароматические аминокислоты с образованием гидроксилированных форм, окисляет SH- группы аминокислот, что ведет к нарушению структуры белка и прямой инактивации ферментов с SH- группами в активных центрах. Этот радикал реагирует также с сахарными остатками ДНК, ведя к образованию продуктов деградации с конечным расщеплением ДНК. С этим, в частности, связаны эффекты многих цитостатиков.
Для защиты от потенциально патогенных АКР в клетках имеется антиоксидантная система защиты. В нее прежде всего входят ферменты- чистильщики, такие как супероксиддисмутаза (СОД), каталаза и глютатионпероксидаза.
СОД существует в двух формах: цитоплазменной и митохондриальной. Первая содержит медь и цинк, вторая - марганец. Под действием СОД происходит дисмутация 'O2 с образованием Н2О2 и О2. СОД относится к внутриклеточным ферментам. В биологических жидкостях его либо вообще нет, либо он содержится в виде следов. Поэтому 'O2 , попав во внеклеточную среду, По-существу встречает слабое противодействие со стороны СОД.
Гемопротеин каталаза действует в комплексе с СОД. Этот фермент разрушает Н2О2, превращая ее в воду и кислород. Каталаза присутствует в пероксисомах многих клеток. Фермент специфичен в отношении Н2О2 и не действует на органические гидропероксиды.
Глютатионпероксидаза разрушает как перекись водорода, так и органические пероксиды. Этот фермент содержит селений в активном центре и ускоряет распад пероксидов за счет восстановленного глютатиона в реакции:
2GSH + LOOH --- GSSG + LOH + H20
Глютатионпероксидаза имеется в большинстве клеток и содержится как в цитозоле так и митохондриях. Указанные ферменты составляют первую линию защиты клеток от окислительного повреждения. Они нейтрализуют 'O2- и H2O2 еще до того как те дают начало 'OH. Помимо первой имеется и вторая линия защиты, представленная неферментными чистильщиками, такими как альфа-токоферол, каротиноиды (бета-каротен), витамин А, аскорбат, сульгидрильные соединения и тиоэфиры.
Окисление жирных кислот в клетках. ВЖК могут окисляться в клетках тремя путями:
а) путем α-окисления,
б) путем β-окисления,
в) путем ω-окисления.
Процессы α- и ω-окисления ВЖК идут в микросомах клеток с участием ферментов монооксигеназ и играют в основном пластическую функцию. В ходе этих процессов идет синтез гидроксикислот, кетокислот и кислот с нечетным числом атомов углерода, необходимых для клеток.
2.1.1в. β-Окисление высших жирных кислот
Периферические ткани постоянно принимают ВЖК из крови. Последние легко проникают через клеточную мембрану, поэтому их поглощение находится в прямой зависимости от концентрации ВЖК в крови. Проникнув через клеточную мембрану, ВЖК изначально подвергаются «активации» - превращаясь в ацил-КоА-производные. Только в форме ацил-КоА ВЖК способны окисляться в митохондриях. Реакция создания ацил-КоА протекает на внешней мембране митохондрий, ее цель создание макроэргического реакционно-способного соединения, – а именно тиоэфира жирной кислоты (только в форме тиоэфира ЖК способны вступать в реакции иначе они
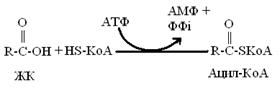 |
просто метаболически инертны). Реакцию катализируют ферменты ацил-КоА-синтетазы – группа ферментов для коротких, средних и длинных цепей жирных кислот.
Далее ацил-КоА переносится в митохондиальный матрикс для дальнейшего окисления с помощью специальной транспортной системы использующей карнитин. Фермент карнитин-ацилтрансфераза I образует ацилкарнитин, он переносится транслоказой в матрикс где работает другой фермент – карнитин-ацилтрансфераза II в обратном направлении и снова образуется тиоэфирная форма ВЖК – ацил-КоА. Реакция идет без затрат энергии так как ацилкарнитин является сам макроэргическим соединением по энергии сопоставимым с тиоэфиром.
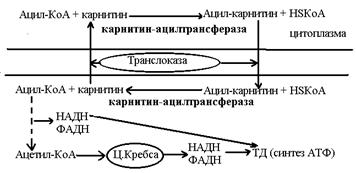 |
Доставленная в митохондрию жирная кислота окисляется путем последовательного отщепления двух углеводородных атомов представляющих ацетильную группу (Ацетил-КоА) и осуществляющийся следующим образом:
1.дегидрогенизация с помощью ФАД-зависимого фермента – Ацетил-КоА-дегидрогеназа; 2.гидротация с помощью Еноил-КоА-гидротаза;
3.НАД-зависимая дегидрогенизация – гидроксиацил-КоА-дегидрогеназа;
4.разрыв углеводородной цепи КоА-SН – кетоацил-КоА-тиолаза.
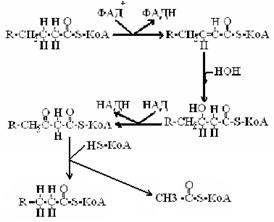
Далее процесс повторяется.
Таким образом, укорочение жирной кислоты идет последовательным удалением из нее двух углеродного фрагмента. Этот фрагмент составляет ацетильную группу Ацетил-КоА.
Последняя реакция взаимодействия КоА-SН с b-кетоацил-КоА, в ходе которой разрывается углеводородная цепь остатка жирной кислоты тиольной группой КоА-SН играет ключевую роль в процессе. Поэтому весь процесс называют b-окислением жирных кислот.
Природные длинноцепочечные жирные кислоты содержат четное число атомов углерода, и последовательное отщепление двухуглеродных фрагментов приводит в итоге к ацетоацетил-КоА. Который, также расщепляется на два ацетил-КоА.
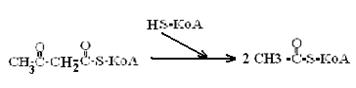
В случае окисления жирной кислоты с нечетным числом углеродных атомов, например, жирные кислоты растительного происхождения, образуется пропионил-КоА - трех углеродный фрагмент. Он превращается в сукцинил-КоА и вовлекается в цикл Кребса.
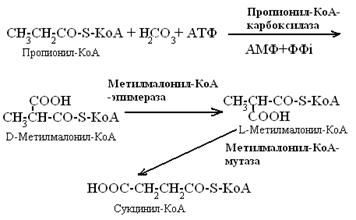
Реакцию изомеризации метилмалонил-КоА катализирует метил-малонил-КоА-мутаза, кофермент этого фермента – витамин В12 (активная форма – дезоксикаденозилкобаламин).
В случае окисления жирной ненасыщенной кислоты (они поступают с растительной пищей) и имеют одну или несколько двойных связей, процесс идет аналогичным образом вплоть до самой двойной связи. А далее либо она сдвигается в нужное положение особым ферментом либо восстанавливается.
Энергетическая ценность ЖК (формула): 5 АТФ х (n/2-1) + 12АТФ х (n/2) – 1АТФ = ВСЕГО АТФ,
число атомов углерода в ЖК, (n/2-1) – число циклов β-окисления, (n/2) – число образовавшихся молекул ацетил-КоА,1АТФ – затрачивается на активацию ЖК
Пальмитиновая кислота состоящая из 16 углеродных атомов (С16) в процессе окисления распадается на 8 молекул ацетил-КоА при этом образуется 7 НАДН и 7 ФАДН. Ацетил-КоА поступая в цикл Кребса создает еще 24 НАДН, 8 ФАДН и 8 ГТФ (один оборот цикла это 3 НАДН, 1 ФАДН и 1 ГТФ таких оборотов будет 8). Суммируя весь НАДН, получим -- 31, суммируем ФАДН – 15. И НАДН и ФАДН в тканевом дыхании будут давать 93 и 30 молекул АТФ (т.к. 1 НАДН – 3 АТФ, 1 ФАДН – 2 АТФ). В итоге 93 + 30 + 8 = 131 АТФ. Одна АТФ тратится на активацию жирной кислоты. Общий выход АТФ при окислении одной молекулы пальмитиновой кислоты составляет: 131-1=130 молекул АТФ.
Date: 2015-05-22; view: 1779; Нарушение авторских прав