
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Генетический дефект дегидрогеназы жирных кислот со средней длиной углеводородной цепи
|
|
В митохондриях имеется 3 вида ацил-КоА-дегидрогеназ, окисляющих жирные кислоты с длинной, средней или короткой цепью радикала. Жирные кислоты по мере укорочения радикала в процессе β-окисления могут последовательно окисляться этими ферментами. Генетический дефект дегидрогеназы жирных кислот со средней длиной радикала наиболее распространён по сравнению с другими наследственными заболеваниями. Активность этой дегидрогеназы особенно важна для грудных детей, у которых жиры молока служат основным источником энергии, а в триацилглицеролах молока преобладают жирные кислоты со средней длиной цепи. Невозможность использовать жирные кислоты как источники энергии приводит к увеличению скорости окисления глюкозы. В результате у детей развивается гипогликемия - причина внезапной детской смертности (10% от общего числа умерших новорождённых). Если такие дети выживают, то после голодания в течение 6-8 ч у них развиваются гипогликемические приступы (слабость, головокружение, рвота, потеря сознания). Введение глюкозы приводит к исчезновению симптомов.
Во всех случаях, когда нарушается β-окисление, жирные кислоты накапливаются в клетках и распадаются по пути ω-окисления, которое в норме идёт с очень низкой скоростью. Окисление происходит по метильному ω-атому углерода и в результате образуются дикарбоновые кислоты, выделяющиеся с мочой. Определение этих кислот в моче может служить диагностическим признаком нарушения β-окисления.
Нарушение окисления фитановой кислоты. При редком наследственном заболевании - болезни Рефсума, развивающейся вследствие генетического дефекта одного из ферментов, участвующих в α-окислении, фитановая кислота, поступающая с пищей, не окисляется и накапливается в организме, в основном в нервной ткани. Это приводит к нарушению структуры нервной ткани и развитию многих неврологических симптомов.
Вопрос 30. Биосинтез пальмитиновой жирной кислоты, химизм, жирнокислотная синтетаза.
1)Образование ацетил-КоА и его транспорт в цитозоль
Синтез жирных кислот происходит в абсорбтивный период. Активный гликолиз и последующее окислительное декарбоксилирование пирувата способствуют увеличению концентрации ацетил-КоА в матриксе митохондрий. Так как синтез жирных кислот происходит в цитозоле клеток, то ацетил-КоА должен быть транспортирован через внутреннюю мембрану митохондрий в цитозоль. Однако внутренняя мембрана митохондрий непроницаема для ацетил-КоА, поэтому в матриксе митохондрий ацетил-КоА конденсируется с оксалоацетатом с образованием цитрата при участии цитратсинтазы:
Ацетил-КоА + Оксалоацетат -> Цитрат + HS-КоА.
Затем транслоказа переносит цитрат в цитоплазму.
Перенос цитрата в цитоплазму происходит только при увеличении количества цитрата в митохондриях, когда изоцитратдегидрогеназа и α-кетоглутаратдегидрогеназа ингибированы высокими концентрациями NADH и АТФ. Эта ситуация создаётся в абсорбтивном периоде, когда клетка печени получает достаточное количество источников энергии. В цитоплазме цитрат расщепляется под действием фермента цитратлиазы:
Цитрат + HSKoA + АТФ → Ацетил-КоА + АДФ + Pi + Оксалоацетат.
Ацетил-КоА в цитоплазме служит исходным субстратом для синтеза жирных кислот, а окса-лоацетат в цитозоле подвергается следующим превращениям (см. схему ниже).
Пируват транспортируется обратно в матрикс митохондрий. Восстановленный в результате действия малик-фермента NADPH используется как донор водорода для последующих реакций синтеза жирных кислот. Другой источник NADPH - окислительные стадии пентозофосфатного пути катаболизма глюкозы..
Образование малонил-КоА из ацетил-КоА - регуляторная реакция в биосинтезе жирных кислот.
2)Первая реакция синтеза жирных кислот - превращение ацетил-КоА в малонил-КоА. Фермент, катализирующий эту реакцию (ацетил-КоА-карбоксилаза), относят к классу лигаз. Он содержит ковалентно связанный биотин (рис. 8-36). В первой стадии реакции СО2 ковалентно связывается с биотином за счёт энергии АТФ, во второй стадии СОО- переносится на ацетил-КоА с образованием малонил-КоА. Активность фермента ацетил-КоА-карбоксилазы определяет скорость всех последующих реакций синтеза жирных кислот.
Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-КоА, в результате чего образуется малонил-КоА:
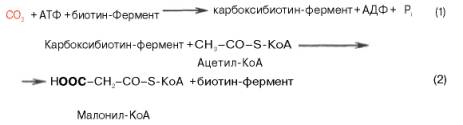
Реакции, катализируемые синтазой жирных кислот, - ферментным комплексом, катализирующим реакции синтеза пальмитиновой кислоты, описывается ниже.
 После образования малонил-КоА синтез жирных кислот продолжается на мультиферментном комплексе - синтазе жирных кислот (пальмитоилсинтетазе). Этот фермент состоит из 2 идентичных протомеров, каждый из которых имеет доменное строение и, соответственно, 7 центров, обладающих разными каталитическими активностями (рис. 8-37). Этот комплекс последовательно удлиняет радикал жирной кислоты на 2 углеродных атома, донором которых служит ма-лонил-КоА. Конечный продукт работы этого комплекса - пальмитиновая кислота, поэтому прежнее название этого фермента - пальмитоилсинтетаза.
После образования малонил-КоА синтез жирных кислот продолжается на мультиферментном комплексе - синтазе жирных кислот (пальмитоилсинтетазе). Этот фермент состоит из 2 идентичных протомеров, каждый из которых имеет доменное строение и, соответственно, 7 центров, обладающих разными каталитическими активностями (рис. 8-37). Этот комплекс последовательно удлиняет радикал жирной кислоты на 2 углеродных атома, донором которых служит ма-лонил-КоА. Конечный продукт работы этого комплекса - пальмитиновая кислота, поэтому прежнее название этого фермента - пальмитоилсинтетаза.
Биосинтез по порядку:

Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО2.
Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:
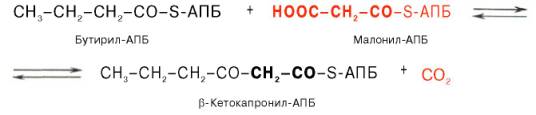
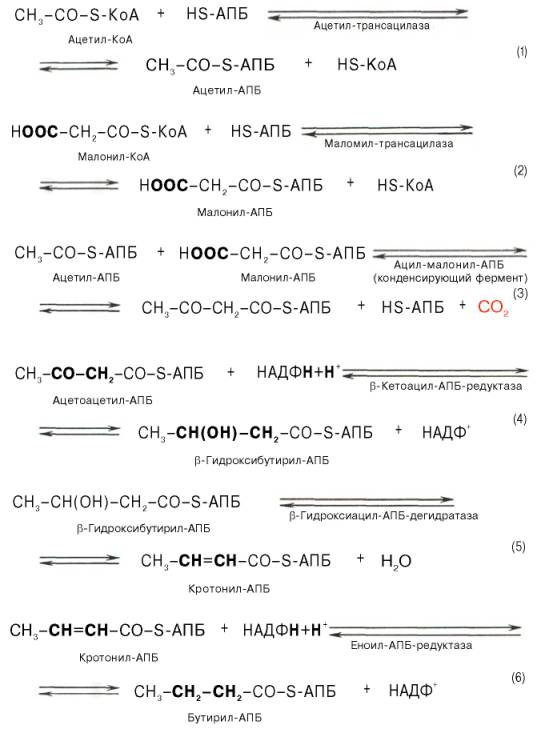
Вопрос 31.Биосентез жирных кислот с длинной цепью углеводных атомов(С18 и больше С-атомов) Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме пече-ночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из уже синтезированной в цитоплазме клетки пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома. Первой реакцией биосинтеза жирных кислот является карбоксилирование ацетил-КоА, для чего требуются бикарбонат, АТФ, ионы марганца. Катализирует эту реакцию фермент ацетил-КоА-кар-боксилаза. Фермент содержит в качестве простетической группы биотин. Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-КоА, в результате чего образуется малонил-КоА. Малонил-КоА представляет собой первый специфический продукт биосинтеза жирных кислот. В присутствии соответствующей ферментной системы малонил-КоА быстро превращается в жирные кислоты. Последовательность реакций, происходящих при синтезе жирных кислот:
Вопрос 32. Биосинтез ненасыщенных кислот. Полиненасыщенные жирные кислоты. 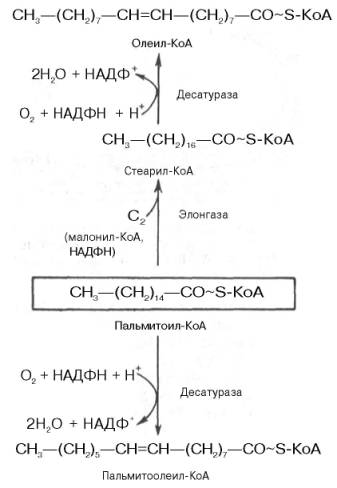
В отличие от растительных тканей ткани животных обладают весьма ограниченной способностью превращать насыщенные жирные кислоты в ненасыщенные. Установлено, что две наиболее распространенные мононенасыщенные жирные кислоты – пальмитоолеиновая и олеиновая – синтезируются из пальмитиновой и стеариновой кислот. Эти превращения протекают в микросомах клеток печени и жировой ткани при участии молекулярного кислорода, восстановленной системы пиридиновых нуклеотидов и цитохрома b5. Превращению подвергаются только активированные формы пальмитиновой и стеариновой кислот. Ферменты, участвующие в этих превращениях, получили название деса-тураз. Наряду с десатурацией жирных кислот (образование двойных связей) в микросомах происходит и их удлинение (элонгация), причем оба эти процесса могут сочетаться и повторяться. Удлинение цепи жирной кислоты происходит путем последовательного присоединения к соответствующему ацил-КоА двууглеродных фрагментов при участии малонил-КоА и НАДФН. Энзиматическая система, катализирующая удлинение жирных кислот, получила название элонгазы. На схеме представлены пути превращения пальмитиновой кислоты в реакциях десатурации и элонгации.
Полиненасыщенные жирные кислоты:омега-3 и омега-6.
Омега-3 полиненасыщенные жирные кислоты (ПНЖК) относятся к семейству ненасыщенных жирных кислот, имеющих двойную углерод-углеродную связь в омега-3 позиции, то есть после третьего атома углерода, считая от метилового конца цепи жирной кислоты.Наиболее важными омега-3 полиненасыщенными жирными кислотами являются альфа-линоленовая кислота (АЛК), эйкозапентаеновая кислота (ЭПК) и докозагексаеновая кислота (ДГК). Организм человека не способен синтезировать эти жирные кислоты из более простых веществ, хотя он может образовывать длинноцепочечные ЭПК и ДГК из более короткоцепочечной АЛК с эффективностью около 5 % у мужчин [1][2] и немного более высокой эффективностью у женщин [3]. Эти реакции, однако, замедляются в присутствии омега-6 жирных кислот. Таким образом, накопление длинноцепочечных ЭПК и ДГК в тканях является наиболее эффективным, когда они поступают непосредственно из пищи, или когда конкурирующие количества омега-6 аналогов являются низкими.
Вопрос 33. Биосинтез и использование ацетоуксусной кислоты, физиологическое значение процессов. К кетоновым телам относят три вещества: β-гидроксибутират, ацетоацетат и ацетон.
Только первые два являются источниками энергии и могут окисляться в тканях. В норме концентрация кетоновых тел в крови невелика и составляет 1-3 мг/дл. Синтез кетоновых тел увеличивается при:
• голодании;
• длительной интенсивной физической нагрузке;
• употреблении пищи, богатой жирами, но с низким содержанием углеводов (диета Аткинса, «кремлевская» диета);
• сахарном диабете.
Кетоновые тела являются водорастворимыми кислотами, поэтому в отличие от жирных кислот, они могут проходить через гематоэнцефалический барьер и служат, наряду с глюкозой, источником энергии для нервной ткани, особенно после 3-5 дней голодания, когда концентрация кетоновых тел в крови существенно увеличивается.Скелетные мышцы и почки используют кетоновые тела даже при их низкой концентрации в крови.
Синтез кетоновых тел происходит в митохондриях печени и в небольшом количестве - в корковом слое почек. Исходным субстратом синтеза служит ацетил-КоА, образующийся в результате β-окисления жирных кислот. Ситуация, в которой увеличивается синтез кетоновых тел, развивается следующим образом. При голодании гормон глюкагон (или адреналин при физической работе) через аденилатциклазную систему в жировой ткани активирует распад жира. Жирные кислоты выделяются в кровь и транспортируются в комплексе с альбуминами в печень. В печени увеличивается скорость β-окисления и образуется большое количество ацетил-КоА. Скорость реакций цикла Кребса в этих условиях снижена в результате ингибирования регуляторных ферментов цитратного цикла аллостерическими ингибиторами АТФ и NADH, концентрация которых повышена в результате активного β-окисления. Кроме того, при высокой концентрации NADH оксалоацетат восстанавливается до малата и в такой форме переносится в цитозоль, где реакция идет в обратном направлении. Оксалоацетат становится субстратом для глюконеогенеза и менее доступен для взаимодействия с ацетил-КоА. В результате в митохондриях накапливается ацетил-КоА, который используется для синтеза кетоновых тел.При голодании в результате преобладания действия глюкагона активируются липолиз в жировой ткани и β-окисление в печени. Количество оксалоацетата в митохондриях уменьшается, так как его образуется меньше, и, кроме того, он выходит в цитозоль (восстанавливаясь до малата), где используется в глюконеогенезе. В результате скорость использования ацетил-КоА в ЦТК снижается и он используется для синтеза кетоновых тел. Синтез кетоновых тел значительно увеличивается при сахарном диабете.Основным кетоновым телом в крови является β-гидроксибутират, так как равновесие в реакции Ацетоацетат β-Гидроксибутират сдвинуто вправо из-за присутствия высоких концентраций NАDН, который восстанавливается в реакциях β-окисления, протекающих, как и синтез кетоновых тел, в матриксе митохондрий. Повышение концентрации кетоновых тел в крови называют кетонемией. Регуляция синтеза кетоновых тел осуществляется через фермент ГМГ-КоА-синтазу. Этот фермент ингибируется при высоких концентрациях свободного кофермента HS-КоА. Таким образом скорость синтеза кетоновых тел координируется с количеством жирных кислот, поступающих в печень. В ситуациях голодания, сахарного диабета, тяжелой физической работы под действием гормонов глюкагона и адреналина происходит мобилизация ТАГ из жировой ткани, поток жирных кислот в печень увеличивается и HS-КоА связывается с жирными кислотами в ацилКоА. Концентрация свободного HS-КоА снижается и синтез кетоновых тел увеличивается. Окисление кетоновых тел как источников энергии происходит во многих тканях.В печени отсутствует фермент, необходимый для активации кетоновых тел - сукцинил-КоА-ацетоацетаттрансфераза. Поэтому печень не окисляет кетоновые тела и продуцирует их только на «экспорт». Эритроциты, в которых отсутствуют митохондрии, также не используют кетоновые тела.
При длительном голодании и особенно при сахарном диабете в крови существенно возрастает концентрация кетоновых тел и организм не успевает их утилизировать. При накоплении кетоновых тел развивается кетоацидоз, так как ацетоацетат и β-гидроксибутират - это легко диссоцирующие кислоты.
Кетоацидоз является опасным осложнением сахарного диабета. При высоких концентрациях кетоновых тел в крови ацетоацетат неферментативно декарбоксилируется, превращаясь в третье кетоновое тело - ацетон. Ацетон не утилизируется как источник энергии и выводится из организма.
Выведение кетоновых тел, в том числе и ацетона, с мочой (кетонурия), потом выдыхаемым воздухом является способом выведения избытка кетоновых тел из организма и уменьшения таким образом ацидоза.
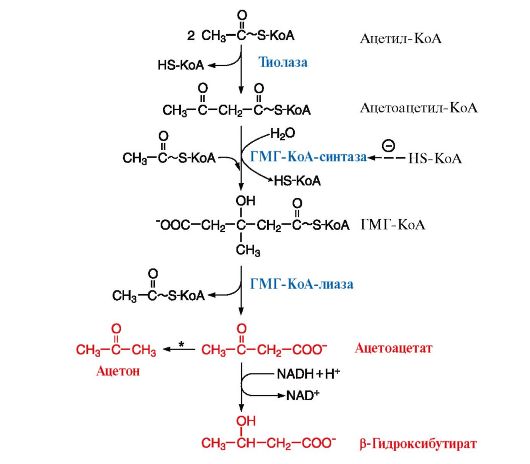
Синтез кетоновых тел:
Окисление кетоновых тел:
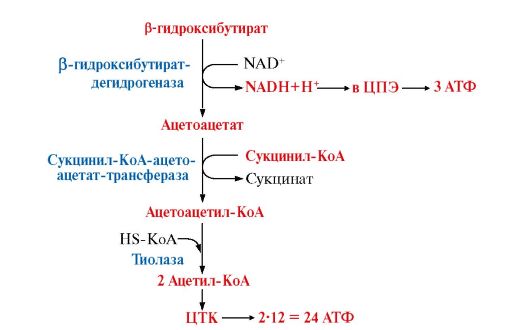 При окислении кетоновые тела активируются путем превращения ацетоацетата в ацетоацетил-КоА. Донором КоА является сукцинил-КоА. В результате окисления β-гидроксибутирата образуется 2 ацетил~КоА, которые далее окисляются в ЦТК. Таким образом при окислении β-гидроксибутирата образуется 27 молекул АТФ, но для активации ацетоацетата используется энергия одной макроэргической связи сукцинил-КоА, поэтому теоретический выход АТФ составляет 26 молекул АТФ
При окислении кетоновые тела активируются путем превращения ацетоацетата в ацетоацетил-КоА. Донором КоА является сукцинил-КоА. В результате окисления β-гидроксибутирата образуется 2 ацетил~КоА, которые далее окисляются в ЦТК. Таким образом при окислении β-гидроксибутирата образуется 27 молекул АТФ, но для активации ацетоацетата используется энергия одной макроэргической связи сукцинил-КоА, поэтому теоретический выход АТФ составляет 26 молекул АТФ
Вопрос 34. Обмен стероидов.Холестерин как предшественник других стероидов.Биосинтез холестерина.
Date: 2015-05-22; view: 2105; Нарушение авторских прав