
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Розрахунок воднеподібних атомів за Бором
|
|
Вивчення спектра випромінювання видимого діапазону водню дозволило Бальмеру описати його за допомогою емпіричної формули
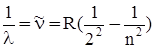 , (6)
, (6)
де 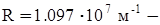 стала Рідберга,
стала Рідберга, 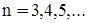 ,
, 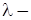 довжина хвилі,
довжина хвилі, 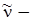 хвильове число. Формула (6) називається серіальною формулою Бальмера-Рідберга.
хвильове число. Формула (6) називається серіальною формулою Бальмера-Рідберга.
В результаті досліджень розсіювання речовиною 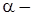 частинок, Резерфорд запропонував планетарну модель будови атомів, за якою у центрі воднеподібного атома знаходиться заряджене ядро з додатним зарядом Ze, а навколо нього на кругових орбітах рухаються Z електронів,
частинок, Резерфорд запропонував планетарну модель будови атомів, за якою у центрі воднеподібного атома знаходиться заряджене ядро з додатним зарядом Ze, а навколо нього на кругових орбітах рухаються Z електронів, 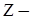 порядковий номер атома в таблиці Менделєєва. Для того щоб теоретично описати планетарну модель найпростішого атома, яким є атом водню, Н. Бор у 1913 установив три принципи існування такої моделі, сутність яких зводиться до такого.
порядковий номер атома в таблиці Менделєєва. Для того щоб теоретично описати планетарну модель найпростішого атома, яким є атом водню, Н. Бор у 1913 установив три принципи існування такої моделі, сутність яких зводиться до такого.
1. Усупереч класичній теорії, за якою заряджена частинка, що рухається із прискоренням, повинна випромінювати, електрони атома, рухаючись прискорено на колових орбітах, не випромінюють електромагнітні хвилі. Такі орбіти Бор назвав стаціонарними.
2. При переході електронів з одної стаціонарної орбіти з більшою енергією 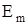 на іншу з меншою енергією
на іншу з меншою енергією 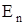 атом випромінює електромагнітні хвилі з частотою
атом випромінює електромагнітні хвилі з частотою
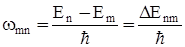 , (2)
, (2)
де 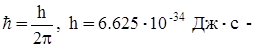 стала Планка.
стала Планка.
При співударяннях атомів з іншими частинками чи опроміненні їх світлом вони поглинають енергію
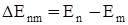 . (3)
. (3)
причому 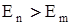 .
.
3. Електрон, що рухається по стаціонарній орбіті, має дискретні значення моменту імпульсу, величини яких, пропорційні цілому числу сталої 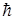
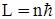 .
.
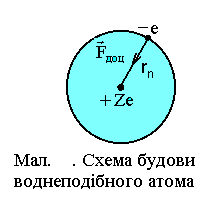 Наведені принципи дозволили Н.Бору з класичної точки зору розрахувати радіуси стаціонарних орбіт та відповідні їм енергії воднеподібних атомів.
Наведені принципи дозволили Н.Бору з класичної точки зору розрахувати радіуси стаціонарних орбіт та відповідні їм енергії воднеподібних атомів.
Розрахунок орбіт та енергій воднеподібних атомів. За постулатами Бора можна одержати спектр енергії та радіуси стаціонарних орбіт воднеподібних атомів (атомів з одним електроном на зовнішній орбіті й зарядом ядра Ze).
З правила квантування орбіт (1) знайдемо, що
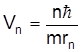 . (4)
. (4)
Бор вважав, що електрон у воднеподібній системі рухається під дією кулонівської сили взаємодії електрона з ядром, яке має заряд Ze
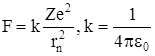 .
.
Ця сила є доцентровою і рівняння другого закону Ньютона 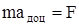 , де
, де 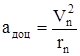 , буде мати вигляд
, буде мати вигляд
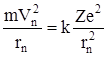 . (5)
. (5)
Підставляючи (4) у (5), одержимо
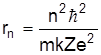 . (6)
. (6)
Електрон має повну енергію, що складається з кінетичної енергії 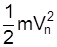 та потенціальної енергії
та потенціальної енергії 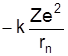 , тобто повна енергія
, тобто повна енергія
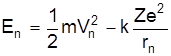 . (7)
. (7)
З (5) можна одержати
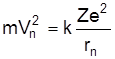 , (8)
, (8)
а (7) та (8) дають
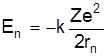 . (9)
. (9)
Підставляючи (6) у (9) одержимо
 |
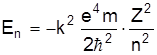 . (10)
. (10)
Вираз (7) можна представити у вигляді
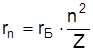 , (11)
, (11)
а вираз (10) у виді
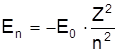 . (12)
. (12)
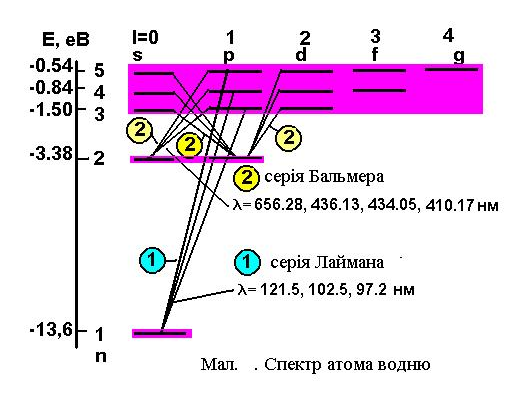
Вирази (11-12), одержані Бором, співпадають із квантово-механічними виразами (4-5). Спектр енергій для атома водню представлено на малюнку.
Для заданого n, стани атома водню в залежності від імпульсу (квантове число l) класифікуються умовними позначеннями
| l | |||||
| стан | s | p | d | f | g |
Випромінювання та поглинання світла атомом відбувається з певними обмеженнями, які ще називають правилами відбору. Виявляється, що при переходах електрона між енергетичними рівнями, у першому наближенні, повинно відбуватися таке обмеження на зміну азимутального квантового числа l
Dl=±1,
яке пов’язане із законом збереження імпульсу, коли враховуються імпульси атома й фотона. Таким чином в атомі можливі переходи
nsÛmp, npÛmd і т.п.
Використовуючи правило частот, можна записати
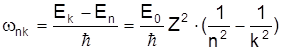 . (15)
. (15)
Вираз для довжини хвилі випромінювання має вид
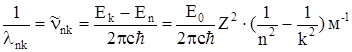 ,
,
або
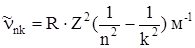 , (16)
, (16)
 де стала Рідберга записується так
де стала Рідберга записується так

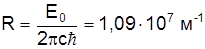 . (17)
. (17)
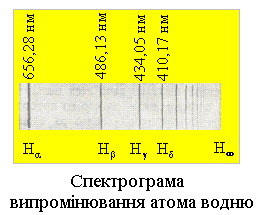
Теорія атома водню, створена Н.Бором, була першим кроком до квантової теорії атомів та молекул, яка має в основі рівняння руху елементарних частинок Шредінгера. Спектр випромінювання атома водню представлено на спектрограмі.
Date: 2015-05-17; view: 922; Нарушение авторских прав