
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Энтальпия. Энтальпией термодинамического тела называют сумму внутренней энергии u и произведения pv
|
|
Энтальпией термодинамического тела называют сумму внутренней энергии u и произведения pv.
i = и + pv.
Дифференцируя данное соотношение получим: di = du + pdv + vdp,
или du + pdv = di - vdp.
На основе первого закона термодинамики dq = du + pdv последнее соотношение перепишется в виде:
dq = di - vdp,или dq = dh + dlt,
где dlt - есть дифференциал технической работы (dlt = - vdp).
Полученное уравнение является также второй формулировкой первого закона термодинамики, используя понятия энтальпии и технической работы.
Величина i может также рассматриваться как параметр состояния термодинамического тела наряду с ранее введенными p, v, T, и. Физический смысл величины i может пояснен на основе уравнения dq = di - vdp, которое для процесса p = const запишется как:
dqp = di. (86)
Откуда следует, что di есть элементарное количество теплоты, подведенное к термодинамическому телу в процессе постоянного давления.
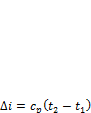
Изменение энтальпии в любом процессе определяется только начальным и конечным состояниями тела и не зависит от характера процесса.
Энтропия является функцией состояния, поэтому её изменение в термодинамическом процессе определяется только начальными и конечными значениями параметров состояния. Изменение энтропии в основных термодинамических процессах:
в изохорном 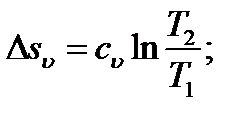
в изобарном 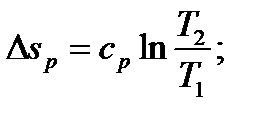
в изотермическом 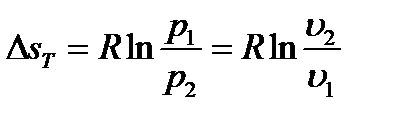
в адиабатном 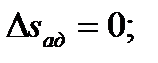
в политропном

Date: 2015-05-09; view: 936; Нарушение авторских прав