
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретические основы. Второе начало термодинамики отражает качественную сторону процессов и устанавливает их направленность
|
|
Второе начало термодинамики отражает качественную сторону процессов и устанавливает их направленность. Этот закон утверждает: «Невозможен процесс, имеющим единственным своим результатом полное превращение теплоты в работу». Из этого закона следует, что невозможно создать вечный двигатель второго рода, в котором теплота полностью превращается в работу. Этот закон отражает принцип существования таких понятий как: абсолютная температура, энтропия, принцип возрастания энтропии.
энтропия – это параметр состояния, изменение которого происходит при обмене энергией в форме теплоты. Энтропию нельзя измерить каким-либо прибором, как и внутреннюю энергию. Принцип существования энтропии используется при анализе обратимых (равновесных) процессов и состоит в утверждении или обосновании существования энтропии как функции состояния. Он гласит: «Для каждой термодинамической системы существует функция состояния (энтропия), изменение которой происходит под действием энергии, подводимой или отводимой в форме теплоты». Для обратимых процессов уравнение запишется в виде:
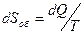 , [Дж/K)],
, [Дж/K)], 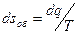 ,
, 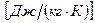
Принцип возрастания энтропии используется при анализе необратимых (реальных) процессов. Для необратимых процессов:
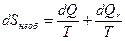 ,
,
здесь dQ – элементарное количество теплоты при внешнем теплообмене, dQr – элементарное количество теплоты, обусловленное необратимостью (реальностью) процесса. В любом необратимом процессе величина dQr>0.
Общее уравнение второго закона термодинамики примет вид:
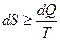
Второй закон термодинамики не позволяет определить меру необратимость (dQr/T), не противоречит закону сохранения энергии, как для обратимых, так и необратимых процессов. Он определяет одностороннюю направленность самопроизвольных необратимых процессов в односторонние необратимые превращения энергии, которые их (процессы) сопровождают
Date: 2015-05-08; view: 1228; Нарушение авторских прав