
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретические основы. Первое начало термодинамики представляет собой количественное выражение закона сохранения и превращения энергии
|
|
Первое начало термодинамики представляет собой количественное выражение закона сохранения и превращения энергии. Этот закон утверждает, что невозможен процесс возникновения ил исчезновения энергии: «Энергия изолированной системы при всех изменениях этой системы сохраняет постоянную величину». Этот закон носит всеобщий характер и используется всюду, где возникает необходимость в определении количества теплоты и работы. Из этого закона, в частности следует вывод о невозможности построения вечного двигателя первого рода, который в состоянии производить работу без получения энергии извне.
Из первого закона термодинамики следует, что каждая термодинамическая система обладает внутренней энергией. Эта функция состояния возрастает на величину подведенной теплоты и убывает на величину совершенной системой внешней работы.
В общем случае аналитическая запись первого закона имеет вид:
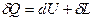 [Дж]
[Дж]
Возможны частные случаи, когда:
- 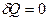 , то
, то 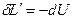 , без подвода теплоты от среды работа совершается телом за счет уменьшения его внутренней энергии.
, без подвода теплоты от среды работа совершается телом за счет уменьшения его внутренней энергии.
- 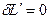 , то
, то 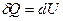 , вся подведенная от среды теплота затрачивается на увеличение внутренней энергии тела.
, вся подведенная от среды теплота затрачивается на увеличение внутренней энергии тела.
- 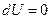 , то
, то 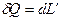 , вся подведенная теплота от среды, затрачивается на совершение телом работы.
, вся подведенная теплота от среды, затрачивается на совершение телом работы.
Для удельных величин уравнение примет вид:
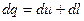 [Дж/кг]
[Дж/кг]
Политропный процесс – термодинамический процесс изменения состояния физической системы, в течение которого сохраняется постоянство теплоемкости. Уравнение политропного процесса имеет вид: 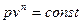 .
.
Политропный процесс обобщает всю совокупность основных термодинамических процессов.
| Процесс | 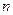
| 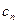
|
изохорный 
| 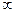
| 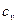
|
изобарный 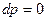
| 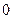
| 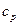
|
изотермический 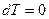
| 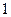
| 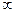
|
адиабатный 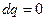
| 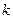
| 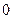
|
Давления обратно пропорциональны объемам в степени 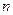 :
: 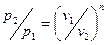
Коэффициент политропы 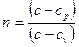 считается для отдельно взятого процесса величиной постоянной
считается для отдельно взятого процесса величиной постоянной 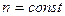 значение которой могут изменятся
значение которой могут изменятся 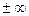 .
.
При известный параметрах состояния: 
Работа расширения в политропном процессе:
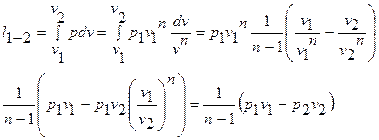
Используя уравнение состояния 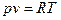 и соотношения:
и соотношения:
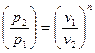 ;
; 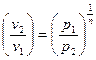 ;
; 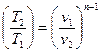 ;
; 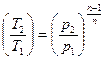 ,
,
можно получить приведенные соотношения для работы расширения в адиабатном процессе:
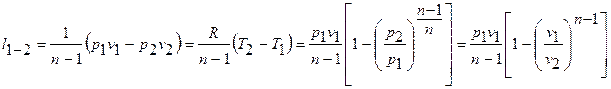
Изменение внутренней энергии в политропном процессе: 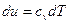
При 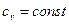 для двух значений температур (
для двух значений температур (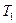 и
и 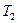 ):
): 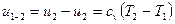
Изменение энтальпии в политропном процессе: 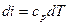
При 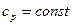 для двух значений температур (
для двух значений температур (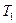 и
и 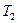 ):
): 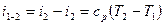
Количество теплоты в политропном процессе: 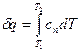
При 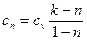 и для двух значений температур (
и для двух значений температур (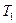 и
и 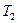 ):
): 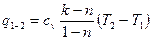
Изменение энтропии в политропном процессе: 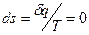
Энтропия в политропном процессе определится по зависимости: 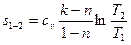
Date: 2015-05-08; view: 734; Нарушение авторских прав