
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Решение. Данные для решения задачи берем из справочника: S, Дж/(моль×К) Теплоемкость, Дж/(моль×К) Ср a СO
|
|
Данные для решения задачи берем из справочника:
| S, Дж/(моль×К) | Теплоемкость, Дж/(моль×К) | ||||
| Ср | a | 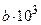
| 
| ||
| СO | 197,55 | 29,14 | 28,41 | 4,1 | -0,46 |
| Cl2 | 222,98 | 33,93 | 37,03 | 0,67 | -2,85 |
| COCl2 | 283,64 | 57,76 | 67,15 | 12,03 | -9,04 |
Рассмотрим два варианта расчета:
Ø Без учета зависимости теплоемкости от температуры:
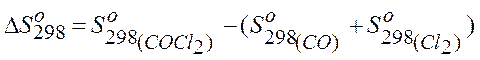
(коэффициенты не учитываем, т.к. они все равны единице);
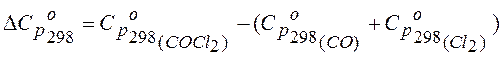
Тогда, 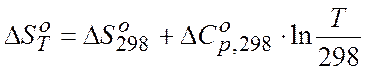
| Температура, К |
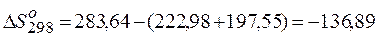 Дж/К Дж/К
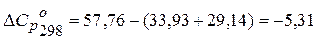 Дж/К Дж/К
|
| 400 | 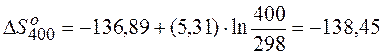 Дж Дж
|
| 1400 | 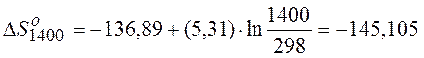 Дж Дж
|
Ø С учетом зависимости теплоемкости от температуры:
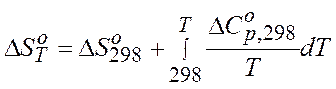 ,
,
где 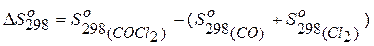 ,
,
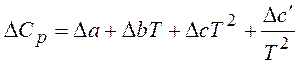 ,
,
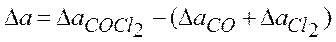
т.е. формула для расчета 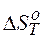 :
:
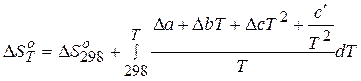 ,
,
после интегрирования получаем:
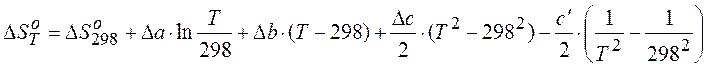
| Температура, К | 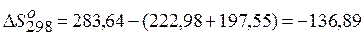 Дж/К Дж/К
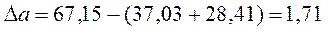 Дж/К Дж/К
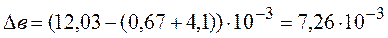 Дж/К Дж/К
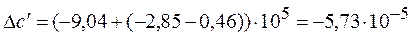 Дж/К Дж/К
|
| 400 | 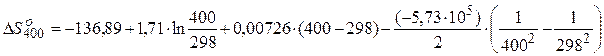 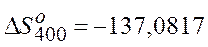 Дж Дж
|
| 1400 | 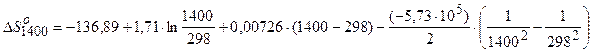
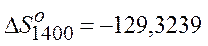 Дж Дж
|
ПОСТУЛАТ ПЛАНКА
Постулат Планка
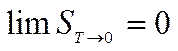 .
.
Его формулировка:
При абсолютном нуле энтропия правильно образованного кристалла любого элемента или соединения в чистом состоянии равна нулю, а при любом другом состоянии вещества его энтропия больше нуля.
Следствие: теплоемкость химически однородного кристалла при абсолютном нуле равна нулю.
На основании этого постулата можно рассчитать абсолютную энтропию для вещества при какой – либо температуре, если известны теплоемкости этих веществ от абсолютного нуля до нужной нам температуры, а также тепловые эффекты и температуры всех фазовых переходов (если они происходят в данном температурном интервале):
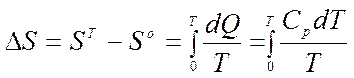
т.к.  ,
,  .
.
Если в интервале от 0 до Т имеется какой – либо фазовый переход с теплотой перехода lпер., и температурой перехода Тпер., то
 ,
,
где С/р – теплоемкость более высокотемпературной модификации.
Если при интересующей нас температуре вещество находится в жидком состоянии, то
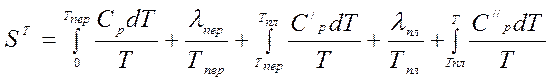 .
.
Например, для воды зависимость S от Т будет иметь следующий вид. Следует отметить, что и при абсолютном нуле некоторые составляющие энтропии, обуславливаемые спином ядра и изотопным эффектом, не становятся равными нулю, поэтому постулат Планка носит условный характер.
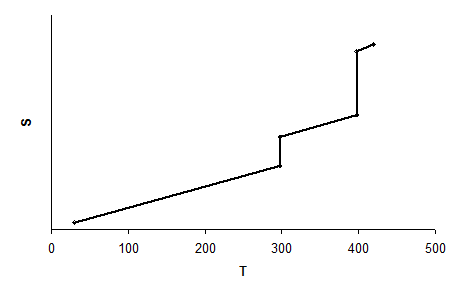
Рис. 1
Date: 2015-05-04; view: 734; Нарушение авторских прав