
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Теоретическая часть
|
|
Лабораторная работа № 4.
Жесткость воды. Определение карбонатной жесткости воды.
Цель работы: Познакомиться с методами определения и способами устранения жесткости воды.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ.
Большое влияние на качество воды оказывает содержащиеся в ней соли кальция магния и железа, которые и обуславливают жесткость воды. Природная вода является жесткой (в большинстве случаев), а жесткая вода непригодна, как известно, для многих технологических процессов, поэтому определение и устранение жесткости воды является очень существенным. Жесткость воды бывает временной и постоянной. Временная, или карбонатная жесткость воды обусловлена содержанием в воде гидрокарбонатов кальция, магния и железа. Постоянная, или некарбонатная жесткость воды обуславливается присутствием в воде сульфатов, хлоридов, нитратов и др. растворимых солей кальция и магния. Общая жесткость это сумма карбонатной и некарбонатной жесткости. Количественно жесткость определяется суммой молярных концентраций эквивалентов ионов кальция и магния, выраженных в миллимоль на литр.
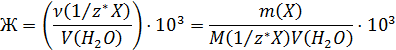
По величине жесткости природную воду делят на:
· Очень мягкую – до 1.5 ммоль/л,
· Мягкую – от 1.5 до 4 ммоль/л,
· Средней жесткости – от 4 до 8 ммоль/л,
· Жесткую – от 8 до 12 ммоль/л,
Очень жесткую – свыше 12 ммоль/л.
В зависимости от конкретных условий требования к жесткости воды могут быть различными. Для умягчения воды использую следующие методы:
1. Термический метод – применим для устранения карбонатной (временной) жесткости. Заключается в обычном кипячении, при котором гидрокарбонаты металлов разрушаются, образуя труднорастворимые вещества.
2. Реагентный метод – к воде добавляются различные химические вещества(реагенты), которые осаждают ионы кальция и магния и тем самым смягчают воду. Этот метод более универсален, так как применим для устранения и карбонатной и некарбонатной жесткости.
3. Ионообменный метод – широко применяется в промышленности. Жесткость воды устраняют с помощью ионитов (ионообменных смол) – сложных веществ, способных связывать содержащиеся в воде ионы: катионы (катиониты) или анионы(аниониты).
Вывод: В ходе данного эксперимента был изучен и закреплен один из методов определения карбонатной жесткости воды – метод титрования и найдено значение жесткости воды. Кроме того были рассмотрены различные способы устранения жесткости воды.
| <== предыдущая | | | следующая ==> |
| Комментарий 145 | | |
Date: 2015-11-13; view: 408; Нарушение авторских прав