
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Физико-химические свойства пластовых вод
|
|
Минерализация воды характеризует содержание в ней растворённых солей в г/л. В пластовых водах всегда растворено некоторое количество солей. По степени минерализации пластовые воды делятся на четыре типа:
- - рассолы (Q>50 г/л);
- - солёные (10<Q<50 г/л);
- - солоноватые (1<Q<10 г/л);
- - пресные (Q£1 г/л).
Минерализация пластовой воды растёт с глубиной залегания пластов.
В пластовой воде содержатся ионы растворённых солей:
- - анионы: OH–; Cl–; SO42–; CO32–; HCO3–;
- - катионы: H+; K+; Na+; NH4+; Mg2+; Ca2+; Fe3+;
- - ионы микроэлементов: I–; Br–;
- - коллоидные частицы SiO2; Fe2O3; Al2O3;
- - нафтеновые кислоты и их соли.
Больше всего в воде содержится хлористых солей, до 80-90% от общего содержания солей. В количественном отношении катионы солей пластовых вод располагаются в следующий ряд: Na+; Ca2+; Mg2+; K+; Fe3+.
Большое значение на растворимость солей и увеличение их концентрации в пластовых водах оказывает температура и парциальное давление СО2. Максимальная растворимость СаСО3 в воде наблюдается при 0оС, с возрастанием температуры она падает. Максимальная растворимость гипса (СаSО4·2Н2О) в воде наблюдается при 40оС. С дальнейшим возрастанием температуры она уменьшается. С увеличением парциальное давление СО2 растворимость СаСО3 возрастает. Уменьшение пластового давления усиливает процесс выпадения солей СаСО3 и др. Изменение термобарической обстановки в пласте даже при небольшой минерализации пластовых вод влияет на растворимость солей и выпадение их.
По типу растворённых в воде солей различают хлоркальциевые (хлоркальциево-магниевые) и гидрокарбонатные (гидрокарбонатно-натриевые, щелочные) пластовые воды. Тип пластовой воды определяется анионом. Гидрокарбонатный тип воды определяется солями угольной кислоты, необходимо наличие карбонат - CO32–, или бикарбонат - HCO3–аниона. Соли всех остальных кислот относятся к хлоркальциевому типу. В основном, это соли соляной кислоты – хлориды (Cl–).
Соли пластовых вод влияют и определяет её жёсткость. Жёсткостью называется суммарное содержание растворённых солей двухвалентных катионов: кальция, магния и железа.
Жёсткость различают временную (карбонатную) и постоянную (некарбонатную). Временная жёсткость или карбонатная (Жк) обусловлена содержанием в воде карбонатов или гидрокарбонатов двухвалентных металлов: кальция, магния, железа.
Постоянная жёсткость или некарбонатная (Жнк) обусловлена наличием в воде сульфатов или хлоридов (или соли других кислот) двухвалентных металлов: кальция, магния, железа.
Общая жёсткость воды определяется как сумма карбонатной и некарбонатной:
Жо = Жк + Жнк (2.39)
Жёсткость воды оценивается содержанием в ней солей в миллиграмм эквивалентах на литр  .
.
Жк, Жнк оценивают как сумму жесткостей всех i-ых ионов (∑gi):
Жо = Sgi (2.40)
Жесткость иона оценивается отношением массы иона к его эквиваленту:
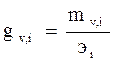 , (2.41)
, (2.41)
где mvi – концентрация i-го иона в воде (мг/л);
эi – эквивалент i-го иона.
Эквивалент иона оценивается отношением молекулярной массы иона (МI) к его валентности (n):
 , (2.42)
, (2.42)
где Мi – молекулярная масса иона;
n – валентность иона.
Природные воды в зависимости от содержания в них двухвалентных катионов кальция, магния, железа подразделяются на следующие типы:
- - очень мягкая вода – до 1,5 мг-экв./л;
- - мягкая вода – 1,5-3,0 мг-экв./л;
- - умеренно жёсткая вода – 3,0-6,0 мг-экв./л;
- - жёсткая вода – более 6 мг-экв./л.
Жесткость пластовой воды и ее тип по жесткости определяется экспериментально-расчетным путем (см. разд. "Практикум для самостоятельной работы").
Временную (карбонатную) жёсткость можно устранить термическим методом, длительным кипячением или химическим методом – добавлением гидроксида кальция Са(ОН)2. В обоих случаях выпадает в осадок карбонат кальция СаСО3.
Постоянную жёсткость устраняют химическим способом с помощью добавления соды или щёлочи.
Содержание водородных ионов в воде определяется показателем концентрации водородных ионов (рН), который равен отрицательному логарифму концентрации ионов водорода:
 , (2.43)
, (2.43)
где Сн+ – концентрация ионов водорода.
Показатель рН характеризует активную часть ионов водорода, которая образовалась в результате диссоциации молекул воды.
В зависимости от рН воды подразделяются на:
- - нейтральные (рН=7);
- - щелочные (pH>7);
- - кислые (p<7).
Поскольку константа диссоциации воды зависит от температуры и давления, то эти параметры влияют на величину рН (см. раздел "Практикум для самостоятельной работы"). С возрастанием температуры рН уменьшается и это обстоятельство необходимо учитывать при закачке воды в пласт.
Плотность пластовых вод сильно зависит от минерализации, т.е. содержания растворённых солей. В среднем плотность пластовой воды изменяется в диапазоне: 1010-1210 кг/м3, однако встречается и исключение - 1450 кг/м3. Пластовые воды месторождений нефтей и газоконденсатов Томской области имеют небольшую плотность: для мезозойских месторождений → 1007 – 1014 кг/м3; для палеозойских → 1040 – 1048 кг/м3; сеноманские воды → 1010 – 1012 кг/м3;
Вязкость воды в пластовых условиях зависит, в основном, от температуры и минерализации. С возрастанием минерализации вязкость возрастает. Наибольшую вязкость имеют хлоркальциевые воды по сравнению с гидрокарбонатными и они приблизительно в 1,5-2 раза больше вязкости чистой воды. С возрастанием температуры вязкость уменьшается. От давления вязкость зависит двояко: в области низких температур (0-40оС) с возрастанием давления вязкость уменьшается, а в области высоких температур (выше 40оС) возрастает.
Тепловое расширение воды характеризуется коэффициентом теплового расширения:
 . (2.44)
. (2.44)
Из формулы следует, что коэффициент теплового расширения воды (Е) характеризует изменение единицы объёма воды при изменении её температуры на 1°С. По экспериментальным данным в пластовых условиях он колеблется в пределах (18-90)×10-5 1/°С. С увеличением температуры коэффициент теплового расширения возрастает, с ростом пластового давления – уменьшается.
Коэффициент сжимаемости воды характеризует изменение единицы объёма воды при изменении давления на единицу:
 . (2.45)
. (2.45)
Коэффициент сжимаемости воды изменяется для пластовых условий от 3,7×10-10 до 5,0×10-10 Па-1. При наличии растворённого газа он увеличивается, и приближённо может оцениваться по формуле:
bвг = bв (1+0,05×S), (2.46)
где S – количество газа, растворённого в воде, м3/м3.
Объёмный коэффициент пластовой воды характеризует отношение удельного объёма воды в пластовых условиях к удельному объёму воды в стандартных условиях:
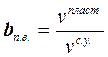 . (2.47)
. (2.47)
Увеличение пластового давления способствует уменьшению объёмного коэффициента, а рост температуры – увеличению. Объёмный коэффициент изменяется в пределах 0,99-1,06.
Соли пластовых вод – электролиты. Электролитом называются химические соединения, которые при взаимодействии с растворителем полностью или частично диссоциируют на ионы. Электрические свойства имеют ионную природу, и пластовая вода проявляет электрические свойства. Электропроводность пластовых вод имеет широкое применение.
Удельная электропроводность (χ) характеризует количество электричества, которое протекает в 1 секунду через 1 см2 поперечного сечения раствора электролита (S) при градиенте электрического поля в 1 в (R) на 1 см длины (L). Удельная электропроводность обратно пропорционально связана с удельным сопротивлением раствора ρ:
χ = L / (RS), χ =1/ρ. (2.48)
Удельная электропроводность имеет размерность в системе СИ [ом· м]-1, в системе СГС [ом·см]-1. С увеличением минерализации и полярности удельная электропроводность растет. Удельная электропроводность изменяется в диапазонах: у речной воды = 10-1 – 10-2; пластовой воды = 10-1 – 1; морской воды = 3 – 4; воды с 5% содержанием NaCl = 6,6; воды с 20% содержанием NaCl = 20; нефтей = 0,5 · 10-7 – 0,5 · 10-6; газоконденсатов = 10-10 – 10-16 [ом· м]-1 .
Вода, находясь в контакте с нефтью, частично в ней растворяется. Коэффициент растворимости нефти в воде зависит от наличия в воде полярных составляющих. Чем легче нефть, тем меньше в ней растворено воды. Нефти парафинового основания содержат мало воды. С ростом в нефти содержания ароматических углеводородов и гетероатомных соединений, растворимость воды в нефти растёт.
За счёт растворения воды в нефти происходят изменения в зоне водонефтяного контакта. Чёткой границы вода-нефть не существует ("зеркало" не образуется). За счёт растворения воды в нефти и диспергирования их друг в друга образуется так называемая "переходная зона", высота которой зависит от величины полярности нефти.
Date: 2015-12-10; view: 885; Нарушение авторских прав