
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Концентрация растворов
|
|
Концентрацией раствора называется количество растворенного вещества, содержащееся в определенном количестве или в определенном объеме раствора или растворителя.
В химии наиболее употребимы следующие способы выражения концентрации.
Процентная концентрация. Показывает число граммов растворенного вещества, содержащихся в 100 г раствора. Например, 15%-ный водный раствор соли – это такой раствор, в 100 г которого содержится 15 г соли и 85 г воды.
Молярная концентрация (молярность). Показывает число молей растворенного вещества, содержащихся в 1 л раствора, обозначается моль/л или формулой вещества, заключенной в квадратные скобки. Например, [NaOH]=2 моль/л – это раствор, содержащий 2 моля (или 80 г) гидроксида натрия в одном литре раствора.
Молярная концентрация эквивалентов. Показывает число молей эквивалентов растворенного вещества, содержащихся в 1 л раствора, обозначается С эк. Например, С эк H2SO4=0,1моль экв/л – это раствор Н2SO4 , содержащий 0,1 моля эквивалентов серной кислоты (или 4,9 г) в 1 л раствора.
Эквивалентом (обозначается буквой Э) называют реальную или условную частицу вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим способом эквивалентна одному иону водорода в кислотно-основных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях.
Эквивалент кислоты равен молярной массе кислоты, деленной на ее основность, т.е. на число атомов водорода в молекуле кислоты, способных замещаться на металл.
Эквивалент основания равен молярной массе основания, деленной на валентность металла.
Эквивалент оксида равен молярной массе оксида, деленной на произведение числа атомов элемента, входящих в состав молекулы, и валентности этого элемента.
Эквивалент соли равен молярной массе соли, деленной на произведение валентности металла и числа атомов металла в ее молекуле.
Например:
моль экв. Н2SO4 (М=98 г/моль) равен 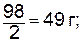
моль экв. Са(ОН)2 (М=74 г/моль) равен 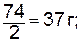
моль экв. Al2O3 (М=102 г/моль) равен 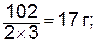
моль экв. Al2(SO4)3 (М=342 г/моль) равен 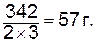
Растворы с молярной концентрацией эквивалентов широко применяются при проведении реакций между растворенными веществами. Пользуясь этой концентрацией, легко заранее рассчитать, в каких объемных соотношениях должны быть смешаны растворенные вещества, для того чтобы они прореагировали без остатка. Согласно закону эквивалентов количества веществ, вступающих в реакцию, пропорциональны их эквивалентам:
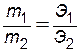 .
.
Следовательно, для реакции всегда нужно брать такие объемы растворов, которые содержали бы одинаковое число молей эквивалентов растворенных веществ. При одинаковой молярной концентрации растворов объемы реагирующих веществ пропорциональны их С эк. Если объемы затрачиваемых на реакцию растворов обозначить через V 1 и V 2 , а их молярные концентрации эквивалентов через С эк.1 и С эк.2, то зависимость между этими величинами выразится отношением:
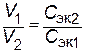
|
или  , ,
| (5.2) |
т.е. объемы реагирующих веществ обратно пропорциональны молярным концентрациям их эквивалентов.
На основании этих зависимостей можно не только вычислить необходимые для проведения реакций объемы растворов, но и по объемам затраченных на реакцию растворов находить их концентрации.
Титр. Показывает количество граммов растворенного вещества, содержащееся в 1 мл раствора. Обозначается буквой Т.
Зная титр раствора, легко вычислить его молярную концентрацию эквивалента, и наоборот:

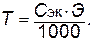
Моляльная концентрация (моляльность). Показывает число молей растворенного вещества, содержащееся в 1000 г растворителя, обозначается С m:
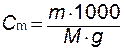 , ,
|  (5.3) (5.3)
|
где m – количество растворенного вещества, 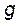 – количество растворителя, г; M – мольная масса растворенного вещества, г/моль.
– количество растворителя, г; M – мольная масса растворенного вещества, г/моль.
Date: 2015-10-19; view: 628; Нарушение авторских прав