
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Исследование минерализатов на наличие соединений марганца
|
|
Ионы марганца, содержащиеся в минерализатах, определяют при помощи реакций с периодатом калия и персульфатом аммония. После окисления ионов марганца этими реактивами образуются перманганат-ионы, имеющие фиолетовую окраску. Обе реакции являются специфичными для обнаружения ионов марганца, так как катионы других металлов при окислении указанными реактивами не дают фиолетовой окраски.
Реакция с периодатом калия КIO 4. При взаимодействии ионов марганца с периодатом калия образуется темно-красный осадок. Образование этого осадка происходит главным образом в сильно разбавленных растворах соединений марганца. В присутствии фосфатов не образуется этот осадок, а происходит окисление ионов марганца Mn 2+ до MnO 4 -:
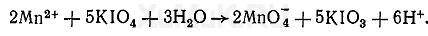
Выполнение реакции. В пробирку вносят 1 мл минерализата, 4 мл воды, 1 мл насыщенного раствора дигидрофосфата натрия и 0,2 г периодата калия. После нагревания пробирки на кипящей водяной бане в течение 20 мин при наличии ионов марганца в минерализате раствор приобретает красно-фиолетовую или розовую окраску. Предел обнаружения: 0,1 мкг марганца в 1 мл. Граница обнаружения: 0,02 мг марганца в 100 г биологического материала.
Реакция с персульфатом аммония. В зависимости от условий выполнения реакции персульфат аммония может окислять ионы марганца с образованием различных соединений. При кипячении в кислой среде без катализаторов персульфат аммония окисляет ионы марганца до марганцовистой кислоты Н 2 MnO 4:
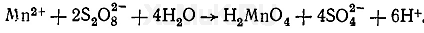
В щелочной среде без катализаторов персульфат аммония окисляет ионы марганца до MnО 2:
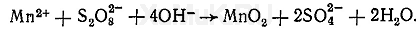
В присутствии катализаторов (соли серебра или смесь 0,1 н. растворов нитратов кобальта, никеля и ртути) персульфат аммония окисляет ионы марганца до перманганат-ионов MnO 4 -:
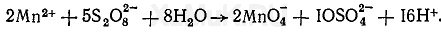
Ионы железа (III), которые могут быть в минерализатах в больших количествах, затрудняют распознавание окраски перманганатионов. Для маскировки ионов железа прибавляют фосфаты, которые с ионами железа образуют бесцветный комплекс [Fe(РО 4) 2 ] 3-.
Реакции окисления ионов марганца персульфатом мешают восстановители, обесцвечивающие перманганат-ионы, а также хлориды, бромиды и другие ионы, которые осаждают ионы серебра, являющиеся катализатором.
На протекание реакции персульфата с ионами марганца влияет рН среды. Эта реакция хорошо протекает в 3 н. кислоте. При недостаточной кислотности образуется темно-бурый осадок марганцовистой кислоты Н 2 MnO 4, а при большом избытке кислоты может происходить восстановление перманганат-ионов персульфатом:
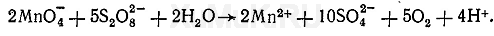
Выполнение реакции. В пробирку вносят 1 мл минерализата, 4 мл воды, 1 мл насыщенного раствора дигидрофосфата натрия. Смесь нагревают на кипящей водяной бане в течение 5—6 мин. К горячему раствору прибавляют 1 каплю 10%-го раствора нитрата серебра и 0,5 г персульфата аммония. Смесь енова нагревают в течение нескольких минут (до разложения избытка персульфата). При наличии ионов марганца в минерализате появляется красно-фиолетовая или розовая окраска. Предел обнаружения: 0,1 мкг марганца в 1 мл. Граница обнаружения: 0,1 мг марганца в 100 г биологического материала.
Date: 2015-09-24; view: 509; Нарушение авторских прав